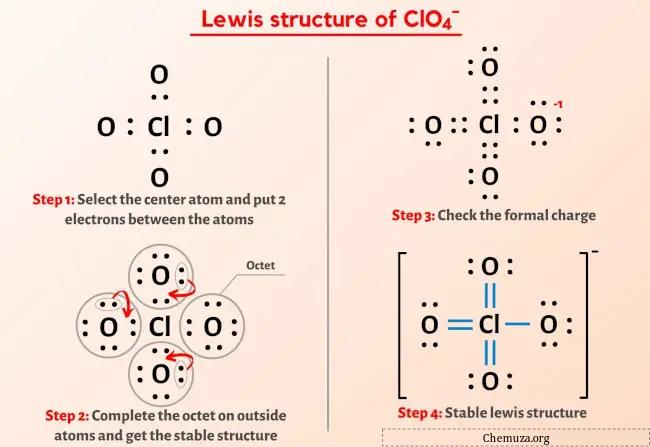
Dus je hebt de afbeelding hierboven al gezien, toch?
Ik zal het bovenstaande beeld kort toelichten.
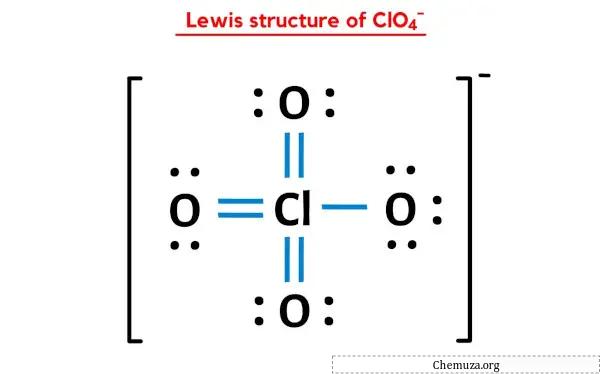
De ClO4- (perchloraation) Lewis-structuur heeft een chlooratoom (Cl) in het midden dat wordt omgeven door vier zuurstofatomen (O). Er zijn 3 dubbele bindingen en 1 enkele binding tussen het chlooratoom (Cl) en elk zuurstofatoom (O). Er zijn 2 alleenstaande paren op dubbelgebonden zuurstofatomen (O) en 3 alleenstaande paren op enkelvoudig gebonden zuurstofatomen (O).
Als je niets hebt begrepen van de bovenstaande afbeelding van de ClO4-Lewis-structuur, blijf dan bij mij en je krijgt de gedetailleerde stap-voor-stap uitleg over het tekenen van een Lewis-structuur van ClO4 – ion .
Laten we dus verder gaan met de stappen voor het tekenen van de Lewis-structuur van het ClO4-ion.
Stappen voor het tekenen van de ClO4-Lewis-structuur
Stap 1: Zoek het totale aantal valentie-elektronen in het ClO4-ion
Om het totale aantal valentie-elektronen in het ClO4-ion (perchloraation) te vinden, moet je allereerst de valentie-elektronen kennen die zowel in het chlooratoom als in het zuurstofatoom aanwezig zijn.
(Valentie-elektronen zijn de elektronen die aanwezig zijn in de buitenste baan van elk atoom.)
Hier zal ik je vertellen hoe je gemakkelijk de valentie-elektronen van chloor en zuurstof kunt vinden met behulp van een periodiek systeem .
Totale valentie-elektronen in ClO4-ion
→ Valentie-elektronen gegeven door het chlooratoom:

Chloor is een element in groep 17 van het periodiek systeem. [1] Daarom zijn de valentie-elektronen in chloor 7 .
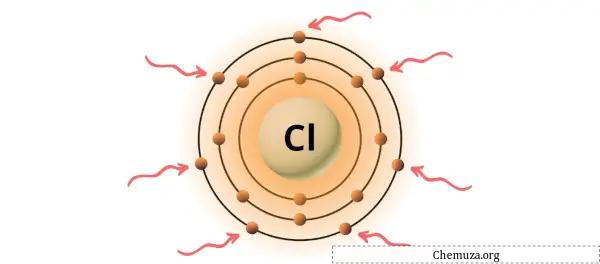
Je kunt de 7 valentie-elektronen in het chlooratoom zien, zoals weergegeven in de afbeelding hierboven.
→ Valentie-elektronen gegeven door het zuurstofatoom:

Zuurstof is een element in groep 16 van het periodiek systeem. [2] Daarom zijn de valentie-elektronen in zuurstof 6 .
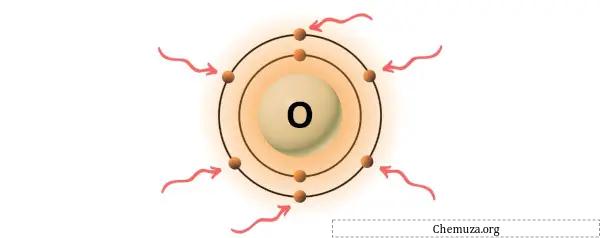
Je kunt de 6 valentie-elektronen zien die aanwezig zijn in het zuurstofatoom, zoals weergegeven in de afbeelding hierboven.
Dus,
Totaal valentie-elektronen in ClO4-ion = valentie-elektronen gedoneerd door 1 chlooratoom + valentie-elektronen gedoneerd door 4 zuurstofatomen + 1 extra elektron toegevoegd vanwege negatieve lading = 7 + 6(4) + 1 = 32 .
Stap 2: Selecteer het centrale atoom
Om het centrale atoom te selecteren, moeten we onthouden dat het minst elektronegatieve atoom in het centrum blijft.
Het gegeven ion is hier ClO4-ion en het bevat chlooratomen (Cl) en zuurstofatomen (O).
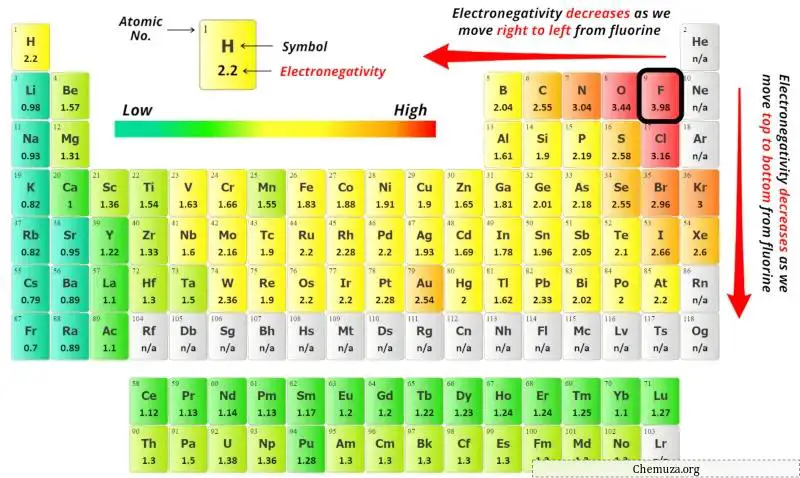
Je kunt de elektronegativiteitswaarden van het chlooratoom (Cl) en het zuurstofatoom (O) zien in het periodiek systeem hierboven.
Als we de elektronegativiteitswaarden van chloor (Cl) en zuurstof (O) vergelijken, dan is het chlooratoom minder elektronegatief .
Hier is het chlooratoom (Cl) het centrale atoom en de zuurstofatomen (O) de buitenste atomen.
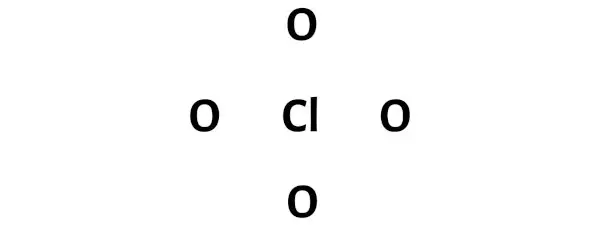
Stap 3: Verbind elk atoom door er een paar elektronen tussen te plaatsen
Nu moet je in het ClO4-molecuul de elektronenparen tussen het chlooratoom (Cl) en de zuurstofatomen (O) plaatsen.
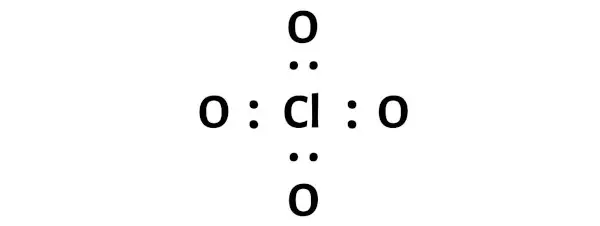
Dit geeft aan dat chloor (Cl) en zuurstof (O) chemisch aan elkaar gebonden zijn in een ClO4-molecuul.
Stap 4: Maak de externe atomen stabiel
In deze stap moet je de stabiliteit van de externe atomen controleren.
Hier in de schets van het ClO4-molecuul kun je zien dat de buitenste atomen zuurstofatomen zijn.
Deze externe zuurstofatomen vormen een octet en zijn daarom stabiel.
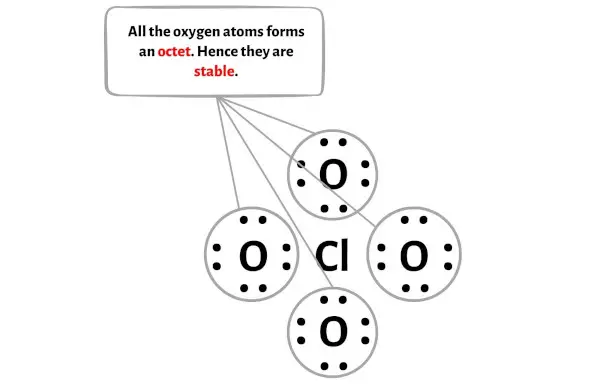
Bovendien hebben we in stap 1 het totale aantal valentie-elektronen in het ClO4-ion berekend.
Het ClO4-ion heeft in totaal 32 valentie-elektronen en al deze valentie-elektronen zijn in het bovenstaande diagram gebruikt.
Er zijn dus geen paren elektronen meer om op het centrale atoom te houden.
Laten we nu verder gaan met de volgende stap.
Stap 5: Controleer de stabiliteit van de Lewis-structuur
Nu ben je bij de laatste stap gekomen waarin je de stabiliteit van de Lewis-structuur van het ClO4-ion moet controleren.
De stabiliteit van de Lewis-structuur kan worden geverifieerd met behulp van een formeel ladingsconcept .
Kortom, we moeten nu de formele lading van de chlooratomen (Cl) en de zuurstofatomen (O) in het ClO4-molecuul vinden.
Om de formele belasting te berekenen, moet u de volgende formule gebruiken:
Formele lading = Valentie-elektronen – (bindende elektronen)/2 – Niet-bindende elektronen
In de onderstaande afbeelding ziet u het aantal bindende elektronen en niet-bindende elektronen voor elk atoom van het ClO4-molecuul.
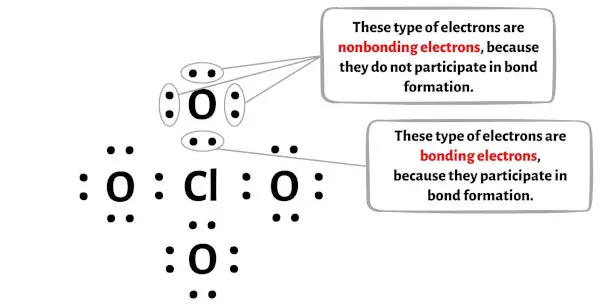
Voor het chlooratoom (Cl):
Valentie-elektronen = 7 (omdat chloor in groep 17 zit)
Bindende elektronen = 8
Niet-bindende elektronen = 0
Voor het zuurstofatoom (O):
Valentie-elektronen = 6 (omdat zuurstof in groep 16 zit)
Bindende elektronen = 2
Niet-bindende elektronen = 6
| Formele beschuldiging | = | valentie-elektronen | – | (Bindende elektronen)/2 | – | Niet-bindende elektronen | ||
| Kl | = | 7 | – | 8/2 | – | 0 | = | +1 |
| Oh | = | 6 | – | 2/2 | – | 6 | = | -1 |
Uit de bovenstaande formele ladingsberekeningen kun je zien dat het chlooratoom (Cl) een lading van +1 heeft, terwijl de zuurstofatomen een lading van -1 hebben.
Laten we deze ladingen dus op de respectieve atomen van het ClO4-molecuul houden.
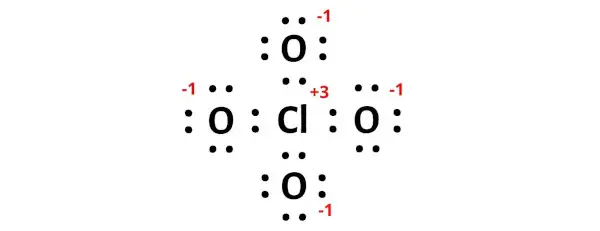
De afbeelding hierboven laat zien dat de Lewis-structuur van ClO4 niet stabiel is.
We moeten deze ladingen dus minimaliseren door de elektronenparen van de zuurstofatomen naar het chlooratoom te verplaatsen.
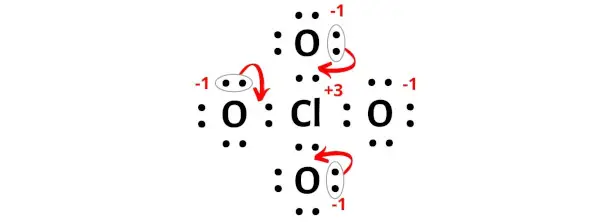
Nadat de elektronenparen van het zuurstofatoom naar het chlooratoom zijn verplaatst, worden de ladingen op het centrale chlooratoom en op drie zuurstofatomen nul. En het is een stabielere Lewis-structuur. (zie afbeelding hieronder).
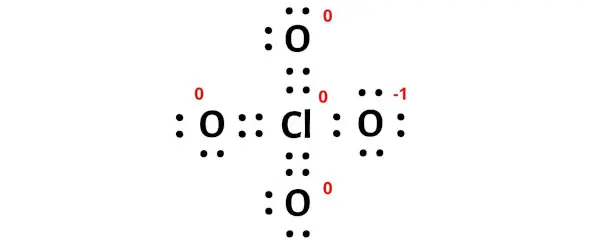
Er blijft een -ve lading op het zuurstofatoom achter, wat een formele -1 lading geeft op het ClO4-molecuul.
Deze totale lading van -1 op het ClO4-molecuul wordt weergegeven in de onderstaande afbeelding.
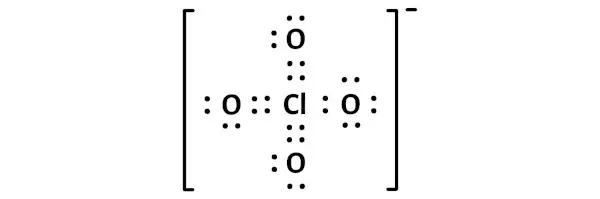
In de bovenstaande Lewis-puntstructuur van het ClO4-ion kun je elk paar bindende elektronen (:) ook voorstellen als een enkele binding (|). Als je dit doet, krijg je de volgende Lewis-structuur van het ClO4-ion.
Ik hoop dat je alle bovenstaande stappen volledig hebt begrepen.
Voor meer oefening en een beter begrip kun je andere Lewis-structuren proberen die hieronder worden vermeld.
Probeer (of bekijk in ieder geval) deze Lewis-structuren voor een beter begrip:
