Piperidine is een cyclisch amine dat bestaat uit een zesring met één stikstofatoom. Het wordt gebruikt in farmaceutische producten, pesticiden en als oplosmiddel voor organische reacties.
| IUPAC-naam | Piperidine |
| Moleculaire formule | C₅H₁₁N |
| CAS-nummer | 110-89-4 |
| Synoniemen | Hexahydropyridine, Azacyclohexaan, Cyclopentimine |
| InChi | InChI=1S/C5H11N/c1-2-4-6-5-3-1/h6H,1-5H2 |
Eigenschappen van piperidine
Piperidine-formule
De chemische formule voor hexahydropyridine is C₅H₁₁N. Het bestaat uit vijf koolstofatomen, elf waterstofatomen en één stikstofatoom. De formule vertegenwoordigt de exacte samenstelling van elementen in een hexahydropyridinemolecuul.
Piperidine Molaire Massa
De molaire massa van hexahydropyridine wordt berekend door de atoommassa’s van de samenstellende elementen op te tellen. Voor hexahydropyridine (C₅H₁₁N) bedraagt de molaire massa ongeveer 85,15 gram per mol. Deze waarde is nuttig voor het bepalen van de hoeveelheid hexahydropyridine in een bepaald monster.
Piperidine Kookpunt
Hexahydropyridine heeft een kookpunt van ongeveer 106 graden Celsius. Deze temperatuur vertegenwoordigt het punt waarop de vloeibare vorm van hexahydropyridine in een gas verandert. Het kookpunt is belangrijk bij verschillende industriële processen waarbij hexahydropyridine wordt gebruikt.
Smeltpunt van piperidine
Het smeltpunt van hexahydropyridine is ongeveer -7 graden Celsius. Het geeft de temperatuur aan waarbij vast hexahydropyridine overgaat in de vloeibare toestand. Het smeltpunt is een cruciaal kenmerk voor de hantering en opslag van hexahydropyridine in verschillende toepassingen.
Piperidinedichtheid g/ml
De dichtheid van hexahydropyridine is ongeveer 0,86 gram per milliliter (g/ml). Dichtheid verwijst naar de massa van een stof per volume-eenheid. Deze eigenschap is waardevol bij het bepalen van de hoeveelheid hexahydropyridine die nodig is voor specifieke toepassingen.
Piperidine-molecuulgewicht
Het molecuulgewicht van hexahydropyridine is ongeveer 85,15 gram per mol. Het vertegenwoordigt de som van de atoomgewichten van alle atomen die aanwezig zijn in een hexahydropyridinemolecuul. Het molecuulgewicht is een essentiële parameter die wordt gebruikt bij verschillende chemische berekeningen en reacties waarbij hexahydropyridine betrokken is.
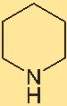
Structuur van piperidine
Hexahydropyridine heeft een ringstructuur die bestaat uit een zesring die één stikstofatoom en vijf koolstofatomen bevat. De rangschikking van atomen in deze structuur beïnvloedt de chemische eigenschappen en het gedrag van hexahydropyridine. Door de structuur te begrijpen, kunnen we de reactiviteit en interacties ervan bestuderen.
Oplosbaarheid van piperidine
Hexahydropyridine is oplosbaar in water en organische oplosmiddelen. Het vormt waterstofbruggen met watermoleculen vanwege de aanwezigheid van een stikstofatoom. Door de oplosbaarheid van hexahydropyridine kan het worden gebruikt als oplosmiddel in verschillende chemische processen en als reagens bij organische synthese.
| Verschijning | Heldere vloeistof |
| Soortelijk gewicht | 0,862 g/ml |
| Kleur | Kleurloos |
| Geur | Sterk, ammoniakaal |
| Molaire massa | 85,15 g/mol |
| Dikte | 0,862 g/ml |
| Fusie punt | -7°C |
| Kookpunt | 106°C |
| Flitspunt | 9°C |
| oplosbaarheid in water | Mengbaar |
| Oplosbaarheid | Oplosbaar in polaire oplosmiddelen zoals water en organische oplosmiddelen |
| Dampdruk | 7,4 mmHg bij 25°C |
| Dampdichtheid | 2,95 (lucht=1) |
| pKa | 11.24 |
| pH | Basis |
Veiligheid en gevaren van piperidine
Hexahydropyridine brengt verschillende veiligheidsrisico’s met zich mee en moet met voorzichtigheid worden gehanteerd. Het is irriterend voor de huid, ogen en luchtwegen. Direct contact kan brandwonden of irritatie veroorzaken. Inademing van hexahydropyridinedampen kan ademhalingsproblemen en longschade veroorzaken. Het is brandbaar en kan met lucht explosieve mengsels vormen. Bij verhitting kunnen giftige dampen vrijkomen, waaronder stikstofoxiden. Bij het werken met hexahydropyridine zijn voldoende ventilatie en persoonlijke beschermingsmiddelen, zoals handschoenen en een veiligheidsbril, vereist. Bovendien moet het worden opgeslagen in een koele, goed geventileerde ruimte, uit de buurt van ontstekingsbronnen. Een goede training en kennis van veiligheidsprotocollen zijn essentieel bij het hanteren van hexahydropyridine om potentiële risico’s te minimaliseren.
| Gevarensymbolen | Schedel en gekruiste knekels, vlam, bijtend |
| Beveiligingsbeschrijving | Vermijd contact met huid en ogen. Gebruik in een goed geventileerde ruimte. Verwijderd houden van ontstekingsbronnen. |
| VN-identificatienummers | UN-nr. 2879 (voor piperidine) |
| HS-code | 2933.99.80 |
| Gevarenklasse | Klasse 6.1 (Giftige stoffen) |
| Verpakkingsgroep | Verpakkingsgroep II |
| Toxiciteit | Piperidine is giftig en kan ernstige gevolgen voor de gezondheid veroorzaken. Inhalatie, inslikken of huidabsorptie moeten worden vermeden. Langdurige of herhaalde blootstelling kan orgaanschade of ademhalingsproblemen veroorzaken. Tijdens hantering en opslag moeten passende beschermende maatregelen worden genomen. |
Piperidinesynthesemethoden
Er zijn verschillende methoden voor het synthetiseren van hexahydropyridine.
Een veelgebruikte methode is de reactie van 1,5-dihalopentaan met ammoniak . In dit proces vervangt de aminogroep (-NH2) de halogeenatomen door nucleofiele substitutie te ondergaan. Een andere methode omvat de reductie van pyridine met waterstofgas over een katalysator, zoals palladium of platina. Deze reductiereactie zet pyridine om in hexahydropyridine door twee waterstofatomen aan het stikstofatoom toe te voegen.
Bovendien levert de hydrogenering van pyridiniumzouten of pyridinederivaten hexahydropyridine op. Dit hydrogeneringsproces vindt plaats onder hoge druk en temperatuur met behulp van een geschikte katalysator. Een andere benadering omvat de reactie van 2,5-dimethylpyrrool met acetyleen gevolgd door hydrogenering, wat hexahydropyridine oplevert.
Bovendien kan reductieve aminering van cyclopentanon of zijn derivaten met ammoniak of primaire aminen ook leiden tot de vorming van hexahydropyridine. Deze reactie omvat de toevoeging van een aminogroep aan de ketongroep, gevolgd door reductie om de hexahydropyridinering te vormen.
Over het geheel genomen maken deze synthetische methoden het mogelijk om hexahydropyridine te verkrijgen uit verschillende grondstoffen, waardoor de productie ervan in verschillende industriële en onderzoeksomgevingen mogelijk wordt. De keuze voor de methode is afhankelijk van factoren als de beschikbaarheid van grondstoffen, het gewenste rendement en specifieke toepassingseisen.
Gebruik van piperidine
Hexahydropyridine heeft vanwege zijn veelzijdige eigenschappen verschillende toepassingen in verschillende industrieën. Enkele veel voorkomende toepassingen van hexahydropyridine zijn onder meer:
- Farmaceutische industrie: De farmaceutische industrie gebruikt hexahydropyridine als bouwsteen om veel farmaceutische verbindingen te synthetiseren. Het speelt een cruciale rol bij de productie van medicijnen zoals antihistaminica, antipsychotica, analgetica en antivirale middelen.
- Agrochemicaliën: Hexahydropyridine verbetert de effectiviteit van pesticiden en insecticiden omdat fabrikanten het bij hun productie gebruiken. Het verbetert de ongediertebestrijding en verbetert de gewasopbrengsten.
- Organische synthese: Hexahydropyridine werkt als katalysator of oplosmiddel bij organische reacties en vergemakkelijkt condensatie-, cyclisatie- en oxidatieprocessen. Het maakt de synthese van verschillende chemische verbindingen mogelijk.
- Rubberindustrie: In de rubberindustrie functioneert hexahydropyridine als vulkanisatieversneller. Het verbetert de mechanische sterkte, elasticiteit en duurzaamheid van rubberproducten door de verknoping van rubberpolymeren te verbeteren.
- Oplosmiddel: Hexahydropyridine dient als oplosmiddel voor verschillende organische verbindingen, waardoor het nuttig is bij extractieprocessen, chemische reacties en als medium voor farmaceutische formuleringen. Het lost een breed scala aan stoffen op.
- Corrosieremmer: Hexahydropyridine functioneert als een corrosieremmer en beschermt metalen oppervlakken tegen afbraak. Het vormt een beschermende film op het metaal, waardoor corrosiereacties worden vertraagd of voorkomen.
- Laboratoriumreagens: Onderzoekers gebruiken hexahydropyridine als reagens in laboratoriumexperimenten, vooral in de organische chemie. Het neemt actief deel aan reacties, zoals N-alkyleringen en ringopeningsreacties, waardoor de synthese van gewenste verbindingen wordt vergemakkelijkt.
- Chemische tussenproducten: Hexahydropyridinederivaten dienen als tussenproducten bij de productie van verschillende chemicaliën, waaronder kleurstoffen, geurstoffen en oppervlakteactieve stoffen.
Deze toepassingen demonstreren de diverse en waardevolle rollen die hexahydropyridine speelt in meerdere industrieën, en dragen bij aan de ontwikkeling van farmaceutische producten, landbouwchemicaliën, rubberproducten en meer.
Vragen:
Vraag: Wat is de pKa van piperidine?
A: De pKa van hexahydropyridine is ongeveer 11,24.
Vraag: Wat is de pKa van diethylmalonaat?
A: De pKa van diethylmalonaat is ongeveer 12,5.
Vraag: Waarom is het geconjugeerde zuur van morfoline zuurder dan het geconjugeerde zuur van piperidine?
A: Morfolineconjugaatzuur is zuurder vanwege de aanwezigheid van een elektronenzuigend zuurstofatoom in de morfolinering, dat de positieve lading van het conjugaatzuur stabiliseert.
Vraag: Hoe dibenzofulvene-piperidine-adduct verwijderen?
A: Dibenzofulveen-piperidine-adduct kan worden verwijderd door geschikte zuiveringstechnieken zoals oplosmiddelextractie, chromatografie of herkristallisatie, afhankelijk van de specifieke omstandigheden en gewenste zuiverheid.
Vraag: Wat is de rol van piperidine in de reactie die u hebt uitgevoerd?
A: Hexahydropyridine kan fungeren als katalysator, base of reagens, afhankelijk van de specifieke reactieomstandigheden en vereisten.
Vraag: Is piperidine mengbaar met THF?
A: Ja, hexahydropyridine is mengbaar met THF (tetrahydrofuran).
Vraag: Wat gebeurt er als piperidine en DMF worden gecombineerd?
A: Wanneer hexahydropyridine en DMF (dimethylformamide) worden gecombineerd, kunnen ze mogelijk verschillende reacties ondergaan, afhankelijk van de reactieomstandigheden en de aanwezigheid van andere reactanten of katalysatoren.
Vraag: Wat is de pH van een oplossing die 0,120 M in piperidine en 0,079 M in het chloridezout is?
A: De pH van de oplossing zou afhangen van de pKa van het hexahydropyridine en de dissociatie van zijn chloridezout, en zou aanvullende berekeningen vereisen om de exacte pH-waarde te bepalen.
Vraag: Hoe de piperidinering breken?
A: Het breken van de hexahydropyridinering kan worden bereikt met verschillende methoden, zoals oxidatie-, reductie- of ringopeningsreacties, met behulp van geschikte reagentia en reactieomstandigheden.
Vraag: Basiciteit van pyridine of piperidine?
A: Hexahydropyridine is over het algemeen basischer dan pyridine vanwege de aanwezigheid van een meer nucleofiel stikstofatoom in de ring, waardoor het gemakkelijker een proton kan doneren.
