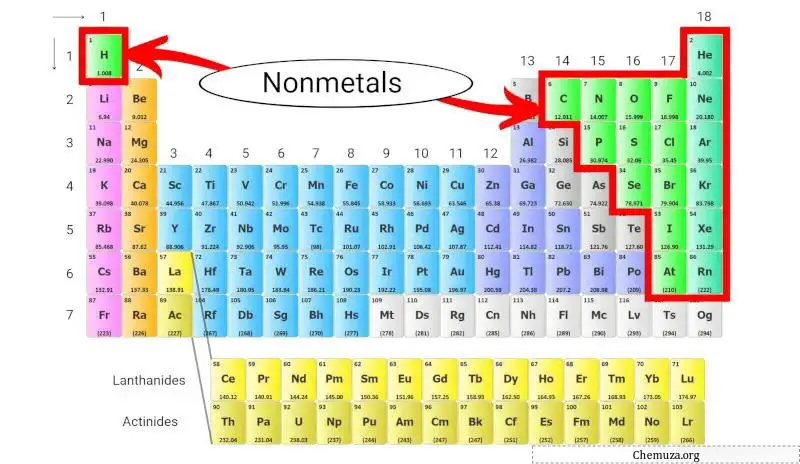
Niet-metalen zijn een groep elementen die de eigenschappen van metalen missen, zoals een hoge elektrische geleidbaarheid en glans. Deze niet-metalen bevinden zich aan de rechterkant van het periodiek systeem , met uitzondering van waterstof .
Niet-metalen kunnen in verschillende vormen worden aangetroffen, waaronder gassen zoals zuurstof en chloor , vloeistoffen zoals broom en vaste stoffen zoals zwavel en koolstof . [1]
Laten we belangrijkere dingen over niet-metalen bekijken.
Wat zijn niet-metalen precies?
Niet-metalen zijn elementen die de neiging hebben elektronen op te nemen tijdens chemische reacties, waarbij ze negatief geladen ionen of anionen vormen.
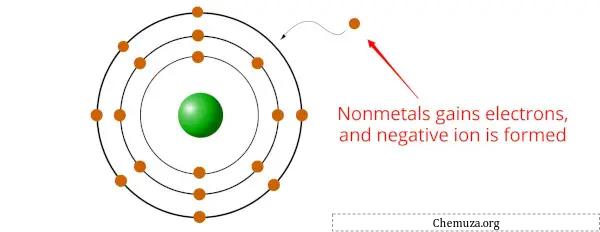
Dit komt omdat niet-metalen over het algemeen een hogere elektronegativiteit hebben dan metalen, [2] wat betekent dat ze een grotere aantrekkingskracht op elektronen hebben.
Wanneer niet-metalen zich binden met metalen , haalt het niet-metalen element een of meer elektronen uit het metaal om een stabiele verbinding te vormen.
Chloor krijgt bijvoorbeeld een elektron uit natrium om de ionische verbinding natriumchloride (NaCl) te vormen.
Er kan ook worden gezegd dat – Niet-metalen een groep chemische elementen zijn die niet de fysische en chemische eigenschappen van metalen hebben.
Laten we eens kijken naar de lijst met niet-metalen die aanwezig zijn in het periodiek systeem.
Lijst met niet-metalen die aanwezig zijn in het periodiek systeem
Hier is een lijst met niet-metalen die aanwezig zijn in het periodiek systeem:
- Waterstof (H)
- Helium (hij)
- Koolstof (C)
- Stikstof (N)
- Zuurstof (O)
- Fluoriet (F)
- Neon (Ne)
- Fosfor (P)
- Zwavel (S)
- Chloor (Cl)
- Argon (Ar)
- Seleen (Se)
- Broom (Br)
- Krypton (KR)
- Jodium (ik)
- Xenon (Xe)
- Astatijn (At)
- Radon (Rn)
Deze niet-metalen bevinden zich aan de rechterkant van het periodiek systeem, met uitzondering van waterstof, dat zich bovenaan het periodiek systeem bevindt, boven de alkalimetalen .
Toestand van niet-metalen (vast, vloeibaar of gasvormig?)
Niet-metalen kunnen in alle drie de toestanden van de materie voorkomen: vast, vloeibaar en gasvormig.
De toestand van een niet-metaal hangt af van de temperatuur- en drukomstandigheden waaraan het wordt blootgesteld.
Van alle niet-metalen op het periodiek systeem;
- 11 Niet-metalen bevinden zich bij kamertemperatuur in gasvormige toestand. [3]
- Broom (Br) is een niet-metaal dat bij kamertemperatuur in vloeibare toestand wordt aangetroffen.
- De rest van de niet-metalen zijn vaste stoffen bij kamertemperatuur.
Meest reactieve niet-metaal
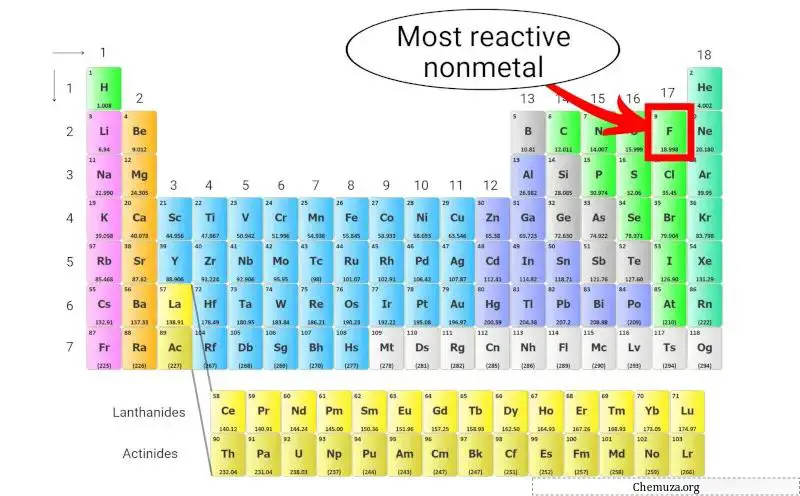
Fluor (F) is het meest reactieve niet-metaal in het periodiek systeem.
Maar waarom? Waarom is fluoride het meest reactief?
Dit komt omdat het de hoogste elektronegativiteit van alle elementen heeft, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen.
Fluor heeft zeven elektronen op het buitenste energieniveau en heeft een extra elektron nodig om zijn valentieschil te vullen en een stabiele configuratie te bereiken.
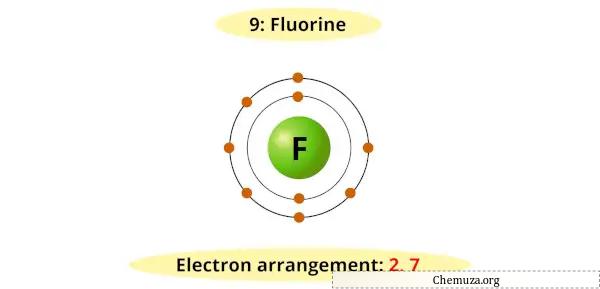
Daarom accepteert het gemakkelijk een elektron van andere elementen om een fluoride-ion (F-) te vormen.
Vanwege de hoge reactiviteit kan fluor explosief reageren met veel andere elementen en verbindingen, waaronder water, metalen en zelfs glas. [4]
Fluor is zo reactief dat het doorgaans wordt opgeslagen en vervoerd in gespecialiseerde containers die zijn gemaakt van materialen die bestand zijn tegen de corrosieve eigenschappen ervan.
Rol van niet-metalen in milieu- en industriële toepassingen
Niet-metalen worden vanwege hun unieke eigenschappen gebruikt in verschillende industriële processen en milieutoepassingen. Hier zijn enkele voorbeelden:
- Beheersing van luchtverontreiniging: Niet-metalen zoals stikstof en zuurstof spelen een cruciale rol bij het beheersen van luchtverontreiniging. Stikstofoxiden (NOx) zijn schadelijke verontreinigende stoffen die vrijkomen uit voertuigen en industriële processen. Niet-metaalhoudende katalysatoren worden gebruikt om NOx om te zetten in onschadelijke gassen zoals stikstof en water. Op dezelfde manier wordt zuurstof gebruikt in verbrandingsprocessen om schadelijke emissies te verminderen.
- Meststof: Stikstof, fosfor en zwavel zijn essentiële voedingsstoffen voor de plantengroei. Niet-metaalhoudende meststoffen zoals ammoniumnitraat en superfosfaat worden in de landbouw veel gebruikt om de gewasopbrengsten te verhogen.
- Batterijen: Niet-metalen elementen zoals zwavel, koolstof en lithium worden in batterijen gebruikt. Lithium-ionbatterijen worden vaak gebruikt in elektronische apparaten, elektrische voertuigen en systemen voor hernieuwbare energie.
- Waterzuivering: Niet-metalen zoals chloor en jodium worden vaak gebruikt als ontsmettingsmiddelen in waterzuiveringssystemen. Ze doden schadelijke bacteriën en virussen en maken water veilig om te drinken. [5]
- Chemische productie: Niet-metalen zoals zwavel en chloor worden veel gebruikt bij de productie van chemicaliën zoals zwavelzuur, zoutzuur en op chloor gebaseerde oplosmiddelen.
Samenvatting
Niet-metalen missen de eigenschappen van metalen, zoals een hoge elektrische geleidbaarheid en glans, en bevinden zich aan de rechterkant van het periodiek systeem, met uitzondering van waterstof. Ze bestaan in alle drie de toestanden van de materie, afhankelijk van de temperatuur- en drukomstandigheden.
Fluor is het meest reactieve niet-metaal vanwege zijn hoge elektronegativiteit en accepteert gemakkelijk een elektron van andere elementen om een fluoride-ion (F-) te vormen.
Niet-metalen worden op verschillende manieren gebruikt in milieu- en industriële toepassingen, waaronder de bestrijding van luchtverontreiniging, meststoffen, batterijen, waterzuivering en chemische productie.
