Nitroglycerine is een explosieve verbinding die medicinaal wordt gebruikt om angina pectoris te behandelen. Het ontspant de bloedvaten, verbetert de bloedcirculatie en vermindert pijn op de borst. Ga er uiterst voorzichtig mee om vanwege de volatiliteit ervan.
| IUPAC-naam | 1,2,3-trinitrooxypropan-2-ylnitraat |
| Moleculaire formule | C3H5N3O9 |
| CAS-nummer | 55-63-0 |
| Synoniemen | Glyceryltrinitraat, Trinitroglycerine, NG, Nitrospan, Nitrostat |
| InChi | InChI=1S/C3H5N3O9/c7-4(8)13-1-3(15-6(11)12)2-14-5(9)10/h3H,1-2H2 |
Eigenschappen van nitroglycerine
Nitroglycerine-formule
De formule voor trinitroglycerine is C3H5N3O9. Het bestaat uit drie koolstofatomen (C), vijf waterstofatomen (H), drie stikstofatomen (N) en negen zuurstofatomen (O). De moleculaire structuur van trinitroglycerine wordt gekenmerkt door de aanwezigheid van verschillende nitraatgroepen gekoppeld aan een glycerolmolecuul.
Nitroglycerine molaire massa
De molaire massa van trinitroglycerine is ongeveer 227,09 gram per mol. Het wordt berekend door de atoommassa’s van elk element in de chemische formule (C3H5N3O9) op te tellen. Molaire massa speelt een cruciale rol bij het bepalen van de hoeveelheid trinitroglycerine die nodig is voor verschillende toepassingen.
Kookpunt van nitroglycerine
Trinitroglycerine is een zeer vluchtige verbinding met een laag kookpunt. Het kookt rond de 55 graden Celsius (131 graden Fahrenheit). Door het lage kookpunt kan trinitroglycerine gemakkelijk van vloeistof in gas veranderen, wat bijdraagt aan de explosieve eigenschappen ervan.
Smeltpunt van nitroglycerine
Het smeltpunt van trinitroglycerine ligt rond de 13 graden Celsius (55 graden Fahrenheit). Door dit relatief lage smeltpunt kan trinitroglycerine bij kamertemperatuur in vloeibare vorm voorkomen. Vanwege de gevoeligheid voor hitte en schokken vereist het echter een zorgvuldige behandeling om onbedoelde ontploffing te voorkomen.
Dichtheid van nitroglycerine g/ml
De dichtheid van trinitroglycerine is ongeveer 1,6 gram per milliliter (g/ml). Dit betekent dat één milliliter trinitroglycerine 1,6 gram weegt. De relatief hoge dichtheid van trinitroglycerine draagt bij aan de stabiliteit ervan en zorgt voor gemakkelijke opslag en transport.
Nitroglycerine Moleculair gewicht
Het molecuulgewicht van trinitroglycerine is ongeveer 227,09 gram per mol. Het is de som van de atoomgewichten van alle atomen in een trinitroglycerinemolecuul. Het molecuulgewicht levert belangrijke informatie op voor chemische berekeningen en voor het bepalen van de hoeveelheid trinitroglycerine die nodig is voor verschillende toepassingen.
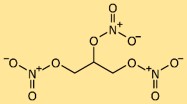
Structuur van nitroglycerine
De structuur van trinitroglycerine bestaat uit een glycerolmolecuul (propaan-1,2,3-triol) gekoppeld aan drie nitraatgroepen (-NO3). Nitraatgroepen zijn gebonden aan verschillende koolstofatomen in de glycerolskelet. Deze unieke moleculaire samenstelling draagt bij aan het explosieve karakter van trinitroglycerine.
Oplosbaarheid van nitroglycerine
Trinitroglycerine is oplosbaar in sommige organische oplosmiddelen zoals ethanol, aceton en ether. Het is echter slechts in geringe mate oplosbaar in water. Deze beperkte wateroplosbaarheid maakt orale toediening van trinitroglycerine moeilijk, en het wordt vaak toegediend via andere routes, zoals sublinguale tabletten of transdermale pleisters voor medische doeleinden.
| Verschijning | Gele vloeistof |
| Soortelijk gewicht | 1,6 g/ml |
| Kleur | Bleek geel |
| Geur | Lichte geur |
| Molaire massa | 227,09 g/mol |
| Dikte | 1,6 g/ml |
| Fusie punt | 13°C (55°F) |
| Kookpunt | 55°C (131°F) |
| Flitspunt | 30°C (86°F) |
| oplosbaarheid in water | Enigszins oplosbaar |
| Oplosbaarheid | Oplosbaar in organische oplosmiddelen zoals ethanol, aceton, ether |
| Dampdruk | 0,1 mmHg |
| Dampdichtheid | 8,2 (lucht = 1) |
| pKa | 7,7 (pKa1), 8,8 (pKa2), 9,3 (pKa3) |
| pH | Neutrale |
Veiligheid en gevaren van nitroglycerine
Trinitroglycerine brengt aanzienlijke veiligheidsrisico’s met zich mee vanwege het explosieve karakter ervan. Het is zeer gevoelig voor hitte, schokken en wrijving, waardoor het uiterst gevaarlijk is als het verkeerd wordt gebruikt. Het kan met grote kracht ontploffen en ernstig letsel of de dood veroorzaken. Bij het hanteren van nitroglycerine moeten strikte veiligheidsprotocollen worden gevolgd, inclusief het dragen van geschikte beschermende uitrusting en het bewaren ervan op een veilige, koele en droge plaats. Het is van cruciaal belang om vonken, open vuur of ontstekingsbronnen in de buurt te vermijden. Er moet bijzondere aandacht worden besteed aan transport en opslag om ongelukken te voorkomen en het risico op explosie te minimaliseren.
| Gevarensymbolen | Explosief, acuut giftig |
| Beveiligingsbeschrijving | Zeer explosief. Ga uiterst voorzichtig te werk. Vermijd hitte, vonken en open vuur. |
| VN-identificatienummers | UN 0143 (vloeistof) |
| HS-code | 2909.10.00 |
| Gevarenklasse | 1.1D (explosieven) |
| Verpakkingsgroep | PG II (Gemiddeld gevaar) |
| Toxiciteit | Giftig bij inslikken of inademen. |
Nitroglycerinesynthesemethoden
Verschillende methoden kunnen nitroglycerine synthetiseren.
Een gebruikelijke aanpak omvat de reactie tussen geconcentreerd salpeterzuur (HNO3) en glycerol (C3H8O3) . De reactie vindt plaats onder zorgvuldig gecontroleerde omstandigheden, meestal met toevoeging van zwavelzuur (H2SO4) als katalysator. Handhaaf een lage temperatuur en voeg langzaam glycerol toe aan een mengsel van geconcentreerd salpeterzuur en zwavelzuur om nitroglycerine te synthetiseren.
Een andere methode omvat het gebruik van gemengd zuur, een combinatie van salpeterzuur en zwavelzuur. Voeg glycerol toe aan het gemengde zuur terwijl u de temperatuur controleert tijdens de nitroglycerinesynthese.
Bij beide methoden werkt salpeterzuur als een oxidatiemiddel en reageert het met glycerol om nitroglycerine te vormen. Zwavelzuur helpt de reactie door voor een geschikte omgeving te zorgen en als katalysator te werken.
Het is belangrijk op te merken dat de synthese van nitroglycerine grote zorg en expertise vereist vanwege het zeer explosieve karakter ervan. Volg te allen tijde strikte veiligheidsmaatregelen om het risico op ongevallen tijdens het hele proces te minimaliseren.
Na de synthese wordt de resulterende nitroglycerine-oplossing vaak gezuiverd door wassen en filtratie om onzuiverheden te verwijderen.
Over het geheel genomen omvat de nitroglycerinesynthese een reeks chemische reacties die nauwkeurige controle en naleving van veiligheidsprotocollen vereisen om een succesvol en veilig proces te garanderen.
Gebruik van nitroglycerine
Trinitroglycerine heeft verschillende belangrijke toepassingen op verschillende gebieden vanwege zijn unieke eigenschappen. Hier zijn enkele belangrijke toepassingen van nitroglycerine:
- Anginabehandeling: Artsen gebruiken nitroglycerine gewoonlijk medicinaal om angina pectoris te verlichten en te voorkomen, een aandoening die pijn op de borst veroorzaakt als gevolg van een verminderde bloedtoevoer naar het hart. Het ontspant de bloedvaten, verbetert de bloedcirculatie en vermindert pijn op de borst.
- Explosieven: Trinitroglycerine is een hoofdingrediënt in veel explosieven. Zijn hoge explosieve kracht en gevoeligheid maken hem geschikt voor toepassingen zoals mijnbouw, bouw en militaire operaties.
- Industriële productie: Trinitroglycerine dient als voorloper voor de synthese van andere explosieve verbindingen, zoals dynamiet en TNT (trinitrotolueen). Deze stoffen worden veel gebruikt in de bouw-, steengroeve- en sloopindustrie.
- Pyrotechniek: Bij vuurwerk en pyrotechnische shows wordt nitroglycerine gebruikt om levendige en oogverblindende visuele effecten te creëren.
- Analytische chemie: Analytische chemici gebruiken nitroglycerine als standaardverbinding om de prestaties en effectiviteit van verschillende analytische instrumenten en methoden te bepalen.
- Stabilisatoren en stuwraketten: Het vindt toepassing in drijfgassen voor raketten en raketten, en levert de stuwkracht die nodig is voor ruimteverkenning en verdedigingssystemen.
- Artilleriegranaten: Fabrikanten verwerken nitroglycerine in artilleriegranaten om hun explosieve kracht en effectiviteit op het slagveld te verbeteren.
- Wetenschappelijk onderzoek: Laboratoria gebruiken nitroglycerine voor onderzoeksdoeleinden, waaronder onderzoek naar explosief gedrag, schokgolffysica en chemische reacties.
De verschillende toepassingen van nitroglycerine benadrukken het belang ervan op medisch, industrieel en wetenschappelijk gebied, maar met grote voorzichtigheid vanwege het explosieve karakter ervan.
Vragen:
Vraag: Waar wordt nitroglycerine voor gebruikt?
A: Trinitroglycerine ontspant de bloedvaten, verbetert de bloedcirculatie en helpt pijn op de borst (angina pectoris) te verminderen.
Vraag: Wat is nitroglycerine?
A: Trinitroglycerine is een explosieve verbinding die medicinaal wordt gebruikt om angina pectoris te behandelen en in explosieven voor verschillende industriële en militaire toepassingen.
Vraag: Waar wordt nitroglycerine voor gebruikt?
A: Trinitroglycerine wordt gebruikt voor de behandeling van angina pectoris, als een explosieve component, en in industrieën zoals de mijnbouw, de bouw en de pyrotechniek.
Vraag: Hoe werkt nitroglycerine?
A: Trinitroglycerine werkt door het vrijgeven van stikstofmonoxide, dat de gladde spieren ontspant, inclusief die in de bloedvaten, wat leidt tot een betere bloedstroom.
Vraag: Hoe werkt nitroglycerine in het lichaam?
A: In het lichaam wordt trinitroglycerine omgezet in stikstofmonoxide, dat de bloedvaten verwijdt en de werklast van het hart vermindert.
Vraag: Welke enkele binding in nitroglycerine is waarschijnlijk de kortste?
A: De enkele binding tussen koolstof en stikstof (CN) in trinitroglycerine is waarschijnlijk de kortste.
Vraag: Is nitroglycerine een bètablokker?
A: Nee, trinitroglycerine is geen bètablokker. Het behoort tot een klasse geneesmiddelen die nitraten worden genoemd.
Vraag: Welke enkele binding in nitroglycerine is het minst polair?
A: De enkele binding tussen koolstof en koolstof (CC) in trinitroglycerine is het minst polair.
Vraag: Hoe werd nitroglycerine gemaakt in het Verre Westen?
A: In het Oude Westen werd trinitroglycerine doorgaans gemaakt door glycerol onder gecontroleerde omstandigheden te mengen met geconcentreerde salpeter- en zwavelzuren.
Vraag: Hoe explodeert nitroglycerine?
A: Trinitroglycerine explodeert wanneer het wordt blootgesteld aan hitte, schokken of wrijving, wat resulteert in een snelle vrijgave van gas en een aanzienlijke toename van het volume en de druk.
Vraag: Hoe ruikt nitroglycerine?
A: Trinitroglycerine heeft een lichte geur, vaak omschreven als licht zoet of etherisch.
