Natriumnitraat (NaNO3) is een verbinding die in de voedingsindustrie veel als conserveermiddel wordt gebruikt. Het wordt ook gebruikt in meststoffen en explosieven vanwege zijn oxiderende eigenschappen.
| IUPAC-naam | Natriumnitraat |
| Moleculaire formule | NaNO3 |
| CAS-nummer | 7631-99-4 |
| Synoniemen | Chileense salpeter, kubieke Niter, natriumsalpeter |
| InChi | InChI=1S/NO3.Na/c2-1(3)4;/q-1;+1 |
Eigenschappen van natriumnitraat
Natriumnitraatformule
De chemische formule voor natriumnitraat is NaNO3. De formule vertegenwoordigt het aantal en de soorten atomen waaruit een natriumnitraatmolecuul bestaat. Dit geeft aan dat elk natriumnitraatmolecuul één natriumatoom, één stikstofatoom en drie zuurstofatomen bevat. De formule is belangrijk voor het begrijpen van de chemische eigenschappen van natriumnitraat en voor het gebruik ervan in verschillende toepassingen.
Natriumnitraat molaire massa
NaNO3 heeft een molaire massa van 84,9947 g/mol. Molaire massa is de massa van één mol van een stof en wordt berekend door de atoommassa’s van alle atomen in een molecuul bij elkaar op te tellen. NaNO3 bevat één Na-atoom, één N-atoom en drie O-atomen. De atoommassa’s van deze atomen zijn 22,98977 g/mol voor natrium, 14,00674 g/mol voor stikstof en 15,9994 g/mol voor zuurstof. Daarom wordt de molaire massa van NaNO3 als volgt berekend:
Molaire massa = (1 x 22,98977) + (1 x 14,00674) + (3 x 15,9994) = 84,9947 g/mol
Kookpunt van natriumnitraat
Het kookpunt van NaNO3 is 380°C (716°F). Kookpunt is de temperatuur waarbij een stof bij atmosferische druk overgaat van een vloeistof naar een gas. NaNO3 is een ionische verbinding met sterke intermoleculaire krachten die de deeltjes bij elkaar houden. Deze intermoleculaire krachten vereisen een grote hoeveelheid energie om te breken, en daarom is het kookpunt van NaNO3 relatief hoog.
Smeltpunt van natriumnitraat
NaNO3 heeft een smeltpunt van 308°C (586°F). Het smeltpunt is de temperatuur waarbij een stof bij atmosferische druk verandert van een vaste stof in een vloeistof. NaNO3 is een ionische verbinding met een kristalstructuur met sterke ionische bindingen tussen de deeltjes. Het verbreken van deze bindingen vergt een grote hoeveelheid energie. Daarom is het smeltpunt van NaNO3 relatief hoog.
Dichtheid van natriumnitraat g/ml
De dichtheid van NaNO3 is 2,257 g/ml. Dichtheid is de massa per volume-eenheid van een stof. NaNO3 is een witte kristallijne vaste stof met een relatief hoge dichtheid vanwege de dicht opeengepakte deeltjes. Het is belangrijk op te merken dat de dichtheid van NaNO3 kan variëren afhankelijk van factoren zoals temperatuur en druk.
Natriumnitraat Molecuulgewicht
Het molecuulgewicht van NaNO3 is 84,9947 g/mol. Het molecuulgewicht is de som van de atoomgewichten van alle atomen in een molecuul. Zoals eerder vermeld bevat NaNO3 één natriumatoom, één stikstofatoom en drie zuurstofatomen, die bijdragen aan het molecuulgewicht.
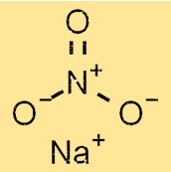
Structuur van natriumnitraat
NaNO3 heeft een kristalstructuur bestaande uit Na+- en NO3–ionen. Na+-kationen en NO3-anionen zijn gerangschikt in een netwerkstructuur die bij elkaar wordt gehouden door sterke ionische bindingen. De structuur van NaNO3 is belangrijk voor het begrijpen van de fysische en chemische eigenschappen ervan.
| Verschijning | Witte kristallen of poeder |
| Soortelijk gewicht | 2.257 g/cm3 bij 20°C |
| Kleur | Kleurloos |
| Geur | Geurloos |
| Molaire massa | 84,9947 g/mol |
| Dikte | 2.257 g/cm3 bij 20°C |
| Fusie punt | 308°C (586°F) |
| Kookpunt | 380°C (716°F) |
| Flitspunt | Niet toepasbaar |
| oplosbaarheid in water | 87g/100ml (20°C) |
| Oplosbaarheid | Oplosbaar in glycerol, ammoniak en waterstofperoxide. Onoplosbaar in alcohol. |
| Dampdruk | 0,003 mmHg bij 20°C |
| Dampdichtheid | Niet toepasbaar |
| pKa | -1,4 |
| pH | 7 (10% oplossing in water) |
Veiligheid en gevaren van natriumnitraat
NaNO3 kan verschillende gevaren voor de menselijke gezondheid en het milieu met zich meebrengen. Het is licht irriterend en kan bij contact huid- en oogirritatie veroorzaken. Inademing van NaNO3-stof kan ook irritatie van de luchtwegen veroorzaken. NaNO3 kan reageren met brandbare materialen en brand of explosies veroorzaken. Het is ook giftig voor in het water levende organismen en mag niet in waterwegen terechtkomen. NaNO3 moet met zorg worden gehanteerd en bij het hanteren ervan moet geschikte beschermende uitrusting worden gedragen. Het moet worden opgeslagen in een droge, goed geventileerde ruimte, uit de buurt van onverenigbare materialen. Ook moeten de juiste verwijderingsmethoden worden gevolgd om besmetting van het milieu te voorkomen.
| Gevarensymbolen | O, Xi |
| Beveiligingsbeschrijving | Vermijd contact met brandbare materialen, draag beschermende uitrusting en bewaar in een droge, goed geventileerde ruimte. Op de juiste manier weggooien. |
| VN-identificatienummers | UN1498 (watervrij) / UN1499 (gesmolten) |
| HS-code | 28342910 |
| Gevarenklasse | 5.1 (Oxidatiemiddel) |
| Verpakkingsgroep | III |
| Toxiciteit | LD50 (oraal, rat): 1260 mg/kg |
Methoden voor de synthese van natriumnitraat
Er zijn verschillende methoden om NaNO3 te synthetiseren, waaronder het laten reageren van salpeterzuur met natriumhydroxide of het laten reageren van salpeterzuur met natriumcarbonaat .
De eerste methode omvat het geleidelijk toevoegen van natriumhydroxideoplossing aan de salpeterzuuroplossing onder roeren totdat de pH 7-8 bereikt. De oplossing reageert en vormt NaNO3, dat een persoon kan verdampen en kristalliseren om de vaste verbinding te verkrijgen.
Een andere methode omvat de reactie van natriumcarbonaat met salpeterzuur . De persoon voegt natriumcarbonaat toe aan het salpeterzuur totdat het bruisen stopt, en verwarmt vervolgens het mengsel totdat de uitstoot van kooldioxide stopt. Vervolgens verdampen en kristalliseren ze de verkregen oplossing om NaNO3 te verkrijgen.
De productie van NaNO3 kan ertoe leiden dat het als bijproduct wordt verkregen door de productie van salpeterzuur of door oxidatie van ammoniak met een platinakatalysator.
Gebruik van natriumnitraat
NaNO3 heeft een breed scala aan industriële, agrarische en medische toepassingen vanwege zijn chemische en fysische eigenschappen. Enkele toepassingen van NaNO3 zijn onder meer:
- Meststof: Wordt vaak gebruikt als stikstofmeststof in de landbouw vanwege de hoge oplosbaarheid en snelle afgifte-eigenschappen.
- Voedselconserveermiddel: Gebruikt als voedselconserveermiddel om de groei van bacteriën en schimmels in vleeswaren zoals ham, spek en hotdogs te voorkomen.
- Glasproductie: Gebruikt als vloeimiddel bij de glasproductie om het smeltpunt te verlagen en de helderheid te verbeteren.
- Pyrotechniek: belangrijk ingrediënt bij de productie van vuurwerk en andere pyrotechnische apparaten vanwege de oxiderende eigenschappen ervan.
- Warmteoverdrachtsvloeistof: gebruikt als warmteoverdrachtsvloeistof in zonne-energiecentrales om thermische energie op te slaan en over te dragen.
- Medische toepassingen: Gebruikt bij de behandeling van angina pectoris, een hartaandoening die pijn op de borst veroorzaakt als gevolg van onvoldoende bloedtoevoer naar het hart.
- Industriële toepassingen: Wordt ook gebruikt bij de productie van kleurstoffen, bleekmiddelen en andere chemicaliën.
Vragen :
Vraag: Is natriumnitraat oplosbaar in water?
A: Ja, NaNO3 is zeer oplosbaar in water, met een oplosbaarheid van 91 gram per 100 milliliter water bij kamertemperatuur.
Vraag: Waar wordt natriumnitraat voor gebruikt?
A: NaNO3 wordt voor verschillende doeleinden gebruikt, waaronder kunstmest, voedselconserveermiddel, glasproductiestroom, pyrotechnisch oxidatiemiddel, warmteoverdrachtsvloeistof en in medische en industriële toepassingen.
Vraag: Is natriumnitraat een sterke elektrolyt?
A: Ja, NaNO3 is een sterke elektrolyt, wat betekent dat het volledig dissocieert in ionen wanneer het wordt opgelost in water, waardoor elektriciteit kan worden geleid.
Vraag: Is NaNO3 oplosbaar in water?
A: Ja, NaNO3 is zeer oplosbaar in water, met een oplosbaarheid van 91 gram per 100 milliliter water bij kamertemperatuur.
Vraag: Is NaNO3 oplosbaar?
A: Ja, NaNO3 is oplosbaar in water, maar het is onoplosbaar in sommige organische oplosmiddelen zoals ethanol en ether.
Vraag: Welk zout ontstaat er als NH4OH reageert met HNO3? KNO2, NaNO3, NH4NO3 of NH4NO2?
A: Het zout dat ontstaat wanneer NH4OH reageert met HNO3 is NH4NO3, ook bekend als ammoniumnitraat.
Vraag: Is NaNO3 een zuur of een base?
A: NaNO3 is een neutrale verbinding en noch een zuur, noch een base.
Vraag: Wat is NaNO3?
A: NaNO3 is de chemische formule voor natriumnitraat, een witte kristallijne vaste stof met diverse industriële, agrarische en medische toepassingen.
