Natriumcyanide is een zeer giftige verbinding die in verschillende industrieën wordt gebruikt. Er komen cyanide-ionen vrij die de cellulaire ademhaling verstoren, wat ernstige gezondheidsrisico’s en zelfs de dood tot gevolg kan hebben.
| IUPAC-naam | Natriumcyanide |
| Moleculaire formule | NaCN |
| CAS-nummer | 143-33-9 |
| Synoniemen | Cyanogran, natriumcyanide, cyanidezout, natriumcyanidezout |
| InChi | InChI=1S/CN.Na/c1-2;/h1H;/q-1;+1 |
Eigenschappen van natriumcyanide
Natriumcyanide-formule
De formule voor natriumcyanide is NaCN. Het bestaat uit een Na+ kation en een CN-anion. Deze chemische verbinding wordt veel gebruikt in verschillende industriële processen.
Natriumcyanide molaire massa
De molaire massa van NaCN wordt berekend door de atoommassa’s van de samenstellende elementen, natrium (Na) en koolstof (C) plus stikstof (N), op te tellen. De molaire massa van NaCN is ongeveer 49,01 gram per mol.
Kookpunt van natriumcyanide
NaCN heeft een kookpunt van ongeveer 1.496 graden Celsius. Bij deze temperatuur ondergaat de verbinding een faseverandering van een vloeistof naar een gas. Het is essentieel om voorzichtig met NaCN om te gaan vanwege de toxische aard ervan.
Natriumcyanide Smeltpunt
Het smeltpunt van NaCN ligt rond de 564 graden Celsius. Bij deze temperatuur verandert de vaste verbinding in de vloeibare toestand. Voorzichtigheid is geboden bij het hanteren van NaCN, aangezien dit ernstige gezondheidsrisico’s met zich meebrengt.
Dichtheid van natriumcyanide g/ml
De dichtheid van NaCN is ongeveer 1,6 gram per milliliter. Deze dichtheidswaarde geeft de massa van de stof per volume-eenheid aan. De hoge dichtheid van NaCN draagt bij aan de stabiliteit ervan en vergemakkelijkt het gebruik ervan in verschillende toepassingen.
Natriumcyanide Molecuulgewicht
Het molecuulgewicht van NaCN is ongeveer 49,01 gram per mol. Deze waarde vertegenwoordigt de som van de atoomgewichten van de samenstellende elementen. Het molecuulgewicht van NaCN is cruciaal bij het bepalen van de hoeveelheid verbinding die nodig is voor chemische reacties.
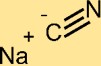
Structuur van natriumcyanide
NaCN heeft een kristalstructuur die bestaat uit Na+-kationen en CN-anionen. Het cyanide-ion bestaat uit een koolstofatoom gebonden aan een stikstofatoom. De structuur van NaCN speelt een belangrijke rol in zijn reactiviteit en chemisch gedrag.
Oplosbaarheid van natriumcyanide
NaCN is zeer oplosbaar in water, met een oplosbaarheid van ongeveer 46 gram per 100 milliliter bij kamertemperatuur. Deze hoge oplosbaarheid maakt een efficiënte oplossing en gebruik van NaCN in verschillende processen mogelijk.
| Verschijning | Witte kristallijne vaste stof |
| Soortelijk gewicht | 1,6 g/ml |
| Kleur | Wit |
| Geur | Geurloos |
| Molaire massa | 49,01 g/mol |
| Dikte | 1,6 g/ml |
| Fusie punt | 564°C |
| Kookpunt | 1496°C |
| Flitspunt | Niet toepasbaar |
| oplosbaarheid in water | Oplosbaar |
| Oplosbaarheid | Oplosbaar in water, ammoniak, methanol, ethanol |
| Dampdruk | Niet beschikbaar |
| Dampdichtheid | Niet beschikbaar |
| pKa | Niet beschikbaar |
| pH | Alkalisch |
Veiligheid en gevaren van natriumcyanide
NaCN brengt aanzienlijke veiligheidsrisico’s en gevaren met zich mee vanwege zijn toxische aard. Blootstelling aan deze stof kan ernstige gevolgen voor de gezondheid hebben. Het verstoort de cellulaire ademhaling en verhindert de zuurstoftoevoer naar vitale organen, wat kan leiden tot ademnood, hartstilstand en zelfs de dood. Inhalatie of inname van NaCN kan snelle en mogelijk fatale symptomen veroorzaken. Het hanteren van NaCN vereist uiterste voorzichtigheid, inclusief het gebruik van geschikte persoonlijke beschermingsmiddelen (PBM) en het naleven van veiligheidsprotocollen. Het is van cruciaal belang om NaCN op de juiste manier op te slaan, te vervoeren en te verwijderen om accidentele vrijgave of besmetting te voorkomen. Regelmatige training en bewustwording zijn essentieel om de risico’s die met NaCN gepaard gaan tot een minimum te beperken.
| Gevarensymbolen | Schedel en gekruiste knekels |
| Beveiligingsbeschrijving | Zeer giftig |
| VN-identificatienummers | Een 1689 |
| HS-code | 2837.11.00 |
| Gevarenklasse | 6.1 |
| Verpakkingsgroep | I |
| Toxiciteit | Dodelijk voor de mens. Er komt waterstofcyanide vrij, een zeer giftig chemisch verstikkend middel dat het vermogen van het lichaam om zuurstof te gebruiken verstoort. |
Methoden voor de synthese van natriumcyanide
Er zijn verschillende methoden voor het synthetiseren van NaCN, waarbij elke methode de reactie van geschikte reagentia omvat. Een veelgebruikte methode is het Castner-proces. In dit proces experimenteert het gesmolten mengsel van natriumcarbonaat , koolstof en stikstofgas met een elektrische stroom, waarbij NaCN wordt gegenereerd. Verzamel vervolgens het gestolde NaCN.
Bij een andere methode reageert natriumhydroxide met HCN-gas. Meng water met natriumhydroxide om een oplossing te creëren en stel de oplossing bloot aan HCN-gas. Daarom vormen NaCN en water bijproducten.
Bovendien omvat de synthese van NaCN de reactie tussen het metaal Na en waterstofcyanidegas. Introduceer het gas in het natriummetaal, waardoor een krachtige reactie ontstaat die NaCN en waterstofgas produceert.
Het is belangrijk op te merken dat de synthese van NaCN alleen mag worden uitgevoerd door opgeleide professionals in goed uitgeruste faciliteiten. Het proces vereist strikte naleving van veiligheidsprotocollen vanwege de zeer giftige aard van de verbinding.
Gebruik van natriumcyanide
NaCN heeft vanwege zijn unieke eigenschappen diverse toepassingen in verschillende industrieën. Hier zijn enkele veelvoorkomende toepassingen:
- Goudwinning: Goudwinning maakt op grote schaal gebruik van NaCN om edele metalen uit ertsen te winnen. Het vormt een complex met goud, waardoor de scheiding en zuivering van het metaal wordt vergemakkelijkt.
- Metaalplating: Bij galvaniseerprocessen wordt NaCN gebruikt om een laag metaal op oppervlakken af te zetten. Het maakt de vorming van een beschermende en decoratieve coating mogelijk, waardoor de duurzaamheid en het uiterlijk worden verbeterd.
- Chemische synthese: NaCN dient als voorloper voor de synthese van verschillende organische verbindingen bij de productie van farmaceutische producten, kunststoffen, kleurstoffen en andere chemicaliën.
- Ongediertebestrijding: NaCN fungeert als ontsmettingsmiddel om ongedierte in bepaalde agrarische contexten te bestrijden. Het elimineert knaagdieren en ongedierte dat schade aan gewassen en opgeslagen producten kan veroorzaken.
- Carbureren: NaCN draagt bij aan het carbureren, een proces dat de oppervlaktehardheid van stalen voorwerpen verbetert. Het vormt een harde buitenlaag, waardoor de weerstand tegen slijtage en corrosie wordt verbeterd.
- Sieraden maken: Bij het maken van sieraden wordt NaCN gebruikt voor het reinigen, polijsten en etsen van metalen. Het helpt de gewenste oppervlakteafwerking te bereiken en onzuiverheden te verwijderen.
- Laboratoriumonderzoek: NaCN vindt toepassingen in verschillende laboratoriumexperimenten en onderzoek, vooral op het gebied van chemie, biochemie en metallurgie.
Vragen:
Vraag: Waar wordt natriumcyanide voor gebruikt?
A: NaCN wordt gebruikt bij de goudwinning, het plateren van metalen, chemische synthese, ongediertebestrijding, carboneren, het maken van sieraden en laboratoriumonderzoek.
Vraag: Hoe maak je natriumcyanide?
A: NaCN kan worden gesynthetiseerd met methoden zoals het Castner-proces, reactie met natriumhydroxide en HCN-gas, of reactie van natriummetaal met HCN-gas.
Vraag: Hoeveel atomen zitten er in totaal in 9,203 e-22 mol natriumcyanide?
A: In 9,203 e-22 mol NaCN kan het totale aantal atomen worden berekend op basis van het getal van Avogadro, dat ongeveer 6,022 x 10^23 atomen/mol is.
Vraag: Is natriumcyanide oplosbaar in water?
A: Ja, NaCN is zeer oplosbaar in water.
Vraag: Maakt natriumcyanide Sn2?
A: NaCN kan deelnemen aan SN2-reacties (bimoleculaire nucleofiele substitutie).
Vraag: Is natriumcyanide dodelijk?
A: Ja, NaCN is zeer giftig en kan dodelijk zijn als er niet op de juiste manier mee wordt omgegaan.
Vraag: Hoe wordt natriumcyanide gebruikt in de mijnbouw?
A: NaCN wordt gebruikt in de mijnbouw voor goudwinning, waar het een complex vormt met goud, waardoor het gemakkelijker van de ertsen kan worden gescheiden.
Vraag: Hoe doof ik natriumcyanide?
A: NaCN kan worden gedeactiveerd door een geschikt deactiveringsmiddel toe te voegen, zoals waterstofperoxide of natriumhypochloriet, om het om te zetten in minder giftige stoffen.
Vraag: Wat is het belangrijkste product dat wordt gevormd bij de behandeling van (R)1-broom-4-methylhexaan met natriumcyanide?
A: Het belangrijkste product dat wordt gevormd tijdens de behandeling van (R)1-broom-4-methylhexaan met NaCN is (R)4-methylhexanitril.
Vraag: Welke van de volgende reageert het langzaamst met NaCN?
A: De reactiviteit met NaCN kan variëren, maar primaire alkylhalogeniden reageren over het algemeen langzamer dan secundaire of tertiaire alkylhalogeniden.
Vraag: Remt cyanide de Na-K-pomp?
A: Ja, CN remt de natrium-kaliumpomp, die cruciaal is voor het behouden van een goede cellulaire functie.
