Natriumbisulfiet (NaHSO3) is een chemische verbinding die wordt gebruikt als conserveermiddel voor levensmiddelen en in verschillende industriële toepassingen. Het werkt door de groei van bacteriën te remmen en oxidatie te voorkomen.
| IUPAC-naam | Natriumwaterstofsulfiet |
| Moleculaire formule | NaHSO3 |
| CAS-nummer | 7631-90-5 |
| Synoniemen | Natriumbisulfiet, Natriumzuursulfiet, Natriumwaterstofsulfiet, Natriumwaterstofsulfiet, Natriumsulfietmonohydraat |
| InChi | InChI=1S/Na.H2O3S/c;1-4(2)3/h;(H2,1,2,3)/q+1;/p-1 |
Eigenschappen van natriumbisulfiet
Natriumbisulfietformule
De chemische formule voor natriumbisulfiet is NaHSO3. Deze formule geeft het aantal en het type atomen aan dat aanwezig is in een enkel molecuul natriumbisulfiet. De formule is cruciaal bij het bepalen van het gedrag van natriumbisulfiet onder verschillende chemische reacties en fysische omstandigheden.
Natriumbisulfiet molaire massa
NaHSO3 heeft een molaire massa van 104,06 g/mol. Dit is de som van de atoommassa’s van de samenstellende elementen van een enkel NaHSO3-molecuul. Molaire massa is een belangrijke fysieke eigenschap die helpt bij het bepalen van de hoeveelheid van een stof in een bepaald monster.
Kookpunt van natriumbisulfiet
Het kookpunt van NaHSO3 is 150°C. Dit is de temperatuur waarbij de vloeibare vorm van NaHSO3 in een gas begint te veranderen. Kookpunt is een cruciale fysieke eigenschap die bepaalt hoe een stof zich gedraagt onder verschillende temperatuuromstandigheden.
Natriumbisulfiet Smeltpunt
Het smeltpunt van NaHSO3 is 150°C. Dit is de temperatuur waarbij de vaste vorm van NaHSO3 in een vloeistof begint te veranderen. Het smeltpunt is een essentiële fysische eigenschap die helpt bij het bepalen van het gedrag van een stof onder verschillende temperatuuromstandigheden.
Dichtheid van natriumbisulfiet g/ml
De dichtheid van NaHSO3 is 1,48 g/ml. Dit verwijst naar de hoeveelheid massa die aanwezig is in een bepaald volume NaHSO3. Dichtheid is een belangrijke fysieke eigenschap die helpt bepalen hoe een stof zich gedraagt onder verschillende druk- en temperatuuromstandigheden.
Natriumbisulfiet Molecuulgewicht
Het molecuulgewicht van NaHS03 bedraagt 104,06 g/mol. Dit is de som van de atoomgewichten van de samenstellende elementen van een enkel NaHSO3-molecuul. Het molecuulgewicht is een essentiële fysische eigenschap die helpt bij het bepalen van de hoeveelheid van een stof in een bepaald monster.
Structuur van natriumbisulfiet
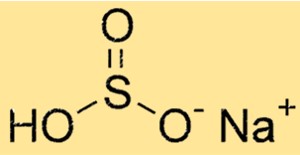
NaHSO3 heeft een moleculaire structuur die bestaat uit een natriumkation (Na+) en een HSO3-anion. Het anion bestaat uit één zwavelatoom, drie zuurstofatomen en één waterstofatoom. De structuur van NaHSO3 bepaalt de chemische en fysische eigenschappen ervan.
Oplosbaarheid van natriumbisulfiet
NaHSO3 is zeer oplosbaar in water, met een oplosbaarheid van 62 g/100 ml bij 20°C. Het is ook oplosbaar in glycerol en enigszins oplosbaar in alcohol. Door de oplosbaarheid in water is het een nuttig reagens bij verschillende chemische reacties.
| Verschijning | Wit kristallijn poeder |
| Soortelijk gewicht | 1.48 |
| Kleur | Wit tot lichtgeel |
| Geur | Zwavelachtige geur |
| Molaire massa | 104,06 g/mol |
| Dikte | 1,48 g/ml |
| Fusie punt | 150°C |
| Kookpunt | 150°C |
| Flitspunt | Niet toepasbaar |
| oplosbaarheid in water | Zeer oplosbaar |
| Oplosbaarheid | Oplosbaar in ethanol |
| Dampdruk | Niet toepasbaar |
| Dampdichtheid | Niet toepasbaar |
| pKa | 6,97 |
| pH | 4,5-5,5 (5% oplossing) |
Veiligheid en gevaren van natriumbisulfiet
NaHSO3 kan schadelijk zijn als het wordt ingeslikt, ingeademd of in contact komt met de huid of ogen. Dit kan huidirritatie, oogbeschadiging, ademhalings- en spijsverteringsproblemen veroorzaken. Langdurige blootstelling kan tot ernstigere gezondheidsproblemen leiden. Het is belangrijk om NaHSO3 met zorg te hanteren en op te slaan, waarbij u persoonlijke beschermingsmiddelen gebruikt, zoals handschoenen, een veiligheidsbril en een gasmasker. Het moet uit de buurt worden gehouden van brandbare materialen en onverenigbare stoffen. In geval van accidenteel contact of inslikken moet onmiddellijk medische hulp worden ingeroepen. Om potentiële gevaren te voorkomen, moeten de juiste opslag- en hanteringsprocedures worden gevolgd.
| Gevarensymbolen | Schedel met gekruiste knekels, bijtend |
| Beveiligingsbeschrijving | Vermijd contact met huid, ogen en kleding. Niet inslikken of inhaleren. Gebruik geschikte beschermende uitrusting. |
| VN-identificatienummers | UN2693 |
| HS-code | 28321000 |
| Gevarenklasse | 8 |
| Verpakkingsgroep | III |
| Toxiciteit | Zeer giftig bij inslikken of inademen. Kan huid- en oogirritatie, ademhalings- en spijsverteringsproblemen veroorzaken. Langdurige blootstelling kan ernstige gezondheidsproblemen veroorzaken. |
Methoden voor de synthese van natriumbisulfiet
Er zijn verschillende methoden voor het synthetiseren van NaHSO3, maar de meest gebruikelijke is het laten reageren van natriumcarbonaat en zwaveldioxide.
Om een NaHSO3-oplossing te produceren, mengt u een oplossing van natriumcarbonaat met zwaveldioxidegas. Bij de reactie komt warmte vrij en is een reactievat met voldoende ventilatie nodig.
Een andere methode omvat de reactie van natriumhydroxide met zwaveldioxidegas om een natriumsulfietoplossing te produceren, die vervolgens wordt aangezuurd om een NaHSO3-oplossing te produceren. Voor grote hoeveelheden NaHSO3 blijkt deze methode bruikbaar.
Om NaHSO3 te synthetiseren, reageert zwavelzuur met natriumsulfiet , waardoor een NaHSO3-oplossing ontstaat. Deze methode is nuttig wanneer een meer geconcentreerde oplossing van NaHSO3 vereist is.
Gebruik van natriumbisulfiet
NaHSO3 heeft een breed scala aan toepassingen in verschillende industrieën. Hier zijn enkele van de meest voorkomende toepassingen:
- Voedingsindustrie – Gebruikt als voedselconserveermiddel om de groei van bacteriën te voorkomen en de houdbaarheid van voedselproducten zoals ingeblikt fruit en groenten, sappen en wijn te verlengen.
- Waterbehandeling – Gebruikt als reductiemiddel om overtollig chloor uit drinkwater- en afvalwaterzuiveringssystemen te verwijderen.
- Textielindustrie – Gebruikt als bleekmiddel om resterende kleurstoffen uit textiel te verwijderen.
- Fotografische industrie – Gebruikt als ontwikkelingsmiddel bij fotografische verwerking.
- Olieboringen – Gebruikt als corrosieremmer en in terugwinningssystemen om zuurstof te verwijderen en corrosie te voorkomen tijdens olie- en gasboringen.
- Farmaceutische producten – Gebruikt als antioxidant en reductiemiddel bij de vervaardiging van bepaalde farmaceutische producten.
- Persoonlijke verzorging – Wordt gebruikt als middel om het haar recht te maken en bij de productie van bepaalde producten voor persoonlijke verzorging, zoals shampoos en conditioners.
- Ander gebruik – Gebruikt bij de productie van papier en pulp, als laboratoriumreagens en als chelaatvormer voor metaalionen.
Vragen:
Vraag: Wat is NaHSO3?
A: NaHSO3 is de chemische formule voor natriumbisulfiet, een zout dat voor verschillende doeleinden in verschillende industrieën wordt gebruikt.
Vraag: Wat is ongeveer de pH van 0,015 M NaHSO3?
A: De geschatte pH van 0,015 M NaHSO3 is ongeveer 7. Deze oplossing is neutraal omdat deze noch een zuur noch een base is.
Vraag: Is NaHSO3 zuur of basisch?
A: NaHSO3 is enigszins zuur omdat het waterstofionen in water kan doneren om HSO3- en H+-ionen te vormen.
Vraag: Wat is het oxidatiegetal van zwavel (S) in NaHSO3, een van de reactanten die in dit experiment zijn gebruikt?
A: Het oxidatiegetal van zwavel (S) in NaHSO3 is +4.
Vraag: Wat doet NaHSO3?
A: NaHSO3 wordt gebruikt als reductiemiddel en als bron van zwaveldioxide. Het kan ook fungeren als antioxidant en conserveermiddel in voedingsmiddelen en farmaceutische producten.
Vraag: Als je 1,00 kg I2 wilt bereiden, welke massa’s NaIO3 en NaHSO3 zijn dan nodig?
A: De uitgebalanceerde chemische vergelijking voor de reactie tussen NaIO3 en NaHSO3 om I2 te vormen is: 5NaIO3 + NaHSO3 + 3H2O → 3I2 + 5NaSO4 + 3H2SO4. Met stoichiometrie zou je 3,33 kg NaIO3 en 1,00 kg NaHSO3 nodig hebben om 1,00 kg I2 te bereiden. .
Vraag: Waarom hebben we aan het einde van de reactie natriumbisulfiet toegevoegd?
A: NaHSO3 wordt aan het einde van sommige chemische reacties toegevoegd om overtollig broom te verwijderen, wat schadelijk kan zijn of latere stappen in het proces kan verstoren.
Vraag: Wat is natriumbisulfiet?
A: NaHSO3 is een zout dat vanwege zijn reducerende, antioxiderende en conserverende eigenschappen wordt gebruikt in verschillende industrieën, waaronder de voedingsmiddelen-, farmaceutische en waterbehandelingsindustrie.
Vraag: Hoe verwijdert natriumbisulfiet broom?
A: NaHSO3 reageert met broom en vormt natriumbromide en zwaveldioxidegas, waardoor overtollig broom effectief uit een oplossing wordt verwijderd.
Vraag: Wat is menadion-natriumbisulfietcomplex?
A: Menadion-natriumbisulfietcomplex is een synthetische verbinding die wordt gebruikt als bron van vitamine K in sommige voedingssupplementen en voedselproducten voor huisdieren.
Vraag: Waar wordt natriumbisulfiet voor gebruikt?
A: NaHSO3 wordt gebruikt als reductiemiddel, antioxidant en conserveermiddel in verschillende industrieën, waaronder de voedingsmiddelenindustrie, de farmaceutische industrie, waterbehandeling en olieboringen. Het kan ook worden gebruikt als haarontkruller en bij fotografische verwerking.
