Naftaleen is een witte kristallijne verbinding die wordt gebruikt in mottenballen en industriële processen. Het heeft een duidelijke geur en verdampt gemakkelijk.
| IUPAC-naam | Naftaleen |
| Moleculaire formule | C10H8 |
| CAS-nummer | 91-20-3 |
| Synoniemen | Teerkamfer, witte teer, naftaleen, albokoolstof |
| InChi | InChI=1S/C10H8/c1-2-6-10-8-4-3-7-9(10)5-1/h1-8H |
Eigenschappen van naftaleen
Naftaleen formule
De formule voor naftaleen of naftaleen is C10H8. Het bestaat uit tien koolstofatomen en acht waterstofatomen. De formule vertegenwoordigt de exacte verhouding van atomen die aanwezig zijn in een mottenbalmolecuul.
Naftaleen molaire massa
De molaire massa van naftaleen is 128,17 gram per mol. Het wordt berekend door de atoommassa’s van alle atomen in een mottenbalmolecuul op te tellen.
Kookpunt van naftaleen
Mothball heeft een kookpunt van ongeveer 218 graden Celsius. Dit betekent dat mottenballen bij temperaturen boven de 218 graden Celsius overgaan van een vaste fase naar een gasfase.
Smeltpunt van naftaleen
Het smeltpunt van mottenballen ligt rond de 80 graden Celsius. Dit geeft aan dat mottenballen veranderen van een vaste naar een vloeibare toestand wanneer ze worden verwarmd tot temperaturen boven de 80 graden Celsius.
Dichtheid van naftaleen g/ml
Mottenbal heeft een dichtheid van ongeveer 1,145 gram per milliliter. Dichtheid is een maatstaf voor de massa die zich in een bepaald volume van een stof bevindt. In het geval van mottenballen betekent dit dat 1 milliliter mottenballen 1,145 gram weegt.
Moleculair gewicht van naftaleen
Het molecuulgewicht van naftaleen is 128,17 gram per mol. Het vertegenwoordigt de gemiddelde massa van een mottenbalmolecuul ten opzichte van de verenigde atomaire massa-eenheid (amu).
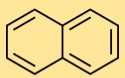
Structuur van naftaleen
Naftaleen heeft een duidelijke structuur die bestaat uit twee gefuseerde benzeenringen. De koolstofatomen van elke benzeenring zijn verbonden door een gedeeld paar koolstofatomen, wat resulteert in een gefuseerd ringsysteem.
Oplosbaarheid van naftaleen
Naftaleen is slecht oplosbaar in water, wat betekent dat het slechts in beperkte mate oplost. Het is echter zeer oplosbaar in organische oplosmiddelen zoals ethanol en benzeen. Dit oplosbaarheidsgedrag is te wijten aan de polariteitsverschillen tussen naftaleen en water.
| Verschijning | Witte kristallen |
| Soortelijk gewicht | 1.145 g/ml |
| Kleur | Kleurloos |
| Geur | Verschillend |
| Molaire massa | 128,17 g/mol |
| Dikte | 1,145 g/cm³ |
| Fusie punt | 80°C |
| Kookpunt | 218°C |
| Flitspunt | 79°C |
| oplosbaarheid in water | ~31,6 mg/l |
| Oplosbaarheid | Oplosbaar in organische oplosmiddelen zoals benzeen, ethanol |
| Dampdruk | 0,4 mmHg bij 25°C |
| Dampdichtheid | 4,37 (lucht = 1) |
| pKa | ~4,7 |
| pH | Neutrale |
Veiligheid en gevaren van naftaleen
Mottenballen brengen veiligheidsrisico’s met zich mee en moeten met zorg worden behandeld. Het is schadelijk bij inslikken, inademen of opname via de huid. Vermijd direct contact en draag geschikte beschermende uitrusting tijdens het hanteren. Het kan de ogen, de huid en de luchtwegen irriteren en ongemak veroorzaken. Houd het uit de buurt van open vuur, omdat het brandbaar is en bij verbranding giftige dampen kan vrijkomen. Bewaar mottenballen in een goed geventileerde ruimte, uit de buurt van onverenigbare stoffen. Indien blootgesteld of ingeslikt, dient u onmiddellijk medische hulp in te roepen. Volg altijd de veiligheidsmaatregelen, gebruik het in een gecontroleerde omgeving en bewaar het veilig om potentiële risico’s te minimaliseren.
| Gevarensymbolen | Schadelijk bij inslikken, inademen of opname via de huid |
| Beveiligingsbeschrijving | Wees voorzichtig, draag beschermende uitrusting en vermijd direct contact |
| VN-identificatienummers | VN 1334 |
| HS-code | 2902.90.0000 |
| Gevarenklasse | 4.1 (ontvlambare vaste stof) |
| Verpakkingsgroep | III |
| Toxiciteit | Giftig voor in het water levende organismen, met langdurige gevolgen |
Houd er rekening mee dat de verstrekte gevarensymbolen en veiligheidsbeschrijvingen representatief zijn, en het is belangrijk om officiële bronnen en veiligheidsrichtlijnen te raadplegen voor specifieke, actuele informatie over mottenballengerelateerde veiligheidsrisico’s en voorzorgsmaatregelen. .
Naftaleensynthesemethoden
Verschillende methoden maken de synthese van naftaleen mogelijk.
Een gebruikelijke aanpak is de “dehydrogenering” van bicyclische verbindingen zoals decaline of tetraline bij hoge temperaturen, resulterend in de vorming van naftaleen. Eén methode omvat het katalytisch reformeren van aardoliefracties, waarbij naftaleen als bijproduct wordt geproduceerd.
Bovendien is “koolteerdestillatie” een belangrijk industrieel proces voor het verkrijgen van naftaleen. Bij dit proces wordt de verzameling van naftaleenrijke fracties uitgevoerd door gefractioneerde destillatie van koolteer.
Bovendien kan “decarboxylering” van ftaalzuur of zijn derivaten naftaleen produceren. Deze reactie omvat de verwijdering van een carboxylgroep om de aromatische structuur van naftaleen te vormen.
Bovendien is “alkylering” van benzeen met alkylhalogeniden gevolgd door “cyclisatie” een haalbare synthetische route naar naftaleen. Bij deze methode ondergaan alkyl-gesubstitueerde benzeenverbindingen een reeks reacties om het naftaleenringsysteem te vormen.
Elk van deze synthesemethoden biedt routes voor de productie van naftaleen, die voldoen aan verschillende industriële eisen en toepassingen. Onderzoekers en industrieën gebruiken deze methoden, rekening houdend met factoren als opbrengst, effectiviteit en veiligheid voor een succesvolle productie van mottenballen.
Gebruik van naftaleen
Mothball heeft diverse toepassingen in verschillende industrieën. Hier zijn enkele belangrijke toepassingen van mottenballen:
- Mottenballen: De mottenballen in mottenballen stoten en voorkomen mottenplagen in opgeslagen kleding en stoffen.
- Chemische productie: Mothball wordt gebruikt als grondstof bij de productie van verschillende chemicaliën, waaronder ftaalzuuranhydride, die worden gebruikt bij de productie van kunststoffen.
- Kleurstofproductie: Naftaleen is essentieel voor de synthese van kleurstoffen, vooral voor het produceren van heldere, levendige kleuren in textiel en andere materialen.
- Oplosmiddel: Industrieën gebruiken naftaleen als oplosmiddel om organische verbindingen te extraheren en speciale chemicaliën te formuleren, waarbij ze profiteren van de lage polariteit ervan.
- Insecticiden: Mottenbalderivaten spelen een sleutelrol bij de formulering van insecticiden en pesticiden, waardoor plagen effectief worden bestreden en gewassen worden beschermd.
- Betonadditief: Naftaleen is een essentieel additief in betonmengsels, werkt als waterreducerend middel en verbetert de verwerkbaarheid en vloeibaarheid tijdens de bouw.
- Brandstof en brandstofadditieven: Naftaleen wordt gebruikt als brandstofadditief in benzine en sommige brandstoffen vanwege het hoge energiegehalte.
- Onderzoek en laboratoriumtoepassingen: Naftaleen vindt toepassingen in wetenschappelijk onderzoek, zoals spectroscopie-experimenten en als standaard referentiemateriaal.
De veelzijdige eigenschappen van Mothball maken het tot een waardevolle verbinding in alle industrieën, en dragen bij aan gebieden variërend van ongediertebestrijding tot chemische synthese en daarbuiten.
Vragen:
Vraag: Wat is het kookpunt van naftaleen?
A: Het kookpunt van mottenballen is ongeveer 218 graden Celsius.
Vraag: Hoe doodt naftaleen motten?
A: De sterke geur van mottenballen werkt afstotend, waardoor vlinders ervan worden weerhouden eieren te leggen en verstikking veroorzaken wanneer ze door vlinders worden ingeademd.
Vraag: Wat is het smeltpunt van naftaleen?
A: Het smeltpunt van mottenballen ligt rond de 80 graden Celsius.
Vraag: Hoe giftig is naftaleen?
A: Mottenbal is giftig bij inslikken of inademen en kan irritatie aan de ogen, huid en luchtwegen veroorzaken.
Vraag: Waar kan ik sneeuwwitte naftaleenballen kopen?
A: Sneeuwwitte mottenballen kunnen worden gekocht bij supermarkten, bouwmarkten of online winkels.
Vraag: Kunnen naftaleenballen mensen doden?
A: Mottenballen kunnen schadelijk zijn als ze in grote hoeveelheden worden ingenomen, maar in kleine hoeveelheden zijn ze over het algemeen niet dodelijk voor mensen.
Vraag: Is de geur van naftaleenballen schadelijk?
A: De geur van mottenballen kan gedurende een korte tijd irritatie veroorzaken, maar het is onwaarschijnlijk dat dit ernstige schade zal veroorzaken.
Vraag: Is naftaleen oplosbaar in water?
A: Naftaleen is slecht oplosbaar in water, maar zeer oplosbaar in organische oplosmiddelen zoals benzeen en ethanol.
Vraag: Wat zijn naftaleenballen?
A: Mottenballen zijn kleine, stevige witte balletjes die worden gebruikt om motten af te weren en opgeslagen kleding tegen besmetting te beschermen.
Vraag: In welke volgorde zou je naftaleen verwachten?
A: Naftaleen wordt doorgaans aangetroffen in de gasfase wanneer het in het milieu terechtkomt.
Vraag: Is naftaleen polair?
A: Nee, mottenballen zijn niet-polair vanwege hun symmetrische moleculaire structuur.
Vraag: Wat is naftaleen?
A: Mottenbal is een witte kristallijne koolwaterstofverbinding met een kenmerkende geur, die vaak wordt gebruikt in mottenballen en diverse industriële processen.
Vraag: Welk percentage naftaleenmoleculen zond een foton uit?
A: Het hangt af van de specifieke omstandigheden, maar een klein percentage mottenbalmoleculen kan fotonen uitzenden wanneer ze worden opgewonden door energiebronnen zoals UV-licht.
