Melkzuur wordt tijdens zware inspanning door de spieren geproduceerd en veroorzaakt vermoeidheid. Het wordt ook aangetroffen in gefermenteerd voedsel zoals yoghurt en wordt gebruikt in huidverzorgingsproducten voor exfoliatie.
| IUPAC-naam | 2-hydroxypropaanzuur |
| Moleculaire formule | C3H6O3 |
| CAS-nummer | 50-21-5 |
| Synoniemen | Melkzuur, 2-hydroxypropionzuur, DL-melkzuur |
| InChi | InChI=1S/C3H6O3/c1-2(4)3(5)6/h2,4H,1H3,(H.5,6) |
Eigenschappen van melkzuur
Melkzuurformule
De chemische formule voor melkzuur is C3H6O3. Het bestaat uit drie koolstofatomen, zes waterstofatomen en drie zuurstofatomen. Deze formule vertegenwoordigt de rangschikking en typen atomen die aanwezig zijn in een melkzuurmolecuul.
Molaire melkzuurmassa
De molmassa van melkzuur is ongeveer 90,08 gram per mol. Het wordt berekend door de atoommassa’s van alle atomen in een melkzuurmolecuul op te tellen.
Kookpunt van melkzuur
Melkzuur heeft een kookpunt van ongeveer 122 tot 135 graden Celsius. Bij deze temperatuur verandert het melkzuur van een vloeibare naar een gasvormige toestand. Het kookpunt kan variëren afhankelijk van de zuiverheid en concentratie van het melkzuur.
Smeltpunt van melkzuur
Het smeltpunt van melkzuur ligt rond de 17 tot 18 graden Celsius. Bij deze temperatuur ondergaat het melkzuur een faseverandering van vast naar vloeibaar. Het smeltpunt kan enigszins variëren, afhankelijk van de specifieke vorm van melkzuur.
Melkzuurdichtheid g/ml
De dichtheid van melkzuur is ongeveer 1,2 gram per milliliter (g/ml). Deze dichtheidswaarde geeft de massa melkzuur aan die in een bepaald volume aanwezig is. Dit is een belangrijk kenmerk dat wordt gebruikt om de concentratie van melkzuuroplossingen te bepalen.
Molecuulgewicht van melkzuur
Het molecuulgewicht van melkzuur is ongeveer 90,08 gram per mol. Het vertegenwoordigt de som van de atoomgewichten van alle atomen in een molecuul zuivelzuur. Molecuulgewicht wordt gebruikt bij verschillende chemische berekeningen en analyses.
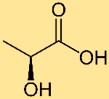
Structuur van melkzuur
Melkzuur heeft een structuur die bestaat uit drie koolstofatomen die met elkaar zijn verbonden in een keten, waarbij een hydroxylgroep (-OH) aan één koolstofatoom is bevestigd en een carboxylgroep (-COOH) aan een ander koolstofatoom is bevestigd. Deze structuur is verantwoordelijk voor de zure eigenschappen van melkzuur.
Oplosbaarheid van melkzuur
Melkzuur is oplosbaar in water en vormt een heldere, kleurloze oplossing. Het lost gemakkelijk op vanwege het vermogen om waterstofbruggen te vormen met watermoleculen. De oplosbaarheid van melkzuur kan variëren afhankelijk van factoren zoals temperatuur en concentratie.
| Verschijning | Kleurloze vloeistof |
| Soortelijk gewicht | 1,2 g/ml |
| Kleur | Kleurloos |
| Geur | Licht zure geur |
| Molaire massa | 90,08 g/mol |
| Dikte | 1,2 g/ml |
| Fusie punt | 17-18°C |
| Kookpunt | 122-135°C |
| Flitspunt | 79°C |
| oplosbaarheid in water | Volledig mengbaar |
| Oplosbaarheid | Oplosbaar in ethanol, water en ether |
| Dampdruk | 3,03 mmHg bij 25°C |
| Dampdichtheid | 2,55 (lucht=1) |
| pKa | 3,86 |
| pH | Ongeveer 2,4-3,4 |
Melkzuurveiligheid en gevaren
Melkzuur brengt enkele veiligheidsproblemen en gevaren met zich mee. Het wordt beschouwd als licht irriterend voor de huid, ogen en luchtwegen. Direct contact kan irritatie, roodheid en ongemak veroorzaken. Inname van geconcentreerd melkzuur kan buikpijn, misselijkheid en braken veroorzaken. Het is belangrijk om voorzichtig om te gaan met melkzuur en passende beschermende maatregelen te nemen, zoals handschoenen en een veiligheidsbril. Bij contact met de huid of ogen wordt spoelen met veel water aanbevolen. Bovendien moet er bij het werken met melkzuur voor voldoende ventilatie worden gezorgd om inademing van dampen te voorkomen.
| Gevarensymbolen | Bijtend (C), Irriterend (Xi) |
| Beveiligingsbeschrijving | Draag beschermende handschoenen en oog-/gezichtsbescherming. Vermijd inademen van dampen. Voorkom lozing in het milieu. |
| VN-identificatienummers | UN3265 |
| HS-code | 2918.12.00 |
| Gevarenklasse | Klasse 8 (corrosief) |
| Verpakkingsgroep | GE III |
| Toxiciteit | Er wordt aangenomen dat melkzuur een lage acute toxiciteit heeft. Dit kan irritatie en brandwonden aan de huid en ogen veroorzaken. Het inademen van dampen kan irritatie van de luchtwegen veroorzaken. Inslikken van geconcentreerd melkzuur kan gastro-intestinale irritatie veroorzaken. De juiste hantering en veiligheidsmaatregelen moeten worden gevolgd om potentiële risico’s te minimaliseren. |
Methoden voor de synthese van melkzuur
Er zijn verschillende methoden voor het synthetiseren van melkzuur.
Een veelgebruikte methode is de fermentatie van koolhydraten door melkzuurbacteriën. Tijdens dit proces zetten micro-organismen suikers, zoals glucose of lactose, via anaëroob metabolisme om in melkzuur. Deze fermentatie komt van nature voor in voedingsmiddelen zoals yoghurt, zuurkool en augurken.
Een andere methode omvat chemische synthese met acetaldehyde als uitgangsmateriaal. Acetaldehyde reageert met cyanide-ionen, wat resulteert in de vorming van lactonitril. Vervolgens vindt hydrolyse plaats, wat leidt tot de omzetting van lactonitril in melkzuur. Deze methode vereist een zorgvuldige omgang en controle van de reactieomstandigheden.
Wetenschappers produceren actief zuivelzuur via bio-engineeringtechnieken door bacteriën zoals Escherichia coli genetisch te modificeren. Ze modificeren deze bacteriën zodat ze enzymen tot expressie brengen die glucose of andere suikers omzetten in melkzuur. Deze methode maakt de productie van zuivelzuur op grotere schaal en met betere procescontrole mogelijk.
Melkzuur wordt verkregen uit hernieuwbare bronnen zoals maïs of suikerriet door het zetmeel of de cellulose in deze plantaardige materialen chemisch te hydrolyseren tot glucose. Microbiële of enzymatische werking fermenteert vervolgens de glucose tot melkzuur.
Elk van deze methoden heeft zijn voordelen en beperkingen in termen van kosten, schaalbaarheid en impact op het milieu. De keuze voor de synthesemethode hangt af van de specifieke toepassing en de gewenste eigenschappen van het zuivelzuur.
Gebruik van melkzuur
Melkzuur vindt vele toepassingen in diverse industrieën. Hier zijn enkele veelvoorkomende toepassingen:
- Voedings- en drankenindustrie: Melkzuur fungeert als natuurlijk conserveermiddel, zuurteregelaar en smaakversterker in voedingsproducten zoals zuivel, gebak en dranken. Het draagt bij aan de pittige smaak van yoghurt en geeft een zure smaak aan zuurdesembrood.
- Farmaceutische industrie: Melkzuur draagt actief bij aan de productie van farmaceutische producten, waaronder medicijnen, zalven en crèmes. Het dient als pH-regelaar en stabilisator in formuleringen, waardoor de effectiviteit en houdbaarheid ervan wordt verbeterd.
- Huidverzorging en cosmetica: Melkzuur is een belangrijk ingrediënt in huidverzorgingsproducten vanwege de exfoliërende eigenschappen. Het helpt dode huidcellen te verwijderen en bevordert een gladdere, helderdere teint. Antiverouderingscrèmes en lotions gebruiken het actief als ingrediënt.
- Textielindustrie: In de textielindustrie neemt melkzuur actief deel aan het verven en reguleert het de pH tijdens het verf- en drukproces. Het helpt de kleurechtheid en kleurpenetratie te verbeteren.
- Bioplastics: Melkzuur is een voorloper voor de productie van biologisch afbreekbare polymeren zoals polymelkzuur (PLA). Bedrijven gebruiken PLA op grote schaal in verpakkingsmaterialen, wegwerpbestek en andere milieuvriendelijke producten.
- Reinigingsproducten: Reinigingsproducten gebruiken melkzuur als krachtig natuurlijk ontsmettings- en ontkalkingsmiddel. Het helpt minerale afzettingen en vlekken van oppervlakken te verwijderen, waardoor het een milieuvriendelijk alternatief is voor agressieve chemicaliën.
- Industriële toepassingen: Melkzuur dient als grondstof voor de synthese van verschillende chemicaliën, waaronder lactaten, oplosmiddelen en biologisch afbreekbare kunststoffen.
De veelzijdige aard van zuivelzuur maakt het tot een waardevol ingrediënt in diverse industrieën en draagt bij aan de ontwikkeling van duurzame en functionele producten.
Vragen:
Vraag: Wat is melkzuur?
A: Melkzuur is een verbinding die door de spieren wordt geproduceerd tijdens intensieve inspanning of door de fermentatie van suikers door micro-organismen, die worden aangetroffen in gefermenteerd voedsel zoals yoghurt.
Vraag: Waar vindt melkzuurfermentatie plaats?
A: Zure fermentatie van melk komt voor in een verscheidenheid aan organismen, waaronder bacteriën, schimmels en onze eigen spiercellen.
Vraag: Wat is melkzuurfermentatie?
A: Melkzuurfermentatie is een metabolisch proces dat suikers omzet in melkzuur, wat plaatsvindt in afwezigheid van zuurstof, wat resulteert in energieproductie.
Vraag: Waar wordt melkzuur voor gebruikt?
A: Melkzuur draagt bij aan vermoeidheid en spierpijn, reguleert de zuurgraad in het lichaam en bemiddelt in verschillende biochemische routes.
Vraag: Wat is een commercieel gebruik van melkzuurfermentatie?
A: Zure fermentatie van melk wordt commercieel gebruikt bij de productie van yoghurt, zuurkool, augurken en ander gefermenteerd voedsel.
Vraag: Hoe kom je van melkzuur af?
A: Zachte lichaamsbeweging, voldoende hydratatie en stretching kunnen helpen melkzuur uit de spieren te verwijderen en af te breken.
Vraag: Waar wordt melkzuur gevonden?
A: Melkzuur wordt aangetroffen in verschillende natuurlijke bronnen, zoals zuivelproducten, gefermenteerd voedsel en dierlijke spieren.
Vraag: Hoe kan ik melkzuur in het lichaam verminderen?
A: Om de opbouw van melkzuur te verminderen, kan men de juiste opwarm- en afkoelroutines inbouwen, een uitgebalanceerd dieet volgen en de trainingsintensiteit geleidelijk verhogen.
