Fosforoxide (P2O5) is een chemische verbinding. Het wordt gevormd uit de combinatie van twee fosforatomen en vijf zuurstofatomen.
| Naam van IUPAC | Fosforpentoxide |
| Moleculaire formule | P2O5 |
| CAS-nummer | 1314-56-3 |
| Synoniemen | Fosforzuuranhydride, fosfor(V)oxide, difosforpentoxide |
| InChi | InChI=1S/2O.P2/c2*1-3-2 |
Eigenschappen van fosforoxide
Fosforoxide-formule
De formule voor difosforpentoxide is P2O5. Het bestaat uit twee fosforatomen en vijf zuurstofatomen. Deze chemische formule vertegenwoordigt de verhouding van elementen in de verbinding.
Fosforoxide molaire massa
De molaire massa van difosforpentoxide (P2O5) wordt berekend door de atoommassa’s van de samenstellende elementen op te tellen. Fosfor heeft een atoommassa van ongeveer 31,0 gram per mol, terwijl zuurstof een atoommassa heeft van ongeveer 16,0 gram per mol. De molaire massa van P2O5 bedraagt dus ongeveer 141,9 gram per mol.
Kookpunt van fosforoxide
Difosforpentoxide heeft geen specifiek kookpunt. In plaats daarvan ondergaat het bij verhitting een chemische reactie, waarbij het wordt omgezet in fosforzuur (H3PO4) en daarbij warmte vrijkomt. Daarom heeft het geen goed gedefinieerd kookpunt zoals veel andere verbindingen.
Smeltpunt van fosforoxide
Difosforpentoxide (P2O5) heeft een smeltpunt van ongeveer 340 graden Celsius (644 graden Fahrenheit). Bij deze temperatuur verandert de vaste verbinding in de vloeibare toestand. Het is belangrijk op te merken dat difosforpentoxide zeer hygroscopisch is, wat betekent dat het gemakkelijk vocht uit de lucht absorbeert.
Fosforoxidedichtheid g/ml
De dichtheid van difosforpentoxide is ongeveer 2,39 gram per milliliter (g/ml). Dichtheid is een maatstaf voor de massa per volume-eenheid, en deze waarde geeft aan hoe zwaar of compact de stof is. De dichtheid van difosforpentoxide draagt bij aan de fysische eigenschappen en het gedrag ervan bij verschillende toepassingen.
Molecuulgewicht van fosforoxide
Het molecuulgewicht van difosforpentoxide (P2O5) is ongeveer 141,9 gram per mol. Deze waarde vertegenwoordigt de som van de atoommassa’s van fosfor en zuurstof in de verbinding. Molecuulgewicht wordt vaak gebruikt bij berekeningen met betrekking tot chemische reacties en de stoichiometrie van verbindingen.
Structuur van fosforoxide
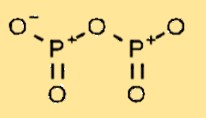
Difosforpentoxide heeft een moleculaire structuur die bestaat uit twee fosforatomen gebonden aan vijf zuurstofatomen. De rangschikking van atomen vormt een cyclische structuur, waarbij elk fosforatoom gebonden is aan twee zuurstofatomen en een dubbele binding deelt met het aangrenzende fosforatoom.
Oplosbaarheid van fosforoxide
Difosforpentoxide is niet oplosbaar in water. Het reageert krachtig met water en vormt fosforzuur, waarbij warmte vrijkomt. Het is echter oplosbaar in sommige organische oplosmiddelen zoals koolstofdisulfide en chloroform. De oplosbaarheidskenmerken van difosforpentoxide spelen een rol bij de chemische reactiviteit en toepassingen ervan.
| Verschijning | Witte kristallijne vaste stof |
| Soortelijk gewicht | 2,39 g/ml |
| Kleur | Kleurloos |
| Geur | Geurloos |
| Molaire massa | 141,9 g/mol |
| Dikte | 2,39 g/ml |
| Fusie punt | 340°C (644°F) |
| Kookpunt | Reageert onder vorming van fosforzuur |
| Flitspunt | Niet toepasbaar |
| oplosbaarheid in water | Reageert met water en vormt fosforzuur |
| Oplosbaarheid | Oplosbaar in organische oplosmiddelen zoals koolstofdisulfide, chloroform |
| Dampdruk | Niet toepasbaar |
| Dampdichtheid | Niet toepasbaar |
| pKa | Niet toepasbaar |
| pH | Niet toepasbaar |
Veiligheid en gevaren van fosforoxide
Difosforpentoxide (P2O5) brengt enkele veiligheidsrisico’s met zich mee en voorzichtigheid is geboden bij het hanteren ervan. Het reageert heftig met water, waarbij warmte vrijkomt en fosforzuur wordt gevormd, wat brandwonden en irritatie aan de huid, ogen en luchtwegen kan veroorzaken. Het is belangrijk om contact met de stof te vermijden en geschikte beschermende uitrusting te gebruiken, zoals handschoenen, een veiligheidsbril en een gasmasker, wanneer u met difosforpentoxide werkt. Bovendien is het van cruciaal belang om de verbinding op te slaan in een goed gesloten container, uit de buurt van vocht en incompatibele materialen. Er moet voor voldoende ventilatie worden gezorgd om ophoping van dampen te voorkomen.
| Gevarensymbolen | Bijtend, schadelijk |
| Beveiligingsbeschrijving | – Veroorzaakt ernstige brandwonden en oogletsel – Kan schadelijk zijn bij inslikken of inademen – Reageert hevig met water – Verwijderd houden van vocht en onverenigbare materialen |
| VN-identificatienummers | Een 1807 |
| HS-code | 2819.10.90 |
| Gevarenklasse | Klasse 8 (bijtende stoffen) |
| Verpakkingsgroep | PG II (Gemiddeld gevaar) |
| Toxiciteit | Giftig voor in het water levende organismen; kan in het aquatisch milieu op lange termijn schadelijke effecten veroorzaken |
Fosforoxidesynthesemethoden
Er kunnen verschillende methoden worden gebruikt om difosforpentoxide (P2O5) te synthetiseren.
Een gebruikelijke methode is het verbranden van fosfor in aanwezigheid van overtollige zuurstof. Deze reactie produceert fosforpentoxide in de vorm van een wit vast residu. De vergelijking voor dit proces is P4 + 5O2 → 2P2O5.
Een andere methode omvat de gecontroleerde oxidatie van fosforverbindingen, zoals fosfortrichloride (PC13) of fosfortribromide (PBr3) , met behulp van zuurstof of lucht. De reactie vindt gewoonlijk plaats bij hoge temperaturen en het resulterende product is fosforpentoxide.
Om difosforpentoxide te verkrijgen, kan fosforzuur (H3PO4) worden gedehydrateerd door het op hoge temperatuur te verwarmen. Dit proces verwijdert watermoleculen en resulteert in de vorming van fosforpentoxide.
Een andere methode voor de bereiding van difosforpentoxide omvat de thermische ontleding van bepaalde fosfaatzouten. Het verwarmen van ammoniumdiwaterstoffosfaat (NH4H2PO4) of ammoniumfosfaat ((NH4)3PO4) leidt bijvoorbeeld tot de vorming van fosforpentoxide.
Bij het synthetiseren van difosforpentoxide is het van cruciaal belang om voorzichtig te zijn vanwege de reactiviteit en het genereren van warmte tijdens specifieke reacties. Er moeten de juiste veiligheidsmaatregelen worden gevolgd, zoals werken in een goed geventileerde ruimte en het dragen van geschikte beschermende uitrusting.
Deze synthetische methoden bieden mogelijkheden voor het verkrijgen van difosforpentoxide, dat toepassingen vindt op verschillende gebieden, waaronder de productie van fosforzuur, kunstmest en chemische tussenproducten.
Gebruik van fosforoxide
Difosforpentoxide (P2O5) vindt vanwege zijn unieke eigenschappen verschillende toepassingen in verschillende industrieën. Hier zijn enkele veelvoorkomende toepassingen van difosforpentoxide:
- Fosforzuurproductie: Bij de productie van fosforzuur wordt op grote schaal difosforpentoxide als een belangrijke voorloper gebruikt. Fosforzuur heeft veel toepassingen in meststoffen, voedseladditieven en reinigingsmiddelen.
- Meststofproductie: Difosforpentoxide speelt een essentiële rol bij de productie van verschillende fosfaatmeststoffen, waaronder superfosfaat- en ammoniumfosfaatmeststoffen. Deze meststoffen voorzien planten van essentiële voedingsstoffen om een gezonde groei te bevorderen.
- Chemische tussenproducten: De synthese van verschillende organische verbindingen, zoals farmaceutische producten, pesticiden en vlamvertragers, heeft betrekking op difosforpentoxide als chemisch tussenproduct.
- Droogmiddel: Difosforpentoxide heeft een sterke affiniteit voor water en werkt als droogmiddel. Het wordt gebruikt in verschillende chemische reacties om water te verwijderen en de gewenste reacties te bevorderen.
- Katalysator: Difosforpentoxide fungeert als katalysator bij specifieke chemische reacties. Het vergemakkelijkt deze reacties door de activeringsenergie te verminderen en daardoor de reactiesnelheden te verhogen.
- Droogmiddel: De hygroscopische aard van difosforpentoxide maakt het geschikt voor gebruik als droogmiddel in vochtgevoelige toepassingen. Het absorbeert en verwijdert effectief vocht uit de omgeving.
- Glasproductie: Glasformuleringen bevatten difosforpentoxide om hun eigenschappen, inclusief thermische uitzetting en brekingsindex, te wijzigen. Speciale brillen, zoals optische glazen en borosilicaatglazen, maken er actief gebruik van.
- Metaaloppervlaktebehandeling: Bij metaaloppervlaktebehandelingen, zoals fosfateren, wordt difosforpentoxide gebruikt om de corrosieweerstand te verbeteren en de hechting van verf aan metalen oppervlakken te verbeteren.
Deze uiteenlopende toepassingen benadrukken het belang van difosforpentoxide in industrieën variërend van de landbouw tot de farmaceutische industrie, waardoor het een waardevolle en breed bruikbare verbinding is.
Vragen:
Vraag: Wat is het oxidatiegetal van fosfor in het PO-ion?
A: Het oxidatiegetal van fosfor in het PO-ion is +5.
Vraag: Wat is de oxidatietoestand van een individueel fosforatoom in PO43−?
A: De oxidatietoestand van een individueel fosforatoom in PO43− is +5.
Vraag: Wat is het oxidatiegetal van fosfor?
A: Het oxidatiegetal van fosfor kan variëren, maar wordt over het algemeen weergegeven als +3 of +5.
Vraag: Wat is de naam van de verbinding P2O5?
A: De naam van de verbinding P2O5 is fosfor (V) pentoxide.
Vraag: Wat is P2O5?
A: P2O5 is een chemische verbinding die fosfor (V) pentoxide wordt genoemd.
Vraag: Wat is de juiste naam voor P2O5?
A: De juiste naam voor P2O5 is fosfor (V) pentoxide.
Vraag: Wat is de naam van P2O5?
A: De naam voor P2O5 is fosfor (V) pentoxide.
Vraag: Is P2O5 amfoteer?
A: Nee, P2O5 is niet amfoteer. Het is een zuuroxide.
Vraag: Wat is P2O5-meststof?
A: P2O5-meststof verwijst naar meststoffen die fosfor (V)-pentoxide (P2O5) bevatten als bron van fosfor, wat belangrijk is voor de plantengroei.
Vraag: Is P2O5 zuur of basisch?
A: P2O5 is een zure verbinding.
Vraag: Is P2O5 een ionische verbinding?
A: Nee, P2O5 is een covalente verbinding.
Vraag: Hoe bereken ik P2O5 in meststoffen?
A: Om de hoeveelheid P2O5 in een meststof te berekenen, vermenigvuldigt u het percentage P2O5 met het gewicht van de meststof.
Vraag: Eigenschappen van P2O5, oplosbaar?
A: P2O5 is slecht oplosbaar in water, maar reageert gemakkelijk met water om fosforzuur te vormen.
Vraag: Hoeveel kilogram P in 14% P2O5?
A: Om de hoeveelheid fosfor (P) in 14% P2O5 te berekenen, vermenigvuldigt u het gewicht van de meststof met 0,14.
