Chloorazijnzuur is een chemische verbinding met de formule CH₂ClCOOH. Het wordt gebruikt in verschillende industriële toepassingen, waaronder de productie van kleurstoffen, farmaceutische producten en herbiciden.
| IUPAC-naam | Chloorazijnzuur |
| Moleculaire formule | CH₂ClCOOH |
| CAS-nummer | 79-11-8 |
| Synoniemen | Monochloorazijnzuur, MCA, chloorethaanzuur, chloorethylzuur |
| InChi | InChI=1S/C2H3ClO2/c3-1-2(4)5/h1H2,(H,4,5) |
Eigenschappen van chloorazijnzuur
Chloorazijnzuurformule
De formule voor chloorazijnzuur is CH₂ClCOOH. Het bestaat uit twee koolstofatomen, drie waterstofatomen, één chlooratoom en twee zuurstofatomen. Het chlooratoom is gebonden aan een van de koolstofatomen, terwijl het andere koolstofatoom gebonden is aan de carbonzuurgroep (-COOH).
Chloorazijnzuur Molaire massa
De molaire massa van monochloorazijnzuur wordt berekend door de atoommassa’s van de samenstellende elementen op te tellen. Monochloorazijnzuur heeft een molaire massa van ongeveer 94,5 gram per mol. Het wordt bepaald door rekening te houden met de atoommassa’s van koolstof (C), waterstof (H), chloor (Cl) en zuurstof (O) die in de verbinding aanwezig zijn.
Kookpunt van chloorazijnzuur
Monochloorazijnzuur heeft een kookpunt van ongeveer 189 graden Celsius. Bij deze temperatuur gaat vloeibaar monochloorazijnzuur over in de gasfase. Het kookpunt van monochloorazijnzuur wordt beïnvloed door intermoleculaire krachten tussen de moleculen en de atmosferische druk.
Chloorazijnzuur Smeltpunt
Het smeltpunt van monochloorazijnzuur ligt rond de 62 graden Celsius. Dit is de temperatuur waarbij de vaste vorm van monochloorazijnzuur overgaat in de vloeibare toestand. Het smeltpunt kan enigszins variëren, afhankelijk van de zuiverheid van het monster en de omstandigheden waaronder het wordt gemeten.
Dichtheid van chloorazijnzuur g/ml
De dichtheid van monochloorazijnzuur is ongeveer 1,58 gram per milliliter. Het geeft de massa monochloorazijnzuur per volume-eenheid aan. De dichtheid van monochloorazijnzuur wordt beïnvloed door factoren zoals temperatuur en druk.
Chloorazijnzuur Molecuulgewicht
Het molecuulgewicht van monochloorazijnzuur is ongeveer 94,5 gram per mol. Het vertegenwoordigt de som van de atoomgewichten van alle atomen in een molecuul monochloorazijnzuur. Het molecuulgewicht is nuttig bij verschillende berekeningen waarbij de verbinding betrokken is, zoals het bepalen van concentraties of molaire hoeveelheden.
Structuur van chloorazijnzuur
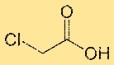
Monochloorazijnzuur heeft een structuur die bestaat uit een centraal koolstofatoom gebonden aan een chlooratoom, een carbonzuurgroep (-COOH) en twee waterstofatomen. Het chlooratoom is rechtstreeks gebonden aan het koolstofatoom. De structurele opstelling van monochloorazijnzuur beïnvloedt de chemische eigenschappen en reactiviteit ervan.
Oplosbaarheid van chloorazijnzuur
Monochloorazijnzuur is matig oplosbaar in water. Het vormt waterstofbruggen met watermoleculen, waardoor het tot op zekere hoogte kan oplossen. De oplosbaarheid van monochloorazijnzuur wordt beïnvloed door factoren zoals temperatuur, pH en de aanwezigheid van andere stoffen in de oplossing.
| Verschijning | Kleurloze vloeistof |
| Soortelijk gewicht | 1,58 g/ml |
| Kleur | Kleurloos |
| Geur | Azijn |
| Molaire massa | 94,5 g/mol |
| Dikte | 1,58 g/ml |
| Fusie punt | 62°C |
| Kookpunt | 189°C |
| Flitspunt | 111°C |
| oplosbaarheid in water | Mengbaar |
| Oplosbaarheid | Oplosbaar in ethanol, ether, chloroform |
| Dampdruk | 0,23 mmHg bij 25°C |
| Dampdichtheid | 3,3 (lucht = 1) |
| pKa | 2,87 |
| pH | 1,5 – 2,5 |
Veiligheid en gevaren van chloorazijnzuur
Monochloorazijnzuur brengt verschillende veiligheidsrisico’s met zich mee en moet met voorzichtigheid worden gehanteerd. Het is bijtend voor de huid, ogen en luchtwegen en veroorzaakt brandwonden en irritatie. Direct contact kan ernstig huid- en oogletsel veroorzaken. Inademing van de dampen of nevels kan de luchtwegen irriteren. Het is ook schadelijk bij inslikken en veroorzaakt maag-darmklachten. Bij het werken met monochloorazijnzuur moeten geschikte persoonlijke beschermingsmiddelen, zoals handschoenen en een veiligheidsbril, worden gedragen. Voldoende ventilatie is van cruciaal belang om de blootstelling tot een minimum te beperken. In geval van contact met de huid of ogen is onmiddellijk spoelen met water essentieel en moet medische hulp worden ingeroepen.
| Gevarensymbolen | Bijtend, giftig |
| Beveiligingsbeschrijving | Vermijd contact. Gebruik persoonlijke beschermingsmiddelen. Zorg voor voldoende ventilatie. Breekbaar. |
| VN-identificatienummers | VN 1751 |
| HS-code | 2915.12.00 |
| Gevarenklasse | 8 (corrosief) |
| Verpakkingsgroep | II |
| Toxiciteit | Giftig bij inslikken, inademen en opname door de huid. Veroorzaakt ernstige brandwonden en oogletsel. Schadelijk bij inslikking. |
Methoden voor de synthese van chloorazijnzuur
Verschillende methoden maken de synthese van monochloorazijnzuur mogelijk.
Een veelgebruikte methode voor het synthetiseren van monochloorazijnzuur is het behandelen van azijnzuur met een halogeneringsmiddel, meestal chloorgas (Cl₂), in aanwezigheid van een katalysator zoals zwavelzuur (H₂SO₄). De reactie tussen azijnzuur en chloor resulteert in de vervanging van een waterstofatoom in het azijnzuurmolecuul door een chlooratoom, waardoor monochloorazijnzuur ontstaat.
Een andere methode is de reactie tussen acetylchloride (CH₃COCl) en water (H₂O). Water hydrolyseert acetylchloride, wat leidt tot de vorming van monochloorazijnzuur. Deze reactie is exotherm en vereist voorzichtigheid bij het uitvoeren ervan.
De vorming van monochloorazijnzuur vindt plaats door de carboxylering van chloormethaan (CH₃Cl) met behulp van koolstofdioxide (CO₂) in aanwezigheid van een robuuste base zoals natriumhydroxide (NaOH) . De reactie verloopt door nucleofiele substitutie, waarbij de carboxylaatgroep (-COOH) van het kooldioxidemolecuul het chloride-ion vervangt.
Houd er rekening mee dat de juiste hantering en veiligheidsmaatregelen cruciaal zijn voor deze synthesemethoden vanwege de corrosieve en toxische aard van monochloorazijnzuur. Zorg voor een zorgvuldige controle van de reactieomstandigheden en een juiste verwijdering van bijproducten en afval om veilige en efficiënte syntheseprocessen te garanderen.
Gebruik van chloorazijnzuur
Monochloorazijnzuur vindt toepassingen in verschillende industrieën vanwege zijn veelzijdige eigenschappen. Hier zijn enkele veelvoorkomende toepassingen:
- Productie van herbiciden: Monochloorazijnzuur is een essentieel ingrediënt bij de synthese van herbiciden, zoals glyfosaat. Het helpt de groei van ongewenste planten en onkruid in de landbouw te remmen.
- Farmaceutische productie: Het dient als bouwsteen bij de productie van farmaceutische verbindingen, waaronder antibiotica, antiseptica en analgetica. Monochloorazijnzuur helpt de gewenste eigenschappen van deze geneesmiddelen te wijzigen en te verbeteren.
- Kleurstoffen- en pigmentindustrie: Fabrikanten gebruiken monochloorazijnzuur bij de productie van kleurstoffen en pigmenten. Het helpt bij de synthese van kleurstoffen die worden gebruikt in textiel, verven, inkten en andere decoratieve toepassingen.
- Chemische tussenproducten: Het fungeert als een belangrijke tussenverbinding bij de productie van verschillende chemicaliën. De synthese van polymeren, oplosmiddelen, weekmakers en andere organische verbindingen omvat het gebruik van deze tussenproducten.
- Productie van oppervlakteactieve stoffen: Monochloorazijnzuur speelt een rol bij de productie van oppervlakteactieve stoffen, die essentiële componenten zijn van wasmiddelen, schoonmaakmiddelen en producten voor persoonlijke verzorging. Oppervlakteactieve stoffen helpen de oppervlaktespanning tussen vloeistoffen te verminderen, waardoor betere meng- en dispergerende eigenschappen mogelijk zijn.
- Onderzoek en laboratoriumtoepassingen: Onderzoekslaboratoria gebruiken monochloorazijnzuur als reagens voor chemische reacties, vooral bij organische synthese en analytische procedures.
- Chemische reacties en organische synthese: Het dient als een belangrijk reagens bij verschillende organische reacties, zoals nucleofiele substituties, veresteringen en carboxyleringsreacties.
- Galvaniseren: Monochloorazijnzuur vindt toepassing bij galvaniseerprocessen, waar het fungeert als een bron van chloor voor de afzetting van metaalcoatings op oppervlakken.
Deze uiteenlopende toepassingen benadrukken het belang van monochloorazijnzuur in alle industrieën en dragen bij aan de ontwikkeling van talrijke chemische producten en processen.
Vragen:
Vraag: Wat is de Ka-waarde voor een 0,15 M oplossing van chloorazijnzuur met een pH van 1,86?
A: De Ka-waarde van monochloorazijnzuur kan worden berekend aan de hand van de pH-waarde en bedraagt ongeveer 1,4 x 10^-3.
Vraag: Is chloorazijnzuur sterk of zwak?
A: Monochloorazijnzuur is een zwak zuur.
Vraag: Wat geeft natrium-4-chloorfenolaat + chloorazijnzuur?
A: De reactie van natrium-4-chloorfenolaat met monochloorazijnzuur geeft 4-chloorfenoxyazijnzuur en natriumchloride.
Vraag: Wat is de Ka van chloorazijnzuur?
A: De Ka-waarde van monochloorazijnzuur is ongeveer 1,4 x 10^-3.
Vraag: Is chloorazijnzuur monoprotisch?
A: Ja, monochloorazijnzuur is monoprotisch, wat betekent dat het bij een chemische reactie slechts één proton (H+ ion) kan afstaan.
Vraag: Wat is de ionisatieconstante van chloorazijnzuur?
A: De ionisatieconstante (Ka) van monochloorazijnzuur is ongeveer 1,4 x 10^-3.
Vraag: Is chloorazijnzuur sterker dan azijnzuur?
A: Ja, monochloorazijnzuur is sterker dan azijnzuur.
Vraag: Waarom is chloorazijnzuur sterker dan azijnzuur?
A: De aanwezigheid van het chlooratoom in monochloorazijnzuur vergroot het elektronenaantrekkende vermogen ervan, waardoor het zuurder wordt dan azijnzuur.
Vraag: Wat is de molaire massa van chloorazijnzuur?
A: De molmassa van monochloorazijnzuur is ongeveer 94,5 gram per mol.
