Calciumsilicaat (Ca2SiO4) is een minerale verbinding die wordt gebruikt in bouwmaterialen, isolatie en brandwering. Het wordt gemaakt door calciumoxide en silica te combineren. Calciumsilicaat zorgt voor thermische isolatie en is brandwerend.
| IUPAC-naam | Calciumsilicaat |
| Moleculaire formule | Ca2SiO4 |
| CAS-nummer | 1344-95-2 |
| Synoniemen | Kiezelzuur, calciumzout (2:1); Calciummetasilicaat; Calcium- en siliciumoxide; Calciumorthosilicaat |
| InChi | InChI=1S/Ca.2O.Si/q+2;2*-1; |
Eigenschappen van calciumsilicaat
Molaire calciumsilicaatmassa
Ca2SiO4 heeft een molaire massa van 172.237 g/mol. Deze waarde wordt berekend door de atoommassa’s van calcium, silicium en zuurstof op te tellen, die respectievelijk 40,078 g/mol, 28,085 g/mol en 15,999 g/mol zijn. De molaire massa is belangrijk bij het bepalen van de hoeveelheid Ca2SiO4 die nodig is voor chemische reacties of de bereiding van oplossingen.
Kookpunt van calciumsilicaat
Ca2SiO4 heeft geen duidelijk kookpunt, omdat het ontleedt voordat het zijn kookpunt bereikt. Wanneer Ca2SiO4 wordt verwarmd, ondergaat het een reeks chemische reacties die leiden tot het vrijkomen van water en de vorming van calciumoxide en silica. De ontledingstemperatuur van Ca2SiO4 hangt af van het specifieke type en de samenstelling van de verbinding.
Smeltpunt van calciumsilicaat
Ca2SiO4 heeft een smeltpunt van 2130°C. Bij deze temperatuur verandert Ca2SiO4 van vaste naar vloeibare toestand. Het smeltpunt van Ca2SiO4 is relatief hoog, waardoor het geschikt is voor toepassingen bij hoge temperaturen, zoals vuurvaste materialen, isolatie en brandwering.
Dichtheid van calciumsilicaat g/ml
De dichtheid van Ca2SiO4 varieert afhankelijk van het specifieke type en de samenstelling van de verbinding. De dichtheid van Ca2SiO4 varieert van 2,2 tot 2,8 g/ml. De hoge dichtheid van Ca2SiO4 maakt het bruikbaar voor toepassingen waarbij gewicht een probleem is. Het wordt bijvoorbeeld gebruikt als lichtgewicht aggregaat in beton.
Calciumsilicaat Molecuulgewicht
Het molecuulgewicht van Ca2SiO4 is 172,237 g/mol. Deze waarde wordt bepaald door de atoomgewichten van calcium, silicium en zuurstof aan de verbinding toe te voegen. Het molecuulgewicht van Ca2SiO4 wordt gebruikt bij verschillende berekeningen, zoals het bepalen van de concentratie van oplossingen of de hoeveelheid verbinding die nodig is voor chemische reacties.
Structuur van calciumsilicaat
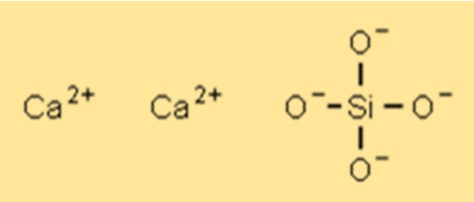
Ca2SiO4 heeft een kristalstructuur die kan variëren afhankelijk van het specifieke type en de samenstelling van de verbinding. De meest voorkomende kristalstructuur is een monoklien kristalsysteem. De kristalstructuur van Ca2SiO4 geeft het bepaalde eigenschappen zoals hoge sterkte, thermische stabiliteit en chemische bestendigheid.
Calciumsilicaatformule
De chemische formule voor calciumsilicaat is Ca2SiO4. Deze formule vertegenwoordigt de verhouding van calcium, silicium en zuurstof in de verbinding. De formule van calciumsilicaat is belangrijk bij het bepalen van de eigenschappen ervan en voor het gebruik ervan in verschillende toepassingen zoals cement, isolatie en brandwering.
| Verschijning | wit poeder |
| Soortelijk gewicht | 2,2 – 2,8 g/cm³ |
| Kleur | Wit |
| Geur | Geurloos |
| Molaire massa | 172.237 g/mol |
| Dikte | 2,2 – 2,8 g/cm³ |
| Fusie punt | 2130°C |
| Kookpunt | Breekt af voordat het kookt |
| Flitspunt | Niet toepasbaar |
| oplosbaarheid in water | Onoplosbaar |
| Oplosbaarheid | Onoplosbaar in water, oplosbaar in zuren |
| Dampdruk | Niet toepasbaar |
| Dampdichtheid | Niet toepasbaar |
| pKa | Niet toepasbaar |
| pH | 7,0 – 9,0 |
Veiligheid en gevaren van calciumsilicaat
Ca2SiO4 wordt over het algemeen als veilig beschouwd voor gebruik in een verscheidenheid aan toepassingen, waaronder bouwmaterialen, isolatie en voedseladditieven. Langdurige of overmatige inademing van Ca2SiO4-stof kan echter de luchtwegen irriteren. Huid- en oogcontact met Ca2SiO4 kan ook irriteren. Hoewel Ca2SiO4 niet als een gevaarlijke stof wordt beschouwd, is het belangrijk om er voorzichtig mee om te gaan en de veiligheidsmaatregelen te volgen bij het werken met dit materiaal. Persoonlijke beschermingsmiddelen zoals handschoenen, veiligheidsbril en ademhalingsbescherming moeten worden gedragen bij het hanteren van Ca2SiO4 om potentiële gezondheidsrisico’s te minimaliseren.
| Gevarensymbolen | Niet toepasbaar |
| Beveiligingsbeschrijving | Geen gevaarlijke stof |
| VN-identificatienummers | Niet toepasbaar |
| HS-code | 6810.19 |
| Gevarenklasse | Niet toepasbaar |
| Verpakkingsgroep | Niet toepasbaar |
| Toxiciteit | Lage toxiciteit; kan bij langdurige of overmatige blootstelling luchtweg- en huidirritatie veroorzaken |
Synthesemethoden voor calciumsilicaat
Er zijn verschillende methoden om Ca2SiO4 te synthetiseren.
Bij één methode reageert calciumoxide (CaO) met silica (SiO2) om een mengsel van calciumsilicaten te produceren. De hogetemperatuuroven maakt de synthese van Ca2SiO4 mogelijk. Het mengsel bevat Ca2SiO4 en Ca3SiO5. Verdere verwerking en vermaling van het mengsel levert verschillende soorten Ca2SiO4-poeder op.
Een andere methode is de reactie tussen calciumhydroxide (Ca(OH)2) en silica in een autoclaaf bij hoge druk en temperatuur. Dit proces levert een zuivere vorm van Ca2SiO4 op, bekend als wollastoniet (CaSiO3), dat een breed scala aan toepassingen heeft, onder meer als vulmiddel in kunststoffen en coatings.
Andere methoden voor het synthetiseren van Ca2SiO4 zijn onder meer de reactie tussen calciumchloride (CaCl2) en natriumsilicaat (Na2SiO3) om Ca2SiO4-hydraat (CSH) te produceren, het belangrijkste bindmiddel in Portland-cement.
Verschillende reagentia en methoden maken de synthese van Ca2SiO4 mogelijk door het neer te slaan uit een oplossing van calcium- en silicaationen.
Gebruik van calciumsilicaat
Ca2SiO4 heeft een breed scala aan toepassingen vanwege de unieke eigenschappen, zoals hoge temperatuurbestendigheid, lage thermische geleidbaarheid en uitstekende brandwerendheid. Hier zijn enkele veelvoorkomende toepassingen van Ca2SiO4:
- Isolatie: Gebruikt als isolatiemateriaal bij toepassingen met hoge temperaturen, zoals ovenbekledingen, ketelisolatie en stoomleidingen. Door de lage thermische geleidbaarheid is het een effectieve isolator in deze omgevingen.
- Bouwmaterialen: Gebruikt in verschillende bouwmaterialen zoals bakstenen, tegels en cement. De weerstand tegen hoge temperaturen en vuur maakt het een ideaal materiaal voor gebruik in brandwerende wanden en plafonds.
- Voedseladditieven: Gebruikt als antiklontermiddel in voedingsmiddelen zoals poedersuiker en zout. Het vermogen om vocht te absorberen en aankoeken te voorkomen, maakt het een populaire keuze bij voedselproducenten.
- Farmaceutische producten: Gebruikt als hulpstof in farmaceutische producten, waar het dient als bindmiddel, desintegratiemiddel en vloeimiddel.
- Cosmetica: Gebruikt in cosmetica als zwel- en absorberend middel. Het helpt de textuur en het gevoel van producten zoals gezichtspoeders en foundations te verbeteren.
- Andere toepassingen: Wordt ook gebruikt bij de productie van keramiek, vuurvaste materialen en als vulmiddel in rubber en kunststoffen.
Vragen:
Vraag: Hoe verwijder je calciumsilicaat uit een zwembad?
A: Om Ca2SiO4 uit een zwembad te verwijderen, gebruikt u een zwembadtegelreiniger of een oplossing van zoutzuur en water. Breng het reinigingsmiddel of de oplossing aan op het aangetaste gebied en scrub met een borstel met harde haren. Na het reinigen met veel water afspoelen.
Vraag: Hoe maak je thuis vuurvast calciumsilicaat?
A: Het wordt niet aanbevolen om thuis vuurvaste Ca2SiO4 te maken vanwege de hoge temperaturen en de vereiste gespecialiseerde apparatuur. Het is het beste om kant-en-klare Ca2SiO4 vuurvaste producten te kopen bij een gerenommeerde leverancier.
Vraag: Calciumsilicaatverbindingen hydrateren en vormen welke twee verbindingen?
A: Ca2SiO4-verbindingen hydrateren en vormen gehydrateerd Ca2SiO4 (CSH) en calciumhydroxide (Ca(OH)2). Deze verbindingen spelen een belangrijke rol bij de vorming en sterkte van beton en andere cementachtige materialen.
