Butadieen (C4H6) is een veelzijdige chemische verbinding. Het wordt gebruikt bij de productie van synthetisch rubber, kunststoffen en diverse andere producten vanwege zijn elasticiteit en sterkte.
| IUPAC-naam | buta-1,3-dieen |
| Moleculaire formule | C4H6 |
| CAS-nummer | 106-99-0 |
| Synoniemen | Divinyl, biethyleen, buta-1,3-dieen, vinylethyleen, erythreen |
| InChi | InChI=1S/C4H6/c1-3-4-2/h3-4H,1-2H2 |
Eigenschappen van butadieen
Butadieen formule
De formule voor butadieen is C4H6. Het bestaat uit vier koolstofatomen en zes waterstofatomen. Deze molecuulformule geeft de rangschikking van atomen in butadieen weer en geeft inzicht in de chemische samenstelling ervan.
Butadieen Molaire Massa
De molaire massa van Buta-1,3-dieen kan worden berekend door de atoommassa’s van de samenstellende elementen op te tellen. Koolstof heeft een molaire massa van ongeveer 12,01 g/mol en waterstof heeft een molaire massa van ongeveer 1,01 g/mol. Daarom is de molaire massa van Buta-1,3-dieen ongeveer 54,09 g/mol.
Kookpunt van butadieen
Buta-1,3-dieen heeft een relatief laag kookpunt vergeleken met veel andere verbindingen. Het kookt rond -4,4 graden Celsius of 24,1 graden Fahrenheit. Dit lage kookpunt maakt een gemakkelijke omzetting van vloeibaar buta-1,3-dieen naar zijn gasvormige toestand mogelijk.
Smeltpunt van butadieen
In tegenstelling tot veel organische verbindingen heeft Buta-1,3-dieen geen duidelijk smeltpunt vanwege het zeer reactieve karakter en de neiging tot polymerisatie. In plaats daarvan bestaat het als een kleurloos gas bij kamertemperatuur en atmosferische druk.
Dichtheid van butadieen g/ml
De dichtheid van buta-1,3-dieen is ongeveer 0,63 g/ml. Deze waarde geeft aan dat Buta-1,3-dieen een lagere dichtheid heeft dan water, dat een dichtheid heeft van 1 g/ml. De lage dichtheid van Buta-1,3-dieen draagt bij aan het drijfvermogen en het vermogen om gemakkelijk dampen te vormen.
Butadieen molecuulgewicht
Het molecuulgewicht van buta-1,3-dieen is ongeveer 54,09 g/mol. Deze waarde vertegenwoordigt de gemiddelde massa van een buta-1,3-dieenmolecuul, rekening houdend met de atoommassa’s van de koolstof- en waterstofatomen die aanwezig zijn in de chemische structuur ervan.
Structuur van butadieen
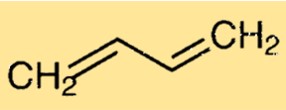
De structuur van Buta-1,3-dieen bestaat uit een keten van vier koolstofatomen die met elkaar zijn verbonden door afwisselend enkele en dubbele bindingen. Elk koolstofatoom is ook gebonden aan twee waterstofatomen. Deze lineaire structuur geeft Buta-1,3-dieen zijn karakteristieke eigenschappen en reactiviteit.
Oplosbaarheid van butadieen
1,3-butadieen is slecht oplosbaar in water, maar lost gemakkelijk op in organische oplosmiddelen zoals benzeen en tolueen. De lage oplosbaarheid in water is te wijten aan verschillen in polariteit tussen buta-1,3-dieen en watermoleculen.
| Verschijning | Kleurloos gas |
| Soortelijk gewicht | 0,62 – 0,63 |
| Kleur | Kleurloos |
| Geur | Lichte en aromatische geur |
| Molaire massa | 54,09 g/mol |
| Dikte | 0,62 – 0,63 g/ml |
| Fusie punt | -138,4°C (-217,1°F) |
| Kookpunt | -4,4°C (24,1°F) |
| Flitspunt | -76°C (-105°F) |
| oplosbaarheid in water | Onoplosbaar |
| Oplosbaarheid | Oplosbaar in organische oplosmiddelen (bijv. benzeen, tolueen) |
| Dampdruk | 448 mmHg bij 20°C |
| Dampdichtheid | 1,9 (Lucht = 1) |
| pKa | ~43 (geschat) |
| pH | Neutrale |
Veiligheid en gevaren van butadieen
1,3-Butadieen brengt enkele veiligheidsrisico’s met zich mee en er moet voorzichtig mee worden omgegaan. Het is brandbaar en kan met lucht explosieve mengsels vormen. Daarom zijn adequate ventilatie- en brandpreventiemaatregelen van cruciaal belang. Langdurige blootstelling aan Buta-1,3-dieen kan irritatie aan de ogen, huid en luchtwegen veroorzaken. Het wordt ook beschouwd als een potentieel carcinogeen en de blootstelling moet tot een minimum worden beperkt. Bij het werken met buta-1,3-dieen moeten beschermende uitrusting zoals handschoenen, een veiligheidsbril en een gasmasker worden gebruikt. Gemorste vloeistoffen moeten onmiddellijk worden ingedamd en opgeruimd. Het is belangrijk om de veiligheidsrichtlijnen te volgen, zoals die van regelgevende instanties, om een veilige behandeling en opslag van Buta-1,3-dieen te garanderen.
| Gevarensymbolen | Ontvlambaar (F), schadelijk (Xn), kankerverwekkend (C) |
| Beveiligingsbeschrijving | Verwijderd houden van hitte/vonken/open vuur. Gebruik in goed geventileerde ruimtes. Vermijd langdurige blootstelling. Hanteren met handschoenen en beschermende kleding. |
| VN-identificatienummers | VN 1010 |
| HS-code | 2903.14.00 |
| Gevarenklasse | 2.1 – Ontvlambare gassen |
| Verpakkingsgroep | GE II |
| Toxiciteit | Beschouwd als een potentieel carcinogeen en kan irritatie van de luchtwegen en de huid veroorzaken. |
Butadieensynthesemethoden
Er zijn verschillende methoden voor het synthetiseren van Buta-1,3-dieen, elk met zijn eigen voordelen en beperkingen. Een veelgebruikte methode is het stoomkraken van koolwaterstoffen, zoals nafta of aardgasvloeistoffen.
Bij dit proces wordt de koolwaterstoftoevoer verwarmd tot hoge temperaturen, doorgaans rond de 800 tot 900°C, in aanwezigheid van stoom. Dit leidt tot het verbreken van koolstof-koolstofbindingen en de vorming van buta-1,3-dieen.
Een andere methode omvat de katalytische dehydrogenering van buteen of butanen. Met behulp van specifieke katalysatoren, zoals metaaloxiden of gedragen metalen, verwijdert de reactie selectief waterstofatomen uit het uitgangsmateriaal, wat resulteert in de productie van Buta-1,3-dieen.
Katalytische dimerisatie van acetyleen levert ook Buta-1,3-dieen op. Dit proces omvat de reactie van twee moleculen acetyleen om Buta-1,3-dieen te vormen, meestal in aanwezigheid van een metaalkatalysator zoals koper.
Katalysatoren zoals aluminiumoxide of zeolieten vergemakkelijken de dehydratatie van ethanol bij hoge temperaturen. Dit proces vormt actief Buta-1,3-dieen.
Bovendien produceren sommige fabrieken buta-1,3-dieen als bijproduct van de ethyleenproductie via het kraakproces van nafta of gasolie. Deze methode maakt gebruik van kraakreacties om een mengsel van olefinen te genereren, waaronder buta-1,3-dieen.
Deze synthesemethoden spelen een cruciale rol bij de productie van Buta-1,3-dieen en bieden verschillende routes om te voldoen aan de vraag naar deze belangrijke chemische stof in industrieën zoals rubber, plastic en de productie van synthetische vezels. .
Gebruik van butadieen
Buta-1,3-dieen vindt toepassing in een breed scala van industrieën vanwege zijn veelzijdige eigenschappen. Hier zijn enkele belangrijke toepassingen van Buta-1,3-dieen:
- Synthetisch rubber: Bij de productie van synthetisch rubber, zoals styreen-buta-1,3-dieenrubber (SBR) en polyButa-1,3-dieenrubber (PBR), wordt voornamelijk gebruik gemaakt van 1,3-butadieenrubber. Deze rubbers bieden uitstekende elasticiteit, veerkracht en slijtvastheid, waardoor ze ideaal zijn voor banden, auto-onderdelen, transportbanden en schoeisel.
- Kunststoffen: 1,3-butadieen is een essentieel monomeer voor de vervaardiging van verschillende kunststoffen, waaronder acrylonitril-buta-1,3-dieen-styreen (ABS) en styreen-buta-1,3-dieen (SB) kunststoffen) . Deze kunststoffen hebben een verbeterde slagvastheid, hittebestendigheid en maatvastheid, waardoor ze waardevol zijn voor toepassingen in consumentengoederen, apparaten en auto-onderdelen.
- Kleefstoffen: De sterke bindingsmogelijkheden van polymeren op basis van 1,3-butadieen maken ze tot een waardevol onderdeel in lijmformuleringen. Ze bieden hechting op een breed scala aan substraten, waardoor ze nuttig zijn voor lijmtoepassingen in industrieën zoals de bouw, houtbewerking en verpakking.
- Coatings: 1,3-Butadieen draagt bij aan de productie van coatings en verven met verbeterde duurzaamheid, flexibiliteit en hechtingseigenschappen. Harsen, zoals epoxy- en alkydharsen, gebruiken het bij hun synthese en vormen essentiële componenten van beschermende coatings voor metalen, beton en andere oppervlakken.
- Textiel en vezels: Bij de productie van synthetische vezels, zoals acrylonitril-buta-1,3-dieen (AB) vezels, wordt buta-1,3-dieen gebruikt. Deze vezels bezitten een hoge sterkte, goede maatvastheid en weerstand tegen chemicaliën, waardoor ze geschikt zijn voor textiel, tapijten en industriële stoffen.
- Brandstofadditieven: Buta-1,3-dieen verbetert het octaangetal van benzine als brandstofadditief dat bij de productie ervan wordt gebruikt. Het verbetert de verbrandingseigenschappen van benzine, wat resulteert in verbeterde motorprestaties en verminderde emissies.
Deze toepassingen benadrukken het brede nut van Buta-1,3-dieen in verschillende industrieën en dragen bij aan de ontwikkeling van verschillende producten die we in ons dagelijks leven tegenkomen.
Vragen:
Vraag: Wat is butadieen?
A: Buta-1,3-dieen is een chemische verbinding met de molecuulformule C4H6, bestaande uit een keten van vier koolstofatomen en twee dubbele bindingen.
Vraag: Wat is de IUPAC-naam voor het hoofdproduct wanneer 1,3-butadieen reageert met gelijke hoeveelheden HCl?
A: Het belangrijkste product, volgens de IUPAC-nomenclatuur, is 3-chloorbut-1-een.
Vraag: Hoeveel H-atomen bevat het molecuul 1,3-butadieen?
A: Buta-1,3-dieen bevat in totaal zes waterstofatomen (H).
Vraag: Wat is de relatie tussen de s-cis- en s-trans-vormen van 1,3-butadieen?
A: De s-cis- en s-trans-vormen van 1,3-butadieen zijn geometrische isomeren, die verschillen in de rangschikking van de substituenten rond de dubbele bindingen.
Vraag: Wat is het totale aantal knooppunten in de ψ3 MO van 1,3-butadieen?
A: De ψ3 moleculaire orbitaal van 1,3-butadieen bevat in totaal drie knooppunten.
Vraag: Hoeveel OM-bindingen heeft butadieen?
A: Butadieen heeft drie bindende moleculaire orbitalen (MO’s) gevormd uit overlappende atomaire orbitalen.
Vraag: Wat is de verwachte absorptie van butadieen?
A: Van butadieen wordt verwacht dat het ultraviolet (UV) licht absorbeert in het bereik van ongeveer 190 tot 200 nm vanwege het geconjugeerde systeem.
