Boterzuur of butaanzuur is een vetzuur met een korte keten dat veel voorkomt in zuivelproducten en bepaalde plantaardige voedingsmiddelen. Het heeft een scherpe, ranzige geur en wordt gebruikt als smaak- en parfumingrediënt in de voedingsindustrie. Het heeft ook potentiële gezondheidsvoordelen, waaronder ontstekingsremmende en kankerbestrijdende eigenschappen.
| IUPAC-naam | Butaanzuur |
| Moleculaire formule | C4H8O2 |
| CAS-nummer | 107-92-6 |
| Synoniemen | n-Butaanzuur, Boterzuuranhydride, Ethylazijnzuur, Ethylazijnzuuranhydride |
| InChi | InChI=1S/C4H8O2/c1-3-2-4(5)6/h3-4H,2H2,1H3,(H,5,6) |
Butyraat
Butyraat is een zout of ester van butaanzuur. Het is een anion met de chemische formule C4H7O2-, gevormd door de reactie van boterzuur met een base. Butyraat wordt vaak gebruikt in een verscheidenheid aan toepassingen, zoals als voedingsadditief in diervoeding, als weekmaker bij de productie van kunststoffen en als ingrediënt in sommige producten voor persoonlijke verzorging en cosmetische producten. Op medisch gebied is aangetoond dat butyraat potentiële ontstekingsremmende en kankerbestrijdende eigenschappen heeft en wordt onderzocht op het mogelijke gebruik ervan bij de behandeling van bepaalde ziekten.
Eigenschappen van boterzuur
Kookpunt van boterzuur:
Het kookpunt van boterzuur is 163°C. Bij deze temperatuur is de dampdruk van de vloeistof gelijk aan de atmosferische druk, waardoor deze kan koken en in een gas kan veranderen. Dit kookpunt is relatief laag in vergelijking met andere organische verbindingen en is belangrijk voor het gebruik ervan in verschillende industriële toepassingen.
Dichtheid van boterzuur g/ml:
De dichtheid van boterzuur is ongeveer 1,05 g/ml. Het heeft een relatief lage dichtheid in vergelijking met andere organische zuren, en de lage dichtheid beïnvloedt de fysische eigenschappen, zoals het vermogen om zich met andere vloeistoffen te mengen. De dichtheid van boterzuur is een belangrijke factor waarmee rekening moet worden gehouden bij gebruik in industriële toepassingen.
Molecuulgewicht van boterzuur:
Het molecuulgewicht van boterzuur is 88,11 g/mol. Het is de som van de atoomgewichten van de elementen van de molecuulformule (C4H8O2). Het molecuulgewicht is een belangrijke factor bij het bepalen van veel fysische en chemische eigenschappen van boterzuur, waaronder het kook- en smeltpunt, de dichtheid en de oplosbaarheid.
Molaire massa boterzuur:
De molaire massa van butaanzuur is 88,11 g/mol. Het is een organisch zuur met vier koolstofketens, dat 8 waterstofatomen, 2 zuurstofatomen en 4 koolstofatomen bevat. Deze combinatie van elementen geeft boterzuur zijn specifieke molecuulgewicht, wat belangrijk is voor veel van zijn fysische en chemische eigenschappen.
Smeltpunt van boterzuur:
Het smeltpunt van butaanzuur is -14°C. Dit betekent dat het bij die temperatuur van vast naar vloeibaar zal veranderen, waardoor het een organisch zuur met een relatief laag smeltpunt is. Dit lage smeltpunt is een belangrijk kenmerk van boterzuur en beïnvloedt de fysische eigenschappen ervan, zoals viscositeit en oplosbaarheid.
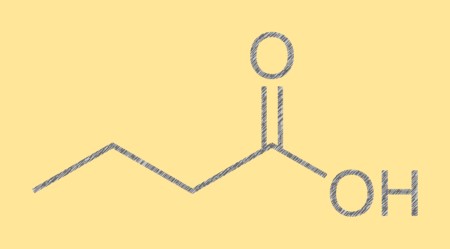
Structuur van boterzuur:
Butaanzuur heeft een rechte koolstofketen met aan één uiteinde een carboxylgroep (-COOH). Deze carboxylgroep geeft boterzuur zijn karakteristieke zure eigenschappen en is verantwoordelijk voor de sterke geur. De moleculaire structuur van butaanzuur is belangrijk bij het bepalen van de fysische en chemische eigenschappen ervan, evenals de reactiviteit ervan met andere verbindingen.
Boterzuurformule:
De chemische formule voor butaanzuur is C4H8O2. Deze formule vertegenwoordigt het aantal atomen van elk element in het molecuul. De vier koolstofatomen zijn verbonden in een rechte keten, met een zuurstofatoom en een hydroxylgroep (-OH) aan het ene uiteinde en een carboxylgroep (-COOH) aan het andere uiteinde.
NMR van boterzuur:
Nucleaire magnetische resonantie (NMR) spectroscopie is een krachtige analytische techniek die wordt gebruikt om de structuur van organische moleculen zoals butaanzuur te bepalen. NMR-spectra geven informatie over de chemische omgeving van de atomen in het molecuul, inclusief de aanwezige soorten bindingen, hun rangschikking en de oriëntatie van het molecuul. Deze informatie is belangrijk voor het begrijpen van de reactiviteit en fysische eigenschappen van boterzuur.
| Verschijning | Heldere, kleurloze tot gele vloeistof |
| Soortelijk gewicht | 1,05 g/ml |
| Kleur | Helder, kleurloos tot geel |
| Geur | Sterke, scherpe, ranzige geur |
| Molaire massa | 88,11 g/mol |
| Dikte | 1,05 g/ml |
| Fusie punt | -14°C |
| Kookpunt | 163°C |
| Flitspunt | 85°C |
| oplosbaarheid in water | Oplosbaar |
| Oplosbaarheid | Oplosbaar in ethanol, ether en andere organische oplosmiddelen |
| Dampdruk | 0,04 mmHg (bij 20°C) |
| Dampdichtheid | 1,04 (lucht = 1) |
| pKa | 4,83 |
| pH | 3,5-5,5 |
Veiligheid en gevaren van boterzuur
Boterzuur wordt als een gevaarlijk materiaal beschouwd vanwege de sterke, scherpe geur en corrosieve eigenschappen. Inademing van boterzuurdampen of -nevels kan irritatie aan de ogen, neus en luchtwegen veroorzaken, evenals hoofdpijn, duizeligheid en misselijkheid. Bovendien kan butaanzuur huid- en oogirritatie veroorzaken en schadelijk zijn bij inslikken. Het is belangrijk om voorzichtig om te gaan met boterzuur en beschermende kleding te dragen, zoals handschoenen en een veiligheidsbril, wanneer u ermee werkt. Het moet ook worden opgeslagen in een goed geventileerde ruimte, uit de buurt van warmtebronnen, om het vrijkomen van gevaarlijke dampen te voorkomen. Bij contact met de huid of ogen, overvloedig spoelen met water en indien nodig een arts raadplegen. Bij inslikken geen braken opwekken en onmiddellijk medische hulp inroepen.
| Gevarensymbolen | Bijtend, irriterend |
| Beveiligingsbeschrijving | S26-S36/37/39-S45 |
| VN-identificatienummers | UN3265 |
| HS-code | 2915.90.90 |
| Gevarenklasse | 8 (corrosief) |
| Verpakkingsgroep | III |
| Toxiciteit | Oraal LD50: 710 mg/kg (rat)<br>Inhalatie LC50: niet beschikbaar<br>Huidirritatie: licht irriterend<br>Oogirritatie: matig irriterend |
Methoden voor de synthese van boterzuur
Butaanzuur (C4H8O2) kan op verschillende manieren worden gesynthetiseerd, waaronder biologische, chemische en enzymatische processen.
De biologische synthese van butaanzuur omvat de fermentatie van koolhydraten door bacteriën, zoals Clostridium acetobutylicum, in afwezigheid van zuurstof. Dit proces produceert een mengsel van boterzuur, azijnzuur en propionzuur, genaamd oplosmiddelzuur.
De chemische synthese van butaanzuur kan worden uitgevoerd door oxidatie van butanol of door hydrolyse van esters, zoals ethylbutyraat.
De enzymatische synthese van butaanzuur wordt uitgevoerd met behulp van een lipase-enzym om de verestering van butanol en azijnzuur te katalyseren.
Ongeacht de synthesemethode wordt butaanzuur vaak gezuiverd door destillatie- of extractietechnieken om het zuivere product te verkrijgen.
Het is belangrijk op te merken dat de keuze van de synthesemethode de kwaliteit, opbrengst en kosten van het eindproduct kan beïnvloeden. Het is daarom belangrijk om bij het selecteren van een butaanzuursynthesemethode zorgvuldig rekening te houden met de specifieke behoeften en vereisten van elke toepassing. .
Gebruik van boterzuur
Boter, kaas en andere zuivelproducten bevatten butaanzuur, dat vaak wordt gebruikt als smaakstof in voedingsmiddelen en bij de vervaardiging van kunststoffen, oplosmiddelen en andere industriële chemicaliën.
Onderzoekers hebben butaanzuur ook gebruikt om gastro-intestinale stoornissen zoals het prikkelbare darm syndroom, de ziekte van Crohn en colitis ulcerosa te behandelen, omdat het ontstekingen vermindert, de darmgezondheid verbetert en genezing bevordert.
Bovendien heeft butaanzuur schimmelwerende eigenschappen en kan het de groei van kankercellen remmen en apoptose in bepaalde soorten kankercellen induceren.
Bovendien hebben sommige onderzoeken gesuggereerd dat butaanzuur neuronen kan beschermen tegen schade veroorzaakt door neurodegeneratieve ziekten zoals de ziekte van Parkinson en de ziekte van Alzheimer. Tenslotte wordt butaanzuur vaak gebruikt als conserveermiddel in voedingsmiddelen omdat het de groei van bacteriën, schimmels en andere micro-organismen remt.
Vragen:
Wat is boterzuur?
Butaanzuur is een vetzuur met een korte keten en de molecuulformule CH3CH2CH2COOH. Het is een kleurloze, in water oplosbare vloeistof met een sterke, scherpe geur en is van nature aanwezig in zuivelproducten, zoals kaas en boter, maar ook in sommige plantaardige oliën. Butaanzuur wordt in verschillende toepassingen gebruikt, onder meer als smaak- en geuringrediënt, als chemisch tussenproduct en als toevoegingsmiddel in diervoeding. Het is ook van belang op medisch gebied vanwege de potentiële ontstekingsremmende en kankerbestrijdende eigenschappen.
Hoe boterzuur maken?
Butaanzuur kan worden gesynthetiseerd door biologische processen, zoals de fermentatie van koolhydraten door bacteriën, maar ook door chemische en enzymatische processen, zoals de oxidatie van butanol of de verestering van butanol en azijnzuur. met behulp van een lipase-enzym. De gebruikte synthesemethode kan de kwaliteit, opbrengst en kosten van het eindproduct beïnvloeden.
Voltooi de zuur-base-reactie tussen boterzuur hc4h7o2 en kaliumhydroxide koh.
De reactie tussen butaanzuur (HC4H7O2) en kaliumhydroxide (KOH) kan als volgt worden weergegeven:
HC4H7O2 + KOH → KC4H7O2 + H2O
Bij deze reactie werkt butaanzuur (HC4H7O2) als een zuur en doneert het een proton (H+) aan kaliumhydroxide (KOH), dat als base fungeert en het proton accepteert. Dit resulteert in de vorming van kaliumbutyraat (KC4H7O2) en water (H2O). Deze reactie kan worden geclassificeerd als een neutralisatiereactie, omdat deze resulteert in de neutralisatie van zuur butaanzuur en basisch kaliumhydroxide om een neutraal zout te vormen.
Indool-3-boterzuur?
Indool-3-boterzuur (IBA) is een plantengroeiregulator en een type auxine dat veel in de tuinbouw wordt gebruikt om de wortelvorming en groei van een verscheidenheid aan plantensoorten te stimuleren. Tuinbouwers dopen de afgesneden uiteinden in een oplossing van IBA opgelost in water of passen de oplossing toe als bladspray voor het vermeerderen en wortelen van stekken van bladverliezende en groenblijvende bomen, struiken en kruidachtige planten voor de productie van sierplanten, fruitbomen, bosbomen, groenten . en bloemengewassen. Het gebruik van IBA moet echter zorgvuldig worden gecontroleerd om overmatige toepassing en mogelijke schade aan de plant of het milieu te voorkomen.
