Benzylalcohol is een kleurloze vloeistof met een aangenaam aroma. Het wordt gebruikt als oplosmiddel, conserveermiddel en geurstof in verschillende producten voor persoonlijke verzorging en medicijnen.
| IUPAC-naam | Benzyl alcohol |
| Moleculaire formule | C7H8O |
| CAS-nummer | 100-51-6 |
| Synoniemen | Fenylmethanol, benzeenmethanol, hydroxytolueen, alfa-tolueenol |
| InChi | InChI=1S/C7H8O/c8-6-7-4-2-1-3-5-7/h1-5,8H,6H2 |
Eigenschappen van benzylalcohol
Benzylalcoholformule
De formule voor benzeenmethanol is C7H8O. Het bestaat uit zeven koolstofatomen, acht waterstofatomen en één zuurstofatoom. Deze chemische formule vertegenwoordigt de rangschikking van atomen in een molecuul benzeenmethanol.
Benzylalcohol Molaire massa
De molaire massa van benzeenmethanol wordt berekend door de atoommassa’s van de samenstellende elementen op te tellen. Koolstof heeft een molaire massa van 12,01 g/mol, waterstof heeft een molaire massa van 1,01 g/mol en zuurstof heeft een molaire massa van 16,00 g/mol. Door deze waarden op te tellen wordt de molaire massa van benzeenmethanol bepaald op 108,14 g/mol.
Kookpunt van benzylalcohol
Benzeenmethanol heeft een kookpunt van ongeveer 205°C (401°F). Dit is de temperatuur waarbij de vloeistof overgaat in een gasvormige toestand, meestal bij verhitting onder standaard atmosferische druk. Het kookpunt van benzeenmethanol bepaalt de vluchtigheid en bruikbaarheid ervan in verschillende toepassingen.
Smeltpunt van benzylalcohol
Het smeltpunt van benzeenmethanol is ongeveer -15°C (5°F). Deze temperatuur geeft het punt aan waarop de vaste vorm van benzeenmethanol bij verhitting vloeibaar wordt. Het smeltpunt is een belangrijk kenmerk voor de opslag en hantering van de stof.
Dichtheid van benzylalcohol g/ml
Benzeenmethanol heeft een dichtheid van ongeveer 1,045 g/ml. Dichtheid vertegenwoordigt de massa van een stof per volume-eenheid. Deze eigenschap is nuttig bij het bepalen van de concentratie of zuiverheid van benzeenmethanol in een oplossing.
Benzylalcohol Molecuulgewicht
Het molecuulgewicht van benzeenmethanol is 108,14 g/mol. Het is de som van de atoomgewichten van alle atomen in een molecuul. Het molecuulgewicht levert waardevolle informatie op over de massa van de verbinding en vergemakkelijkt berekeningen met stoichiometrie en chemische reacties.
Structuur van benzylalcohol
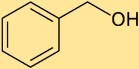
De structuur van benzeenmethanol bestaat uit een benzeenring bevestigd aan een hydroxylgroep (-OH). De hydroxylgroep is bevestigd aan het koolstofatoom van de benzeenring. Deze structuur geeft benzeenmethanol zijn unieke eigenschappen en chemische reactiviteit.
Oplosbaarheid van benzylalcohol
Benzeenmethanol is tot op zekere hoogte oplosbaar in water. Het vertoont een matige oplosbaarheid vanwege de aanwezigheid van de hydroxylgroep, die waterstofbinding met watermoleculen mogelijk maakt. Benzeenmethanol is echter beter oplosbaar in organische oplosmiddelen zoals ethanol en chloroform. De oplosbaarheid van benzeenmethanol heeft invloed op het gebruik ervan als oplosmiddel of additief in verschillende industrieën.
| Verschijning | Kleurloze vloeistof |
| Soortelijk gewicht | 1,045 g/ml |
| Kleur | Kleurloos |
| Geur | Aangenaam aroma |
| Molaire massa | 108,14 g/mol |
| Dikte | 1,045 g/ml |
| Fusie punt | -15°C (5°F) |
| Kookpunt | 205°C (401°F) |
| Flitspunt | 93°C (199°F) |
| oplosbaarheid in water | Oplosbaar |
| Oplosbaarheid | Oplosbaar in organische oplosmiddelen zoals ethanol en chloroform |
| Dampdruk | 0,39 mmHg bij 25°C |
| Dampdichtheid | 3,74 (lucht = 1) |
| pKa | 15.4 |
| pH | Ongeveer 7 |
Veiligheid en gevaar van benzylalcohol
Benzeenmethanol brengt bepaalde veiligheidsoverwegingen en gevaren met zich mee waarmee rekening moet worden gehouden. Het kan bij direct contact oog- en huidirritatie veroorzaken. Daarom worden beschermende maatregelen zoals handschoenen en een bril aanbevolen. Het inslikken of inademen van grote hoeveelheden benzeenmethanol kan misselijkheid, hoofdpijn en duizeligheid veroorzaken. Het is essentieel om benzeenmethanol in een goed geventileerde ruimte te gebruiken om dampophoping te voorkomen. Bovendien kan langdurige of herhaalde blootstelling aan hoge concentraties benzeenmethanol mogelijk leverschade veroorzaken. Om de risico’s te minimaliseren en de veiligheid in de werkomgeving te garanderen, moeten de juiste opslag- en hanteringsprocedures worden gevolgd.
| Gevarensymbolen | Irriterend |
| Beveiligingsbeschrijving | Schadelijk bij inslikken, veroorzaakt huid- en oogirritatie. Gebruik passende beschermende maatregelen. |
| VN-identificatienummers | Een 1986 |
| HS-code | 29062100 |
| Gevarenklasse | 6.1 |
| Verpakkingsgroep | III |
| Toxiciteit | Bij hoge concentraties giftig voor de lever. |
Methoden voor de synthese van benzylalcohol
Verschillende methoden synthetiseren benzeenmethanol.
Een veelgebruikte methode is de katalytische hydrogenering van benzaldehyde . Benzaldehyde reageert met waterstofgas in aanwezigheid van een metaalkatalysator zoals palladium of platina om benzeenmethanol te produceren. De katalysator vergemakkelijkt de reductie van de carbonylgroep in benzaldehyde tot benzeenmethanol.
Een andere methode omvat de oxidatie van tolueen. Tolueen wordt eerst geoxideerd om benzaldehyde te vormen met behulp van een oxidatiemiddel zoals kaliumpermanganaat of chroomzuur. Vervolgens reduceert een reductiemiddel zoals natriumboorhydride of waterstofgas het benzaldehyde verder om benzeenmethanol te vormen.
Benzylchloride reageert met natrium- of kaliumhydroxide om benzeenmethanol te produceren door de synthese van Williamson-ether. Het proces omvat de behandeling van benzylchloride met een hydroxideoplossing, resulterend in de vorming van benzeenmethanol.
Deze synthesemethoden bieden verschillende routes om benzeenmethanol te verkrijgen, elk met zijn voordelen en beperkingen. De keuze voor de methode is afhankelijk van factoren als de beschikbaarheid van grondstoffen, de gewenste zuiverheid en specifieke toepassingseisen. Het is belangrijk om veiligheidsmaatregelen in acht te nemen en chemicaliën in een gecontroleerde omgeving te hanteren bij het uitvoeren van deze syntheseprocessen.
Gebruik van benzylalcohol
Benzeenmethanol vindt verschillende toepassingen in verschillende industrieën vanwege zijn veelzijdige eigenschappen. Hier zijn enkele veelvoorkomende toepassingen:
- Oplosmiddel: Benzeenmethanol lost effectief oliën, harsen, kleurstoffen en cellulosederivaten op, waardoor het een ideaal oplosmiddel is voor coatings, verven en inkten.
- Conserveermiddel: Benzeenmethanol conserveert een breed scala aan producten, waaronder artikelen voor persoonlijke verzorging, cosmetica en farmaceutische producten, door de groei van bacteriën en schimmels actief te remmen.
- Geurbestanddeel: Benzeenmethanol geeft een aangenaam aroma en fungeert als geuringrediënt in parfums, colognes en geurproducten.
- Medicijnen: Verschillende medicijnen zoals plaatselijke zalven, lotions en antiseptische oplossingen gebruiken benzeenmethanol als het actieve farmaceutische ingrediënt.
- Smaakstof: Benzeenmethanol verbetert de smaak van voedingsmiddelen en dranken als actieve smaakstof.
- Reinigingsproducten: De oplosmiddel- en antimicrobiële eigenschappen van benzeenmethanol maken het tot een waardevol ingrediënt in schoonmaakmiddelen, was- en ontsmettingsmiddelen.
- Industriële toepassingen: Industrieën gebruiken benzeenmethanol als oplosmiddel en reactiemedium bij de productie van polymeren en andere industriële processen.
- Textielindustrie: Benzeenmethanol vergemakkelijkt het spinproces van synthetische vezels in de textielindustrie.
- Chemisch tussenproduct: Benzeenmethanol neemt actief deel als tussenproduct bij de synthese van verschillende chemicaliën, waaronder benzylesters, benzylethers en benzylaminen.
- Veterinaire toepassingen: In de diergeneeskunde dient benzeenmethanol als verdovingsmiddel en behandelt het actief oorinfecties bij dieren.
Deze uiteenlopende toepassingen benadrukken het belang en de wijdverbreide bruikbaarheid van benzylalcohol in meerdere industrieën.
Vragen:
Vraag: Wat is benzylalcohol?
A: Benzeenmethanol is een kleurloze vloeistof met een aangenaam aroma, die vaak wordt gebruikt als oplosmiddel, conserveermiddel en geurstof in verschillende producten voor persoonlijke verzorging en medicijnen.
Vraag: Is benzylalcohol slecht voor haar?
A: Benzeenmethanol is, indien gebruikt in de juiste concentraties, over het algemeen veilig voor het haar en wordt vaak aangetroffen in haarverzorgingsproducten als conserveermiddel of geurstof.
Vraag: Is benzylalcohol halal?
A: De halalstatus van benzeenmethanol hangt af van de bron en het productieproces. Als het afkomstig is van geautoriseerde bronnen en volgens halal-normen wordt geproduceerd, kan het als halal worden beschouwd.
Vraag: Waar kan ik benzylalcohol kopen?
A: Benzeenmethanol kan bij verschillende bronnen worden gekocht, waaronder chemische leveranciers, online retailers en lokale apotheken of winkels die cosmetische ingrediënten verkopen.
Vraag: Waar wordt benzylalcohol voor gebruikt?
A: Benzeenmethanol wordt gebruikt als oplosmiddel, conserveermiddel, geuringrediënt en farmaceutisch ingrediënt in producten voor persoonlijke verzorging, cosmetica, medicijnen en industriële toepassingen.
Vraag: Tolueen naar benzylalcohol?
A: Tolueen kan worden omgezet in benzeenmethanol via een tweestapsproces: oxidatie van tolueen tot benzaldehyde, gevolgd door reductie van het benzaldehyde tot benzylalcohol.
Vraag: Van benzylchloride naar benzylalcohol?
A: Benzylchloride kan worden omgezet in benzeenmethanol door het te behandelen met natrium- of kaliumhydroxide via Williamson-ethersynthese.
Vraag: Van aniline naar benzylalcohol?
A: Aniline kan worden omgezet in benzeenmethanol via een reeks stappen waarbij aniline wordt gereduceerd tot benzylamine, gevolgd door de oxidatie van benzylamine tot benzylalcohol.
Vraag: Benzeenmethanol naar 2-fenylethaanzuur?
A: Benzeenmethanol kan worden omgezet in 2-fenylethaanzuur door oxidatie met behulp van sterke oxidatiemiddelen zoals kaliumpermanganaat of chroomzuur.
Vraag: Hoe kan ik benzaldehyde omzetten in benzylalcohol?
A: Benzaldehyde kan worden gereduceerd tot benzeenmethanol met behulp van reductiemiddelen zoals natriumboorhydride of waterstofgas in aanwezigheid van een katalysator.
Vraag: Wat is zuurder: benzylalcohol of fenol?
A: Fenol is zuurder dan benzeenmethanol vanwege resonantiestabilisatie van het fenox-ion dat wordt gevormd tijdens deprotonering.
