Acetylsalicylzuur (C9H8O4) of aspirine is een medicijn dat vaak wordt gebruikt om pijn te verlichten, koorts te verminderen en bloedstolling te voorkomen. Het behoort tot de klasse geneesmiddelen die niet-steroïde anti-inflammatoire geneesmiddelen (NSAID’s) worden genoemd.
| IUPAC-naam | 2-acetoxybenzoëzuur |
| Moleculaire formule | C9H8O4 |
| CAS-nummer | 50-78-2 |
| Synoniemen | Aspirine, ASA, acetylsalicylaat, enz. |
| InChi | InChI=1S/C9H8O4/c1-6(10)13-8-5-3-2-4-7(8)9(11)12/h2-5H,1H3,(H,11,12) |
Eigenschappen van acetylsalicylzuur
Acetylsalicylzuurformule
De chemische formule voor acetylsalicylzuur is C9H8O4. Het bestaat uit negen koolstofatomen, acht waterstofatomen en vier zuurstofatomen.
Acetylsalicylzuur Molaire massa
De molaire massa van acetylsalicylaat wordt berekend door de atoommassa’s van de samenstellende elementen op te tellen. Dit is ongeveer 180,16 gram per mol (g/mol).
Kookpunt van acetylsalicylzuur
Acetylsalicylaat heeft een kookpunt van ongeveer 140 graden Celsius (°C). Bij deze temperatuur verandert de verbinding van vloeibare naar gasvormige toestand.
Acetylsalicylzuur Smeltpunt
Het smeltpunt van acetylsalicylaat is ongeveer 135 graden Celsius (°C). Wanneer het tot deze temperatuur wordt verwarmd, verandert het van een vaste stof in een vloeistof.
Dichtheid van acetylsalicylzuur g/ml
De dichtheid van acetylsalicylaat is doorgaans ongeveer 1,40 gram per milliliter (g/ml). Deze waarde geeft de massa van de verbinding per volume-eenheid aan.
Acetylsalicylzuur Molecuulgewicht
Het molecuulgewicht van acetylsalicylaat is ongeveer 180,16 gram per mol (g/mol). Het vertegenwoordigt de som van de atoomgewichten van alle atomen van een molecuul van de verbinding.
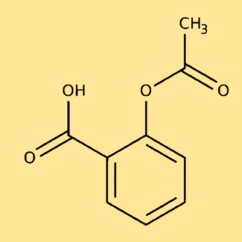
Structuur van acetylsalicylzuur
De structuur van acetylsalicylaat bestaat uit een benzeenring waaraan een carbonzuurgroep (-COOH) en een acetylgroep (-COCH3) zijn bevestigd. Deze structuur geeft het zijn unieke eigenschappen en farmacologische effecten.
Oplosbaarheid van acetylsalicylzuur
Acetylsalicylaat is slecht oplosbaar in water, met een oplosbaarheid van ongeveer 1 tot 2 gram per 100 milliliter (g/100 ml) water bij kamertemperatuur. Het is echter beter oplosbaar in organische oplosmiddelen zoals ethanol en aceton.
Deze eigenschappen van acetylsalicylaat spelen een cruciale rol in de farmaceutische toepassingen ervan, zoals het gebruik ervan als pijnstiller, koortsverlagend middel en ontstekingsremmend middel.
| Verschijning | Wit kristallijn poeder |
| Soortelijk gewicht | 1.40 |
| Kleur | Kleurloos |
| Geur | Geurloos |
| Molaire massa | 180,16 g/mol |
| Dikte | 1,40 g/ml |
| Fusie punt | 135°C |
| Kookpunt | 140°C |
| Flitspunt | Niet toepasbaar |
| oplosbaarheid in water | Slecht oplosbaar |
| Oplosbaarheid | Oplosbaar in organische oplosmiddelen |
| Dampdruk | Niet beschikbaar |
| Dampdichtheid | Niet beschikbaar |
| pKa | 3,5 (carbonzuurgroep) |
| pH | 2.4 (indien opgelost in water) |
Veiligheid en gevaren van acetylsalicylzuur
Acetylsalicylaat moet met voorzichtigheid worden gehanteerd vanwege de potentiële veiligheidsrisico’s. Het kan bij contact of inademing irritatie van de huid, ogen en luchtwegen veroorzaken. Inname van hoge doses kan leiden tot maag-darmklachten en zelfs tot toxiciteit. Mensen met een voorgeschiedenis van bloedingsstoornissen of maagzweren moeten bijzonder voorzichtig zijn bij het gebruik van dit middel. Zoals bij elk medicijn zijn allergische reacties mogelijk en moet onmiddellijk medische hulp worden ingeroepen als symptomen zoals ademhalingsmoeilijkheden of zwelling optreden. Het is belangrijk om de aanbevolen doseringen te volgen en een arts te raadplegen voordat u acetylsalicylaat gebruikt, vooral in combinatie met andere medicijnen.
| Gevarensymbolen | SGH07 |
| Beveiligingsbeschrijving | Veroorzaakt oog- en huidirritatie. Schadelijk bij inslikken of inademen. |
| VN-identificatienummers | UN 2811 (massief) |
| HS-code | 2918.11.00 |
| Gevarenklasse | 6.1 (giftige stoffen) |
| Verpakkingsgroep | III |
| Toxiciteit | Matige toxiciteit met potentiële gastro-intestinale effecten. |
Deze risico- en veiligheidseigenschappen beschrijven de potentiële gevaren die verband houden met acetylsalicylaat en bieden richtlijnen voor de veilige hantering, het transport en de opslag ervan. Het is belangrijk om de juiste veiligheidsmaatregelen en voorschriften te volgen bij het hanteren van deze stof om elk potentieel risico voor de menselijke gezondheid en het milieu tot een minimum te beperken.
Methoden voor de synthese van acetylsalicylzuur
Verschillende methoden maken de synthese van acetylsalicylaat mogelijk.
Een veelgebruikte methode om acetylsalicylaat te synthetiseren omvat het veresteren van salicylzuur met azijnzuuranhydride in aanwezigheid van een katalysator zoals zwavelzuur of fosforzuur . De reactie levert acetylsalicylaat en azijnzuur op als bijproducten, en het filtratieproces verzamelt deze na afkoelen van het reactiemengsel.
Een andere methode maakt gebruik van azijnzuur in plaats van azijnzuuranhydride . Een mengsel van salicylzuur en azijnzuur wordt verwarmd met een zure katalysator, meestal zwavelzuur. De reactie verloopt onder vorming van acetylsalicylaat en water. Tijdens het afkoelen wordt uit het verkregen mengsel het vaste product geïsoleerd.
De Kolbe-Schmitt-reactie biedt een alternatieve route om acetylsalicylaat te bereiden. Natriumfenolaat, verkregen uit de reactie van salicylzuur met natriumhydroxide, ondergaat een koolstofdioxidebehandeling onder hoge druk en temperatuur. Het resulterende salicylaat wordt vervolgens aangezuurd, waardoor acetylsalicylaat ontstaat.
Deze synthesemethoden maken het mogelijk om acetylsalicylaat op industriële schaal te produceren, waardoor een stabiele en betrouwbare aanvoer voor verschillende toepassingen in de farmaceutische industrie wordt gegarandeerd. Het is belangrijk op te merken dat deze processen expertise en naleving van veiligheidsprotocollen vereisen om een efficiënte en veilige productie te garanderen.
Gebruik van acetylsalicylzuur
Acetylsalicylaat vindt een breed scala aan toepassingen vanwege zijn gunstige eigenschappen. Hier zijn enkele belangrijke toepassingen:
- Pijnverlichting: Acetylsalicylaat verlicht milde tot matige pijn, zoals hoofdpijn, tandpijn en spierpijn.
- Koortsreductie: Acetylsalicylaat vermindert effectief koorts, waardoor het een voorkeurskeuze is voor het beheersen van koortsaandoeningen.
- Ontstekingsremmende effecten: Acetylsalicylaat heeft ontstekingsremmende eigenschappen, waardoor het nuttig is voor het verminderen van ontstekingen die gepaard gaan met aandoeningen zoals artritis en sportblessures.
- Preventie van bloedstolsels: Als antistollingsmiddel helpt acetylsalicylaat de vorming van bloedstolsels te voorkomen, waardoor het risico op hartaanvallen en beroertes wordt verminderd.
- Cardiovasculaire gezondheid: Beroepsbeoefenaren in de gezondheidszorg kunnen regelmatige lage doses acetylsalicylaat aanbevelen aan mensen met een hoog risico op hart- en vaatziekten om hun cardiovasculaire gezondheid te verbeteren.
- Antibloedplaatjestherapie: Bij antibloedplaatjestherapie wordt gebruik gemaakt van acetylsalicylaat om de aggregatie van bloedplaatjes actief te remmen en de kans op de vorming van bloedstolsels actief te verminderen bij aandoeningen zoals atriale fibrillatie en na het plaatsen van een stent.
- Preventie van voorbijgaande ischemische aanvallen (TIA): Acetylsalicylaat kan worden voorgeschreven om voorbijgaande ischemische aanvallen te voorkomen, dit zijn korte episodes van verminderde bloedtoevoer naar de hersenen.
- Profylaxe van reumatische koorts: Bij risicopatiënten wordt acetylsalicylaat in sommige gevallen actief gebruikt voor profylaxe tegen reumatische koorts.
Deze verschillende toepassingen demonstreren de grote bruikbaarheid van acetylsalicylaat bij de behandeling van pijn, ontstekingen, koorts en hart- en vaatziekten. Het is echter essentieel om een beroepsbeoefenaar in de gezondheidszorg te raadplegen voordat u acetylsalicylaat gebruikt, om zeker te zijn van de juiste dosering en geschiktheid voor specifieke omstandigheden.
Vragen:
Vraag: Hoeveel pi-bindingen zijn er aanwezig in acetylsalicylzuur?
A: Acetylsalicylaat bevat twee pi-bindingen.
Vraag: Welke delen van acetylsalicylzuur zijn stijf?
A: De benzeenring en de carbonzuurgroep van acetylsalicylzuur worden als stijf beschouwd.
Vraag: Hoeveel sigmabindingen zijn er aanwezig in acetylsalicylzuur?
A: Acetylsalicylaat heeft 20 sigma-bindingen.
Vraag: Hoeveel sigmabindingen zijn er aanwezig in acetylsalicylzuur en welke delen zijn stijf?
A: Acetylsalicylaat bestaat uit 20 sigma-bindingen, waarbij de benzeenring en de carbonzuurgroep stijve delen zijn.
Vraag: Wat is acetylsalicylzuur?
A: Acetylsalicylaat, algemeen bekend als aspirine, is een medicijn dat wordt gebruikt om pijn te verlichten, koorts te verminderen en bloedstolling te voorkomen.
Vraag: Wat is de pH van een 0,10 M waterige oplossing van acetylsalicylzuur?
A: De pH van een 0,10 M waterige oplossing van acetylsalicylaat kan niet worden bepaald zonder aanvullende informatie.
Vraag: Waar wordt acetylsalicylzuur voor gebruikt?
A: Acetylsalicylaat wordt gebruikt als pijnstiller (pijnstiller), koortswerend middel (verlaagt koorts), ontstekingsremmende medicijnen en bloedplaatjesaggregatieremmers.
Vraag: Wat is het bereik van serumacetylsalicylzuur?
A: Het bereik van serumacetylsalicylaat kan variëren afhankelijk van de specifieke medische aandoening die wordt behandeld. Het wordt bepaald door gezondheidswerkers via geïndividualiseerde monitoring.
Vraag: Kan acetylsalicylzuur tinnitus veroorzaken?
A: Ja, in zeldzame gevallen kan acetylsalicylaat als bijwerking tinnitus (oorsuizen) veroorzaken. Als u dergelijke symptomen ervaart, is het raadzaam een arts te raadplegen.
