Acetofenon of methylfenylketon is een aromatische organische verbinding met de formule C8H8O. Het wordt gebruikt bij de productie van parfums en harsen, en als oplosmiddel en tussenproduct in farmaceutische producten.
| IUPAC-naam | 1-fenylethanon |
| Moleculaire formule | C8H8O |
| CAS-nummer | 98-86-2 |
| Synoniemen | Methylfenylketon, fenylmethylketon, AP, acetylbenzeen, benzoylmethyl, ethylfenylketon, Hypnon |
| InChi | InChI=1S/C8H8O/c1-7(9)8-5-3-2-4-6-8/h2-6H,1H3 |
Structuur van acetofenon
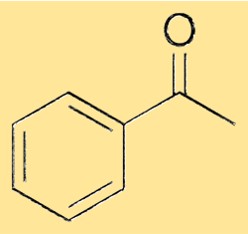
De structuur van acetofenon bestaat uit een fenylgroep die via een enkele binding aan een carbonylgroep is gekoppeld. De carbonylgroep bestaat uit een koolstofatoom dat dubbel gebonden is aan een zuurstofatoom. De fenylgroep is een zesledige ring van koolstofatomen waaraan vijf waterstofatomen zijn bevestigd, en de zesde positie wordt ingenomen door het carbonylkoolstofatoom. Deze structuur geeft acetofenon zijn karakteristieke eigenschappen en zorgt ervoor dat het kan dienen als veelzijdige grondstof voor de synthese van allerlei chemicaliën.
Acetofenon smeltpunt
Acetofenon heeft een smeltpunt van -15,7°C. Het smeltpunt is de temperatuur waarbij een vaste stof bij constante druk in een vloeistof verandert. Acetofenon is bij kamertemperatuur een kristallijne vaste stof en heeft een relatief laag smeltpunt vergeleken met andere soortgelijke verbindingen. Het smeltpunt van een verbinding wordt bepaald door de moleculaire structuur en de sterkte van de intermoleculaire krachten.
IR-spectrum van acetofenon
Het IR-spectrum van acetofenon vertoont karakteristieke pieken bij 1705 cm^-1, wat overeenkomt met de carbonylgroep, en bij 3030-3100 cm^-1, wat overeenkomt met de uitrekking van aromatisch CH. Deze pieken verschaffen belangrijke informatie over de functionele groepen die in het molecuul aanwezig zijn.
Molaire massa van acetofenon:
Acetofenon heeft een molaire massa van 120,15 g/mol. Het is een aromatische organische verbinding met een carbonylgroep bevestigd aan een fenylring. De molmassa is de som van de atoommassa’s van de atomen in één mol van de verbinding. In het geval van acetofenon heeft het 8 koolstofatomen, 8 waterstofatomen en één zuurstofatoom, wat een totaal van 17 atomen in een molecuul oplevert. Molaire massa is een belangrijke eigenschap van een verbinding omdat deze wordt gebruikt om de hoeveelheid stof in een bepaald monster te berekenen, wat nodig is voor verschillende toepassingen in de chemie en de industrie.
Kookpunt van acetofenon
Acetofenon heeft een kookpunt van 202°C. Het kookpunt is de temperatuur waarbij een vloeistof bij constante druk in een gas verandert. Acetofenon is een vluchtige organische verbinding en heeft een relatief hoog kookpunt in vergelijking met andere soortgelijke verbindingen. Het kookpunt van een verbinding wordt bepaald door de sterkte van de intermoleculaire krachten, de krachten die moleculen bij elkaar houden in een vloeibare of vaste toestand. In het geval van acetofenon heeft het een polaire carbonylgroep die waterstofbruggen kan vormen met andere acetofenonmoleculen, wat de intermoleculaire krachten versterkt en het kookpunt verhoogt.
Dichtheid van methylfenylketon g/ml
Methylfenylketon heeft een dichtheid van 1,03 g/ml bij kamertemperatuur. Dichtheid is de massa van een stof per volume-eenheid. Methylfenylketon is een vloeistof bij kamertemperatuur en heeft een relatief hoge dichtheid in vergelijking met andere soortgelijke verbindingen. De dichtheid van een verbinding wordt bepaald door het molecuulgewicht en de dichtheid van de moleculen in een bepaald volume. In het geval van methylfenylketon heeft het een relatief hoog molecuulgewicht en een relatief compacte moleculaire structuur, waardoor de pakking van de moleculen efficiënter wordt en de dichtheid toeneemt.
Molecuulgewicht van methylfenylketon
Methylfenylketon heeft een molecuulgewicht van 120,15 g/mol. Het molecuulgewicht is de som van de atoomgewichten van alle atomen in een molecuul. Methylfenylketon heeft 8 koolstofatomen, 8 waterstofatomen en één zuurstofatoom, wat een totaal van 17 atomen in een molecuul oplevert. Het molecuulgewicht is een belangrijke eigenschap van een verbinding omdat het wordt gebruikt om de hoeveelheid stof in een bepaald monster te berekenen, wat nodig is voor verschillende toepassingen in de chemie en de industrie.
| Verschijning | Kleurloze tot lichtgele vloeistof |
| Soortelijk gewicht | 1,028-1,031 bij 25°C |
| Kleur | Kleurloos tot lichtgeel |
| Geur | Zoet, bloemig, honingachtig |
| Molaire massa | 120,15 g/mol |
| Dikte | 1,03 g/ml bij 25°C |
| Fusie punt | -15,7°C |
| Kookpunt | 202°C |
| Flitspunt | 78°C |
| oplosbaarheid in water | 3,3 g/l bij 25°C |
| Oplosbaarheid | Oplosbaar in alcohol, ether, chloroform en benzeen |
| Dampdruk | 0,27 mmHg bij 25°C |
| Dampdichtheid | 4,15 (lucht = 1) |
| pKa | 10.01 |
| pH | Niet van toepassing (methylfenylketon is noch een zuur, noch een base) |
Veiligheid en gevaren van methylfenylketon
Methylfenylketon kan gevaarlijk zijn als het niet op de juiste manier wordt behandeld. Het kan bij contact of inademing irritatie van de huid, ogen en luchtwegen veroorzaken. Directe blootstelling aan hoge concentraties methylfenylketondamp kan hoofdpijn, duizeligheid of misselijkheid veroorzaken. Inslikken van methylfenylketon kan gastro-intestinale irritatie, braken of diarree veroorzaken. Methylfenylketon is ook brandbaar en kan met lucht explosieve mengsels vormen. Het moet worden bewaard op een koele, droge, goed geventileerde plaats, uit de buurt van ontstekingsbronnen. Bij het hanteren van methylfenylketon moeten persoonlijke beschermingsmiddelen worden gedragen, zoals handschoenen, een veiligheidsbril en een gasmasker.
| Gevarensymbolen | Xi: Irriterend, F: Licht ontvlambaar |
| Beveiligingsbeschrijving | S16: Verwijderd houden van ontstekingsbronnen – Niet roken, S26: Bij aanraking met de ogen onmiddellijk met veel water afspoelen en een arts raadplegen, S36: Draag geschikte beschermende kleding, S37: Draag geschikte handschoenen, S39: Draag geschikte beschermende kleding. gezichtsbescherming |
| VN-identificatienummers | VN 2319 |
| HS-code | 291439 |
| Gevarenklasse | 3 (Ontvlambare vloeistoffen) |
| Verpakkingsgroep | III |
| Toxiciteit | Methylfenylketon is geclassificeerd als irriterend voor de ogen van categorie 3 en huidirriterend voor categorie 4. Het wordt niet als kankerverwekkend of mutageen beschouwd. De orale LD50 (dodelijke dosis voor 50% van de geteste proefpersonen) bij ratten bedraagt ongeveer 3.000 mg/kg. Het wordt niet als een significant milieurisico beschouwd. |
Methoden voor de synthese van methylfenylketon
Er bestaan verschillende methoden om methylfenylketon te synthetiseren.
Een gebruikelijke methode is de Friedel-Crafts-acylering van benzeen met acetylchloride in aanwezigheid van een Lewis-zuurkatalysator zoals aluminiumchloride. Deze reactie produceert methylfenylketon en waterstofchloride als bijproducten.
Een andere methode is de oxidatie van ethylbenzeen met behulp van lucht of zuurstof in aanwezigheid van een metaalkatalysator zoals kobalt of mangaan. Deze reactie produceert methylfenylketon en azijnzuur als bijproducten.
Methylfenylketon kan worden gesynthetiseerd door fenylaceton te reduceren met behulp van reductiemiddelen zoals natriumboorhydride of lithiumaluminiumhydride. Deze reactie produceert methylfenylketon en de overeenkomstige alcohol als bijproducten.
Een andere methode omvat de reactie van benzoylchloride met ethylbenzeen in aanwezigheid van een aluminiumchloridekatalysator om methylfenylketon en waterstofchloride als bijproducten te produceren.
Gebruik van methylfenylketon
Methylfenylketon heeft verschillende toepassingen in verschillende industrieën.
- Methylfenylketon wordt veel gebruikt als oplosmiddel voor verschillende harsen, cellulose-esters en kunststoffen.
- De voedingsindustrie gebruikt methylfenylketon als smaakstof, vooral voor kersen- en amandelsmaken.
- De parfumindustrie gebruikt methylfenylketon als grondstof voor de productie van parfums en andere geurproducten.
- Verschillende chemicaliën zoals farmaceutische producten, landbouwchemicaliën en kleurstoffen worden gesynthetiseerd met behulp van methylfenylketon.
- Methylfenylketon dient als tussenproduct bij de productie van fenylaceton, een voorloper voor de synthese van amfetaminen.
- Coumarine, een geurstof die wordt gebruikt in zepen en wasmiddelen, wordt gesynthetiseerd uit methylfenylketon.
- Reagentia uit de organische chemie gebruiken methylfenylketon als reagens voor de synthese van verschillende verbindingen.
- Methylfenylketon dient als grondstof voor de productie van andere chemicaliën zoals styreen en methylstyreen.
Over het algemeen heeft methylfenylketon een breed scala aan toepassingen in verschillende industrieën vanwege zijn veelzijdige eigenschappen en toepassingen.
Vragen:
Vraag: Is acetofenon polair?
A: Ja, acetofenon is polair vanwege de aanwezigheid van een carbonylgroep (C=O) en een fenylring, die een dipoolmoment creëert.
Vraag: Zijn benzaldehyde of acetofenon polairder?
A: Benzaldehyde is polairder dan acetofenon omdat het een hoger dipoolmoment heeft vanwege de aanwezigheid van een aldehydegroep (CHO) naast de fenylring.
Vraag: IR-spectrum van acetofenon?
A: Het IR-spectrum van acetofenon vertoont een sterke en brede absorptieband rond 1700 cm^-1, wat kenmerkend is voor de rekvibratie van carbonyl (C=O). Het vertoont ook pieken rond 3000-3100 cm^-1, wat overeenkomt met de rekvibraties van aromatische CH.
Vraag: Van acetofenon naar benzoëzuur?
A: Acetofenon kan worden omgezet in benzoëzuur door oxidatie met behulp van een oxidatiemiddel zoals kaliumpermanganaat of chroomzuur. Deze reactie resulteert in het splitsen van de koolstof-koolstofbinding grenzend aan de carbonylgroep, gevolgd door oxidatie van het resulterende tussenproduct om benzoëzuur te produceren.
Vraag: Van benzeen naar acetofenon?
A: Benzeen kan worden omgezet in acetofenon door middel van Friedel-Crafts-acylering met behulp van acetylchloride of azijnzuuranhydride in aanwezigheid van een Lewis-zuurkatalysator zoals aluminiumchloride. Deze reactie resulteert in de vervanging van een waterstofatoom van benzeen door een acetylgroep (-COCH3), gevolgd door herschikking om acetofenon te vormen.
