Natriumazide (NaN3) is een chemische verbinding. Het is zeer giftig en explosief. Het wordt gebruikt in airbags om snel stikstofgas te genereren dat bij een botsing kan worden opgeblazen.
| IUPAC-naam | Natriumazide |
| Moleculaire formule | NaN3 |
| CAS-nummer | 26628-22-8 |
| Synoniemen | Azium, natriumzout van waterstofzuur, natriumtrinitride |
| InChi | InChI=1S/3HNO.Na/c1-4-2;2-1-3;/h3*1H;/q;;;+1/p-1 |
Eigenschappen van natriumazide
Natriumazide-formule
De formule voor natriumazide is NaN3. Het bestaat uit één natriumatoom (Na) en drie stikstofatomen (N). Het natriumatoom is positief geladen, terwijl de stikstofatomen negatief geladen zijn. De formule vertegenwoordigt de verhouding van natrium- en stikstofatomen in de verbinding.
Natriumazide Molaire Massa
De molaire massa van natriumazide wordt berekend door de atoommassa’s van de bestanddelen ervan op te tellen. Natrium heeft een molmassa van 22,99 g/mol en stikstof een molmassa van 14,01 g/mol. Omdat er drie stikstofatomen in natriumazide zitten, vermenigvuldigen we de molaire massa van stikstof met drie. Optelling van deze waarden geeft een molaire massa van ongeveer 65,01 g/mol voor natriumazide.
Kookpunt van natriumazide
Natriumazide heeft een hoog kookpunt. Bij verhitting ondergaat het ontbinding in plaats van te koken. Bij temperaturen boven 275 graden Celsius (527 graden Fahrenheit) valt het snel uiteen in metallisch natrium- en stikstofgas. Het kookpunt is daarom niet goed gedefinieerd.
Natriumazide Smeltpunt
Het smeltpunt van natriumazide is relatief laag vergeleken met het kookpunt. Het smelt bij ongeveer 275 graden Celsius (527 graden Fahrenheit). Bij deze temperatuur verandert de verbinding van vast naar vloeibaar. Het is echter belangrijk om voorzichtig met natriumazide om te gaan vanwege de toxische en explosieve aard ervan.
Dichtheid van natriumazide g/ml
De dichtheid van natriumazide wordt gewoonlijk uitgedrukt in gram per milliliter (g/ml). De geschatte dichtheid van vast natriumazide is ongeveer 1,85 g/ml. Er moet echter worden opgemerkt dat de dichtheid enigszins kan variëren, afhankelijk van factoren zoals temperatuur en druk.
Natriumazide Molecuulgewicht
Het molecuulgewicht van natriumazide is de som van de atoommassa’s van de samenstellende elementen. Zoals eerder vermeld bestaat natriumazide uit één natriumatoom en drie stikstofatomen. Het optellen van de atoommassa’s van deze elementen geeft een molecuulgewicht van ongeveer 65,01 gram per mol (g/mol).
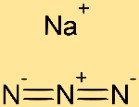
Structuur van natriumazide
De structuur van natriumazide bestaat uit afwisselende natriumkationen (Na+) en azide-anionen (N3-). Het natriumion is omgeven door drie stikstofatomen, die elk een elektronenpaar delen met het natriumatoom. Deze opstelling creëert een stabiele kristalroosterstructuur voor natriumazide.
Oplosbaarheid van natriumazide
Natriumazide is matig oplosbaar in water. Het lost op in water en vormt een heldere oplossing. De oplosbaarheid van natriumazide neemt toe bij hogere temperaturen. Het is echter belangrijk om voorzichtig met de oplossing om te gaan vanwege de toxische en explosieve aard van natriumazide.
| Verschijning | Witte vaste stof |
| Soortelijk gewicht | 1,85 g/ml |
| Kleur | Kleurloos |
| Geur | Geurloos |
| Molaire massa | 65,01 g/mol |
| Dikte | 1,85 g/ml |
| Fusie punt | 275°C |
| Kookpunt | Ontbonden |
| Flitspunt | Niet toepasbaar |
| oplosbaarheid in water | Matig oplosbaar |
| Oplosbaarheid | Oplosbaar in polaire oplosmiddelen zoals ammoniak |
| Dampdruk | Niet toepasbaar |
| Dampdichtheid | Niet toepasbaar |
| pKa | Niet toepasbaar |
| pH | Neutrale |
Veiligheid en gevaren van natriumazide
Natriumazide brengt aanzienlijke veiligheidsrisico’s met zich mee en moet met uiterste voorzichtigheid worden behandeld. Het is zeer giftig als het wordt ingeslikt, ingeademd of via de huid wordt opgenomen. Blootstelling aan natriumazide kan ernstige gezondheidsrisico’s veroorzaken, waaronder ademhalingsproblemen, duizeligheid en zelfs de dood. Het is ook een potentieel explosiegevaar, vooral als het wordt blootgesteld aan hitte, schokken of contact met bepaalde metalen. Bij het werken met natriumazide moeten mensen geschikte persoonlijke beschermingsmiddelen dragen, inclusief handschoenen en een veiligheidsbril. Het is van cruciaal belang om deze verbinding op te slaan en te hanteren in goed geventileerde ruimtes, uit de buurt van ontstekingsbronnen en onverenigbare stoffen, om het risico op ongevallen te minimaliseren en de veiligheid op de werkplek te garanderen.
| Gevarensymbolen | Giftig, explosief |
| Beveiligingsbeschrijving | Ga uiterst voorzichtig te werk. Giftige en explosieve stof. |
| VN-identificatienummers | UN1687 (voor natriumazide, giftige vaste stoffen, anorganisch, neg) |
| HS-code | 28500090 |
| Gevarenklasse | 6.1 (giftige stoffen) |
| Verpakkingsgroep | II (matig gevaarlijke stof) |
| Toxiciteit | Zeer giftig |
Methoden voor de synthese van natriumazide
Er zijn een paar veelgebruikte methoden voor het synthetiseren van natriumazide.
Eén methode omvat de reactie tussen natriumamide (NaNH2) en waterstofzuur (HN3). Bij deze methode lost u natriumamide op in vloeibare ammoniak en voegt u vervolgens langzaam waterstofzuur toe. De reactie vindt plaats, wat resulteert in de vorming van natriumazide en ammoniumchloride als bijproducten.
Een andere synthesemethode omvat de reactie tussen natriumnitriet (NaNO2) en natriumazide (NaN3). In een waterige oplossing controleert de reactie zorgvuldig de toevoeging van natriumnitriet aan een natriumazide-oplossing, wat leidt tot de vorming van natriumazide en natriumnitraat.
Om natriumazide te synthetiseren, kan natriumcyanide (NaCN) bij hoge temperatuur worden gereageerd met lachgas (N2O). Tijdens deze reactie worden natriumazide en natriumcyanaat gevormd als bijproducten.
Volg altijd de juiste veiligheidsmaatregelen om de risico’s die aan het syntheseproces zijn verbonden tot een minimum te beperken. Dit omvat het gebruik van persoonlijke beschermingsmiddelen en het volgen van verwerkingsprotocollen.
Gebruik van natriumazide
Natriumazide heeft verschillende belangrijke toepassingen in verschillende industrieën. Hier zijn enkele opmerkelijke apps:
- Airbagopblazen: Natriumazide is een belangrijk onderdeel van auto-airbags. Tijdens een botsing reageert een kleine hoeveelheid natriumazide snel en genereert stikstofgas, waardoor de airbag wordt opgeblazen en de passagiers worden beschermd.
- Biochemisch onderzoek: Onderzoekers gebruiken natriumazide om enzymen, zoals cytochroomoxidase, te remmen, waardoor de studie van cellulaire processen en metabolische routes wordt vergemakkelijkt.
- Bewaring van biologische monsters: Natriumazide bewaart biologische monsters, zoals antilichamen, door de groei van bacteriën te voorkomen en hun stabiliteit te behouden.
- Explosieve initiatie: Natriumazide dient als primair explosief in sommige pyrotechnische apparaten, ontstekers en explosieve initiatoren vanwege zijn explosieve karakter.
- Chemische synthese: Natriumazide fungeert als een voorloper in verschillende chemische reacties, waardoor de synthese van organische verbindingen, farmaceutische producten en kleurstoffen mogelijk is.
- Corrosiepreventie: Industrieën gebruiken natriumazide als corrosieremmer om metalen oppervlakken te beschermen tegen degradatie veroorzaakt door oxidatie of blootstelling aan corrosieve stoffen.
- Mijnbouw: Natriumazide helpt bij het scheiden van waardevolle mineralen van ongewenste stoffen bij mijnbouwactiviteiten als depressivum bij minerale flotatieprocessen.
- Polymeerindustrie: Natriumazide fungeert als blaasmiddel bij de productie van polyurethaanschuimen en vergemakkelijkt de vorming van gasbellen die het schuim de gewenste structuur geven.
- Analytische chemie: Natriumazide dient als reagens voor verschillende chemische analyses, waaronder spectrofotometrie, gaschromatografie en massaspectrometrie.
- Diergeneeskunde: Dierenartsen gebruiken natriumazide in sommige gevallen als euthanasiemiddel voor dieren in de dierenartspraktijk.
Deze toepassingen benadrukken de diverse toepassingen van natriumazide, maar het is van cruciaal belang om voorzichtig met deze verbinding om te gaan en veiligheidsprotocollen te volgen vanwege de toxische en explosieve aard ervan.
Vragen
Vraag: Hoe testen op natriumazide?
A: Natriumazide kan worden getest met behulp van geschikte analytische technieken zoals spectroscopie, chromatografie of testen van chemische reactiviteit.
Vraag: Wordt natriumazide nog steeds gebruikt in airbags?
A: Ja, natriumazide wordt nog steeds in airbags gebruikt als drijfgas om bij een botsing snel op te blazen.
Vraag: Hoeveel gram natriumazide is nodig om 30,5 g stikstof te produceren?
A: Er is ongeveer 34 gram natriumazide nodig om 30,5 gram stikstofgas te produceren.
Vraag: Waar kan ik natriumazide kopen?
A: Natriumazide kan worden gekocht bij chemische leveranciers, laboratoriumleveranciers of online chemische marktplaatsen.
Vraag: Hoe bereid ik een oplossing van 0,01% natriumazide in PBS?
A: Om een 0,01% natriumazide-oplossing in PBS te bereiden, lost u 0,01 gram natriumazide op in 100 ml fosfaatgebufferde zoutoplossing (PBS).
Vraag: Wat is de rol van natriumazide in de experimenten?
A: Natriumazide wordt vaak gebruikt als remmer of conserveermiddel in experimenten die bedoeld zijn om de enzymactiviteit te remmen of de groei van bacteriën te voorkomen.
Vraag: Hoe verwijder ik natriumazide uit een monster?
A: Natriumazide kan uit een monster worden verwijderd door het grondig te wassen of te spoelen met geschikte oplosmiddelen of door het te onderwerpen aan ontleding bij hoge temperaturen.
Vraag: Welke invloed heeft natriumazide op ETC?
A: Natriumazide remt de elektronentransportketen (ETC) in de mitochondriën door het enzym cytochroomoxidase te blokkeren, waardoor de elektronenstroom en de ATP-productie worden onderbroken.
Vraag: Hoeveel gram natrium wordt gevormd wanneer 93 gram natriumazide reageert?
A: Er wordt 35,9 gram natrium gevormd wanneer 93 gram natriumazide reageert.
Vraag: Is de explosieve ontleding van natriumazide een fysieke verandering in de ontplooiing van de airbag?
A: Nee, de explosieve ontleding van natriumazide om de airbag van een auto op te blazen is een chemische verandering.
Vraag: Hoe natriumazide bereiden?
A: Natriumazide wordt gewoonlijk bereid via chemische synthesemethoden waarbij reacties plaatsvinden tussen geschikte precursors, zoals natriumamide en waterstofzuur.
Vraag: Hoeveel natriumazide is giftig?
A: Natriumazide is zeer giftig en zelfs kleine hoeveelheden, zoals een paar gram, kunnen aanzienlijke gezondheidsrisico’s met zich meebrengen als ze worden ingenomen, ingeademd of via de huid worden opgenomen.
Vraag: Waar wordt natriumazide voor gebruikt?
A: Natriumazide wordt gebruikt in een verscheidenheid aan toepassingen, waaronder het opblazen van airbags, biochemisch onderzoek, chemische synthese en als conserveermiddel of remmer in biologische monsters.
Vraag: Reageert natriumazide met zuren?
A: Ja, natriumazide kan reageren met zuren, zoals zoutzuur (HCl), waardoor giftige gassen ontstaan, zoals waterstofazide (HN3). Er moeten passende voorzorgsmaatregelen worden genomen bij het hanteren van natriumazide en zuren.
