Isobutanol is een kleurloze vloeistof met een sterke geur. Het wordt gebruikt als oplosmiddel, brandstofadditief en bij de productie van verschillende chemicaliën. Het kan irritatie veroorzaken bij inademing of bij contact met de huid.
| IUPAC-naam | 2-methylpropaan-1-ol |
| Moleculaire formule | C4H10O |
| CAS-nummer | 78-83-1 |
| Synoniemen | Isobutylalcohol, 2-methyl-1-propanol, 2-methylpropylalcohol |
| InChi | InChI=1S/C4H10O/c1-4(2)3-5/h4-5H,3H2,1-2H3 |
Eigenschappen van isobutanol
Isobutanol-formule
De formule voor isobutylalcohol is C4H10O. Het bestaat uit vier koolstofatomen, tien waterstofatomen en één zuurstofatoom. Het is een alcoholverbinding die ook bekend staat als 2-methylpropan-1-ol.
Molaire massa van isobutanol
De molaire massa van isobutylalcohol wordt berekend door de atoommassa’s van de samenstellende elementen op te tellen. Voor isobutylalcohol is de molaire massa ongeveer 74,12 gram per mol.
Kookpunt van isobutanol
Isobutylalcohol heeft een kookpunt van ongeveer 107,89 graden Celsius (225,2 graden Fahrenheit). Dit betekent dat isobutylalcohol bij deze temperatuur verandert van een vloeistof in een gas.
Smeltpunt van isobutanol
Het smeltpunt van isobutylalcohol is ongeveer -108 graden Celsius (-162,4 graden Fahrenheit). Dit is de temperatuur waarbij isobutylalcohol verandert van vaste naar vloeibare toestand.
Isobutanol Dichtheid g/ml
Isobutylalcohol heeft een dichtheid van ongeveer 0,806 gram per milliliter. Deze dichtheid geeft de massa isobutylalcohol per volume-eenheid aan en helpt bij het bepalen van het gedrag ervan in verschillende toepassingen.
Isobutanol Moleculair gewicht
Het molecuulgewicht van isobutylalcohol, dat de som is van de atoomgewichten van de samenstellende atomen, is ongeveer 74,12 gram per mol. Het is een belangrijke factor bij verschillende chemische berekeningen en reacties.
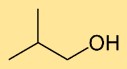
Structuur van isobutanol
De structuur van isobutylalcohol bestaat uit een centraal koolstofatoom gebonden aan drie andere koolstofatomen en een hydroxylgroep (-OH). Het heeft een vertakte structuur waarbij de methylgroep (CH3) aan het tweede koolstofatoom is bevestigd.
Oplosbaarheid van isobutanol
Isobutylalcohol is mengbaar met veel organische oplosmiddelen, waaronder water, ethanol en diethylether. De oplosbaarheid ervan in water is echter relatief laag. De oplosbaarheid van isobutylalcohol hangt af van factoren zoals de temperatuur en de polariteit van het oplosmiddel.
| Eigendom | Waarde |
| Verschijning | Kleurloze vloeistof |
| Soortelijk gewicht | 0,806 |
| Kleur | N.v.t |
| Geur | sterk |
| Molaire massa | 74,12 g/mol |
| Dikte | 0,806 g/ml |
| Fusie punt | -108°C |
| Kookpunt | 107,89°C |
| Flitspunt | 35°C |
| oplosbaarheid in water | Mengbaar |
| Oplosbaarheid | Mengbaar met organische oplosmiddelen, waaronder water, ethanol en diethylether |
| Dampdruk | 7,49 mmHg bij 25°C |
| Dampdichtheid | 2,55 (lucht = 1) |
| pKa | 16:18 uur |
| pH | 7 (neutraal) |
Veiligheid en gevaren van isobutanol
Isobutylalcohol brengt enkele veiligheidsrisico’s met zich mee waarmee rekening moet worden gehouden. Het kan irritatie veroorzaken bij inademing, inslikken of bij contact met de huid of ogen. Bij het hanteren van deze chemische stof moeten adequate ventilatie en persoonlijke beschermingsmiddelen worden gebruikt. Isobutylalcohol is brandbaar en kan explosieve damp-luchtmengsels vormen. Het vlampunt is laag, namelijk 35 graden Celsius, waardoor het een potentieel brandgevaar oplevert. Er moeten voorzorgsmaatregelen worden genomen om ontstekingsbronnen te vermijden. In geval van accidentele lozing moeten passende insluitings- en schoonmaakprocedures worden gevolgd. Het is belangrijk om de veiligheidsinformatiebladen te raadplegen en de juiste veiligheidsprotocollen te volgen bij het werken met isobutylalcohol.
| Gevarensymbolen | Ontvlambaar, irriterend |
| Beveiligingsbeschrijving | Verwijderd houden van ontstekingsbronnen. Gebruik in een goed geventileerde ruimte. Vermijd direct contact met huid en ogen. |
| VN-identificatienummers | VN 1212 |
| HS-code | 2905.13.00 |
| Gevarenklasse | Klasse 3 – Ontvlambare vloeistoffen |
| Verpakkingsgroep | GE II |
| Toxiciteit | Kan irritatie veroorzaken. Kan schadelijk zijn bij inslikken. |
Methoden voor de synthese van isobutanol
Er zijn verschillende methoden voor het synthetiseren van isobutylalcohol. Een gebruikelijke methode is het katalytisch hydrogeneren van isobutyraldehyde door het te mengen met waterstofgas in aanwezigheid van een metaalkatalysator, zoals nikkel of platina. De katalysator vergemakkelijkt de omzetting van isobutyraldehyde in isobutylalcohol.
Een andere methode omvat de hydroformylering van propyleen , waarbij het propyleen reageert met koolmonoxide en waterstofgas met behulp van een katalysator, meestal een op rhodium gebaseerd complex. Bij deze reactie ontstaat isobutyraldehyde, dat vervolgens verder kan worden gehydrogeneerd om isobutylalcohol op te leveren.
Het biomassafermentatieproces maakt de productie van isobutylalcohol mogelijk. Sommige micro-organismen, waaronder bacteriën en gisten, kunnen suikers of andere koolstofbronnen metaboliseren en als bijproduct isobutylalcohol produceren. Deze biogebaseerde methode biedt een hernieuwbare en duurzame benadering van de productie van isobutylalcohol.
Indirecte hydratatie van isobuteen is een methode die wordt gebruikt om isobutylalcohol te synthetiseren. Dit omvat de reactie van isobuteen met zwavelzuur om tert-butylalcohol (TBA) te vormen, die vervolgens dehydratatie kan ondergaan om isobutylalcohol te genereren.
Elk van deze methoden heeft zijn voordelen en overwegingen in termen van kosten, effectiviteit en impact op het milieu. De keuze van de synthesemethode hangt af van factoren zoals de gewenste zuiverheid van de isobutylalcohol, beschikbaarheid van grondstoffen en specifieke industriële eisen.
Gebruik van isobutanol
Isobutylalcohol vindt toepassingen in verschillende industrieën vanwege zijn veelzijdige eigenschappen. Hier zijn enkele veelvoorkomende toepassingen van isobutylalcohol:
Oplosmiddel: Isobutylalcohol lost en verspreidt actief andere stoffen, waardoor de toepassing en prestaties ervan in verschillende toepassingen zoals verven, coatings en harsen worden verbeterd.
Brandstofadditief: Isobutylalcohol verbetert actief het octaangetal en verbetert de verbrandingsefficiëntie van benzine wanneer het als brandstofadditief wordt gemengd. Het dient actief als een hernieuwbaar alternatief voor conventionele benzine-additieven.
Chemisch tussenproduct: Isobutylalcohol speelt actief een sleutelrol als tussenproduct bij de productie van verschillende chemicaliën. Het is actief betrokken bij de productie van esters, weekmakers, herbiciden en farmaceutische producten.
Extractiemiddel: Isobutylalcohol extraheert en concentreert actief smaakstoffen en dient als extractiemiddel bij de productie van natuurlijke en synthetische smaak- en geurstoffen.
Drukinkten: Isobutylalcohol draagt actief bij aan het oplossen van pigmenten en het verbeteren van de inktstroom bij de formulering van drukinkten, vooral bij flexografische en diepdrukprocessen.
Producten voor persoonlijke verzorging: Isobutylalcohol werkt actief als oplosmiddel voor geuringrediënten in de formulering van producten voor persoonlijke verzorging, zoals parfums, eau de colognes en lotions. Het draagt actief bij aan het verkrijgen van de gewenste reukprofielen.
Geneesmiddelen: Isobutylalcohol dient actief als oplosmiddel of reactiemedium in farmaceutische productieprocessen, waardoor de synthese en formulering van verschillende geneesmiddelen mogelijk is.
Deze uiteenlopende toepassingen benadrukken het belang van isobutylalcohol in meerdere industrieën, waardoor het een waardevolle verbinding is met een breed scala aan toepassingen.
Vragen:
Vraag: Wat is isobutanol?
A: Isobutylalcohol is een kleurloze vloeibare alcohol met een sterke geur, die vaak wordt gebruikt als oplosmiddel, brandstofadditief en chemisch tussenproduct in verschillende industrieën.
Vraag: Is isobutanol oplosbaar in water?
A: Isobutylalcohol is gedeeltelijk oplosbaar in water, met beperkte mengbaarheid vanwege zijn hydrofobe karakter.
Vraag: Bij welke chemische verschuivingen (ppm) verwachten we de vier isobutanolpieken waar te nemen?
A: De vier isobutylalcoholpieken worden doorgaans waargenomen bij chemische verschuivingen van ongeveer 0,9 ppm (singlet), 1,1 tot 1,3 ppm (kwartet), 1,6 tot 1,8 ppm (multiplet) en 3,7 tot 4,0 ppm (multiple).
Vraag: Hoe kan ik isobutanol produceren?
A: Isobutylalcohol kan op verschillende manieren worden geproduceerd, waaronder katalytische hydrogenering van isobutyraldehyde, hydroformylering van propyleen, fermentatie van biomassa of indirecte hydratatie van isobuteen.
Vraag: Waar wordt isobutanol in gebruikt?
A: Isobutylalcohol wordt gebruikt als oplosmiddel, brandstofadditief, chemisch tussenproduct, extractiemiddel, drukinktcomponent en in producten voor persoonlijke verzorging en farmaceutische producten.
Vraag: Hoe oplosbaar is isobutanol?
A: Isobutylalcohol heeft een matige oplosbaarheid in water, maar is zeer oplosbaar in organische oplosmiddelen zoals ethanol en diethylether.
Vraag: Is isobutanol een peroxide?
A: Nee, isobutylalcohol wordt niet als een peroxidemiddel beschouwd, in tegenstelling tot sommige andere organische verbindingen die bij blootstelling aan lucht en licht explosieve peroxiden kunnen vormen.
Vraag: Welk voordeel heeft de directe productie van isobutanol door kunstmatige cyanobacteriën ten opzichte van andere alternatieve biobrandstoffen?
A: De directe productie van isobutylalcohol door kunstmatige cyanobacteriën biedt voordelen zoals een hoge opbrengst, koolstofneutraliteit en het potentieel om hernieuwbare en duurzame biobrandstoffen te produceren.
