Decaan (C10H22) is een koolwaterstofverbinding die tien koolstofatomen bevat, gerangschikt in een rechte keten. Het wordt vaak gebruikt als oplosmiddel in verschillende industriële toepassingen, zoals reinigings- en productieprocessen.
| IUPAC-naam | Decaan |
| Moleculaire formule | C10H22 |
| CAS-nummer | 124-18-5 |
| Synoniemen | n-Decaan, Decylhydride, n-Amylmethine, Capdecaan |
| InChi | InChI=1S/C10H22/c1-3-5-7-9-10-8-6-4-2/h3-10H2,1-2H3 |
Eigenschappen van decaan
Decaan-formule
De formule voor decaan is C10H22. Het vertegenwoordigt een koolwaterstofverbinding bestaande uit tien koolstofatomen en tweeëntwintig waterstofatomen. De formule toont het exacte aantal en type atomen dat aanwezig is in een decaanmolecuul.
Decaan molaire massa
De molaire massa van decylhydride kan worden berekend door de atoommassa’s van de samenstellende elementen bij elkaar op te tellen. De molaire massa van koolstof (C) is 12,01 g/mol en de molaire massa van waterstof (H) is 1,008 g/mol. Daarom is de molaire massa van decylhydride ongeveer 142,28 g/mol.
Kookpunt van decaan
Decaan heeft een kookpunt van ongeveer 174°C (345°F). Dit betekent dat decylhydride bij normale atmosferische druk begint te verdampen en bij die temperatuur in een gasvormige toestand overgaat. Kookpunt is een belangrijk kenmerk van decylhydride en wordt gebruikt om de fysische eigenschappen en toepassingen ervan te bepalen.
Decaan smeltpunt
Het smeltpunt van decylhydride is ongeveer -29°C (-20°F). Dit betekent de temperatuur waarbij decylhydride verandert van zijn vaste toestand naar zijn vloeibare toestand. Door dit lage smeltpunt is decylhydride onder normale omstandigheden gemakkelijk vloeibaar te maken.
Dichtheid van decaan g/ml
Decylhydride heeft een dichtheid van ongeveer 0,73 g/ml. Dichtheid is de maat voor de massa per volume-eenheid. De dichtheid van decylhydride geeft de relatieve zwaarte of lichtheid aan in vergelijking met een gelijk volume water. De lage dichtheid van decylhydride suggereert dat het lichter is dan water.
Decaan molecuulgewicht
Het molecuulgewicht van decylhydride is ongeveer 142,28 g/mol. Het wordt berekend door de atoomgewichten van alle atomen in een decylhydridemolecuul op te tellen. Het molecuulgewicht levert waardevolle informatie op over de grootte en massa van het decylhydridemolecuul.
Structuur van decaan
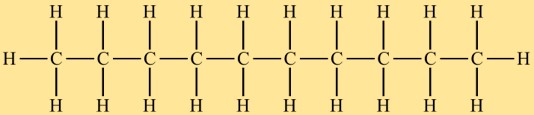
Decylhydride heeft een rechte ketenstructuur, met tien koolstofatomen die in een lineaire opstelling met elkaar zijn verbonden. Elk koolstofatoom vormt vier enkele covalente bindingen met omringende waterstofatomen. De koolstofketen van decylhydride is onvertakt en dit structurele kenmerk beïnvloedt de chemische en fysische eigenschappen ervan.
Oplosbaarheid van decaan
Decylhydride is onoplosbaar in water, maar oplosbaar in niet-polaire oplosmiddelen zoals benzeen, ether en hexaan. Zijn niet-polaire karakter belemmert de interactie met polaire stoffen zoals water. De oplosbaarheid van decylhydride is een belangrijke overweging bij verschillende industriële processen en toepassingen, vooral als het gaat om niet-polaire oplosmiddelen.
| Verschijning | Kleurloze vloeistof |
| Soortelijk gewicht | 0,73 |
| Kleur | Kleurloos |
| Geur | Geurloos |
| Molaire massa | 142,28 g/mol |
| Dikte | 0,73 g/ml |
| Fusie punt | -29°C (-20°F) |
| Kookpunt | 174°C (345°F) |
| Flitspunt | 43°C (109°F) |
| oplosbaarheid in water | Onoplosbaar |
| Oplosbaarheid | Oplosbaar in niet-polaire oplosmiddelen zoals benzeen, ether en hexaan |
| Dampdruk | 1,22 mmHg bij 20°C |
| Dampdichtheid | 4,88 (lucht = 1) |
| pKa | Niet toepasbaar |
| pH | Neutrale |
Veiligheid en gevaren van Decane
Decylhydride kent bepaalde veiligheidsoverwegingen en gevaren. Het is brandbaar en moet met voorzichtigheid worden behandeld, omdat het kan ontbranden bij blootstelling aan open vuur of vonken. Decylhydridedamp is zwaarder dan lucht, wat betekent dat het zich over de grond kan verplaatsen en zich kan ophopen in laaggelegen gebieden, wat een potentieel brand- of explosiegevaar met zich meebrengt. Direct contact met decylhydride kan huidirritatie veroorzaken en kan ook oogirritatie veroorzaken. Het is belangrijk om de juiste beschermende maatregelen te nemen, zoals handschoenen en een veiligheidsbril, wanneer u met decylhydride werkt. Adequate ventilatie is van cruciaal belang om de concentratie van decylhydridedampen in besloten ruimtes tot een minimum te beperken.
| Gevarensymbolen | Brandbaar |
| Beveiligingsbeschrijving | – Verwijderd houden van open vuur. – Gebruiken in goed geventileerde ruimtes – Draag handschoenen en een veiligheidsbril. – Vermijd direct contact met de huid en ogen |
| Identificatiegegevens van de Verenigde Naties | VN 2247 |
| HS-code | 2901.10.00 |
| Gevarenklasse | Klasse 3 (ontvlambare vloeistof) |
| Verpakkingsgroep | GE II |
| Toxiciteit | Lage toxiciteit |
Decaansynthesemethoden
Er zijn verschillende methoden voor het synthetiseren van decylhydride.
- Een gebruikelijke methode voor het synthetiseren van decylhydride is het laten reageren van deceen met waterstofgas in aanwezigheid van een geschikte katalysator, zoals palladium of nikkel. Dit proces verzadigt de dubbele koolstof-koolstofbindingen van deceen en zet het om in decylhydride.
- Een andere methode is ethyleenoligomerisatie , waarbij katalysatoren, meestal overgangsmetaalcomplexen, ethyleenmoleculen combineren om koolwaterstoffen met een hoger molecuulgewicht te vormen, waaronder decylhydride.
- Petroleumraffinageprocessen produceren ook decylhydride. Bij dit proces wordt door destillatie van ruwe olie een fractie die decylhydride en soortgelijke koolwaterstoffen bevat afgescheiden en gezuiverd, waardoor zuiver decylhydride wordt verkregen.
- Het Fischer-Tropsch-proces maakt de synthese van decylhydride mogelijk door koolmonoxide en waterstof te laten reageren via een katalysator, gewoonlijk een ijzer- of kobaltkatalysator, onder omstandigheden van hoge temperatuur en druk. Dit proces resulteert in een mengsel van koolwaterstoffen, waaronder decylhydride.
Het is van cruciaal belang om te benadrukken dat deze synthesemethoden op industriële schaal gespecialiseerde apparatuur en expertise vereisen. De keuze van de synthesemethode hangt af van factoren zoals de beschikbaarheid van grondstoffen, de gewenste zuiverheid en economische overwegingen.
Gebruik van decaan
Decylhydride vindt vanwege zijn eigenschappen en kenmerken verschillende toepassingen in verschillende industrieën. Enkele veel voorkomende toepassingen van decylhydride zijn:
- Oplosmiddel: Decylhydride wordt gebruikt als oplosmiddel in industriële processen, zoals reinigings- en ontvettingstoepassingen. Het vermogen om verschillende niet-polaire stoffen op te lossen maakt het nuttig bij deze processen.
- Brandstof: Dieselbrandstof bevat decylhydride als component en gebruikt dit als referentieverbinding om de cetaanindex te meten, die de ontstekingskwaliteit van dieselbrandstoffen evalueert. Het draagt bij aan de verbrandingseigenschappen van dieselbrandstof.
- Chemisch tussenproduct: Decylhydride dient als bouwsteen voor de productie van andere chemicaliën. Decylhydride dient als grondstof voor de synthese van verschillende verbindingen, waaronder oppervlakteactieve stoffen, smeermiddelen en polymeren.
- Extractiemiddel: De farmaceutische en voedingsindustrie gebruiken decylhydride als extractiemiddel. Het helpt bij het scheiden en zuiveren van bepaalde verbindingen en aroma’s uit grondstoffen.
- Onderzoek en laboratoriumtoepassingen: Wetenschappelijk onderzoek en laboratoria gebruiken decylhydride. Het dient als referentieverbinding bij gaschromatografie en als standaard voor kalibratiedoeleinden.
- Cosmetische formuleringen: Cosmetische producten en producten voor persoonlijke verzorging bevatten decylhydride in hun formuleringen. Het werkt als conditioneringsmiddel, verzachtend middel en viscositeitsregelaar in verschillende huid- en haarverzorgingsproducten.
- Industriële smeermiddelen: Industriële toepassingen profiteren van de lage vluchtigheid en goede smering van decylhydride, door het als smeermiddel te gebruiken. Het vermindert wrijving en slijtage tussen bewegende delen.
- Kalibratiestandaarden: Analytische chemie gebruikt decylhydride als kalibratiestandaard. Het helpt bij de kalibratie en validatie van analytische instrumenten en technieken.
Over het geheel genomen maken de veelzijdige eigenschappen van decylhydride het waardevol in verschillende industrieën, variërend van productie tot onderzoek en ontwikkeling.
Vragen:
Vraag: Wat is een decaan?
A: Decylhydride is een koolwaterstof met de molecuulformule C10H22, bestaande uit tien koolstofatomen en tweeëntwintig waterstofatomen.
Vraag: Hoeveel equivalenten waterstofgas zijn nodig om 1-decyne te reduceren tot decaan?
A: Voor de reductie van 1-decyne tot decylhydride zijn twee equivalenten waterstofgas nodig.
Vraag: Is decaan polair?
A: Nee, decylhydride is niet-polair omdat het bestaat uit koolstof- en waterstofatomen die met elkaar zijn verbonden door niet-polaire covalente bindingen.
Vraag: Is jodium oplosbaar in C10H22?
A: Ja, jodium is oplosbaar in C10H22 (decylhydride) omdat de twee stoffen niet-polair zijn en zich kunnen vermengen.
Vraag: Welke van de volgende stoffen heeft de hoogste viscositeit? (a) C4H10 (b) C8H18 (c) C10H22
A: C10H22 (decylhydride) zou de hoogste viscositeit hebben van de gegeven stoffen vanwege de grotere molecuulgrootte en langere koolstofketen.
Vraag: Bereken het vriespunt van 23,0 g decaan (C10H22) in 53,0 g CHCl3.
A: Voor het berekenen van het vriespunt is aanvullende informatie nodig, zoals de vriespuntsdalingconstante voor het oplosmiddel (CHCl3) en de molfracties van de componenten om de vriespuntsdaling te bepalen.
