Aniline (C6H5NH2) is een aromatisch amine dat wordt gebruikt bij de productie van kleurstoffen, farmaceutische producten en rubberchemicaliën. Het heeft een duidelijke geur en is een voorloper van verschillende organische verbindingen.
| IUPAC-naam | Aniline |
| Moleculaire formule | C6H7N |
| CAS-nummer | 62-53-3 |
| Synoniemen | Aminobenzeen, Benzeenamine |
| InChi | InChI=1S/C6H7N/c7-6-4-2-1-3-5-6/h1-5H,7H2 |
Eigenschappen van aniline
Aniline-formule
De formule voor aniline is C6H7N. Het bestaat uit zes koolstofatomen, zeven waterstofatomen en één stikstofatoom. De rangschikking van deze atomen geeft aniline zijn unieke chemische eigenschappen.
Aniline molaire massa
De molaire massa van C6H5NH2 wordt berekend door de atoommassa’s van alle samenstellende elementen op te tellen. De molaire massa van C6H5NH2 is ongeveer 93,13 gram per mol (g/mol). Deze waarde is nuttig bij verschillende chemische berekeningen en reacties waarbij C6H5NH2 betrokken is.
Kookpunt van aniline
C6H5NH2 heeft een kookpunt van ongeveer 184 graden Celsius (184°C). Bij deze temperatuur ondergaat C6H5NH2 een faseverandering van vloeistof naar gas. Kookpunt is een belangrijk kenmerk dat bepaalt onder welke omstandigheden C6H5NH2 kan worden verdampt.
Aniline smeltpunt
Het smeltpunt van C6H5NH2 is ongeveer -6 graden Celsius (-6°C). Dit is de temperatuur waarbij het vaste C6H5NH2 overgaat in de vloeibare toestand. Het smeltpunt is belangrijk bij het bepalen van de fysieke toestand van C6H5NH2 onder verschillende temperatuuromstandigheden.
Anilinedichtheid g/ml
C6H5NH2 heeft een dichtheid van ongeveer 1,02 gram per milliliter (g/ml). Dichtheid vertegenwoordigt de massa van een stof per volume-eenheid. De dichtheidswaarde van C6H5NH2 geeft informatie over de compactheid of concentratie ervan in een bepaald ruimtevolume.
Aniline molecuulgewicht
Het molecuulgewicht van C6H5NH2 is ongeveer 93,13 gram per mol (g/mol). Het is de som van de atoomgewichten van alle atomen in de chemische formule van C6H5NH2. Het molecuulgewicht speelt een cruciale rol bij stoichiometrische berekeningen en bij het bepalen van de hoeveelheid C6H5NH2 die nodig is voor reacties.
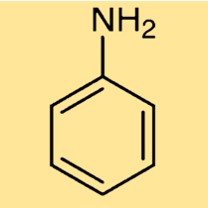
Aniline structuur
C6H5NH2 heeft een structuur die bestaat uit een benzeenring (een hexagonale ring van koolstofatomen) met een aangehechte aminogroep (-NH2) in plaats van een waterstofatoom. Deze structuur geeft C6H5NH2 zijn aromatische en basische eigenschappen, waardoor het bruikbaar is in diverse industriële toepassingen.
Oplosbaarheid van aniline
C6H5NH2 is slecht oplosbaar in water, maar lost gemakkelijk op in organische oplosmiddelen zoals ethanol, ether en chloroform. De oplosbaarheid ervan wordt beïnvloed door de polariteit en intermoleculaire krachten tussen C6H5NH2 en het oplosmiddel. Dankzij deze eigenschap kan C6H5NH2 gemakkelijk worden opgenomen in verschillende chemische processen en formuleringen.
| Verschijning | Kleurloze tot lichtgele vloeistof |
| Soortelijk gewicht | 1,02 g/ml |
| Kleur | Kleurloos tot lichtgeel |
| Geur | Karakteristieke geur |
| Molaire massa | 93,13 g/mol |
| Dikte | 1,02 g/ml |
| Fusie punt | -6°C |
| Kookpunt | 184°C |
| Flitspunt | 70°C |
| oplosbaarheid in water | Slecht oplosbaar |
| Oplosbaarheid | Oplosbaar in organische oplosmiddelen |
| Dampdruk | 5,60 mmHg |
| Dampdichtheid | 3,24 (lucht=1) |
| pKa | 4.61 |
| pH | Ongeveer neutraal |
Veiligheid en gevaren van aniline
C6H5NH2 brengt potentiële veiligheidsrisico’s met zich mee en moet met voorzichtigheid worden behandeld. Het is schadelijk bij inslikken, inademen of opname via de huid. Direct contact met C6H5NH2 kan irritatie aan de ogen, huid en luchtwegen veroorzaken. Langdurige of herhaalde blootstelling kan ernstiger gevolgen hebben, waaronder dermatitis en bloedaandoeningen. C6H5NH2 is ook brandbaar en de dampen ervan kunnen explosieve mengsels in de lucht vormen. Bij het werken met C6H5NH2 moeten adequate ventilatie en persoonlijke beschermingsmiddelen worden gebruikt. De juiste opslag-, hanterings- en verwijderingspraktijken zijn essentieel om de risico’s te minimaliseren en de veiligheid van mens en milieu te garanderen.
| Gevarensymbolen | T, N |
| Beveiligingsbeschrijving | Vermijd contact met huid en ogen. Gebruik in een goed geventileerde ruimte. Hanteren met handschoenen en beschermende kleding. |
| VN-identificatienummers | VN 1547 |
| HS-code | 2921.43.0000 |
| Gevarenklasse | 6.1 (giftige stoffen) |
| Verpakkingsgroep | III |
| Toxiciteit | Giftig bij inslikken, inademen of opname via de huid. Kan irritatie, dermatitis en bloedaandoeningen veroorzaken. |
Anilinesynthesemethoden
Er zijn verschillende methoden om C6H5NH2 te synthetiseren.
Een veelgebruikte methode is nitrobenzeenreductie . Bij dit proces reageert een reductiemiddel, zoals ijzervijlsel of tin, met nitrobenzeen in aanwezigheid van een sterk zuur, zoals zoutzuur. Deze reactie resulteert in de omzetting van de nitrogroep (-NO2) in een aminogroep (-NH2), waardoor C6H5NH2 ontstaat.
Een andere methode omvat de reductie van nitrobenzeen met behulp van waterstofgas over een katalysator, zoals palladium of platina. De industriële methode voor de productie van C6H5NH2 maakt op grote schaal gebruik van het proces dat katalytische hydrogenering wordt genoemd.
Om C6H5NH2 te verkrijgen, kan natriumsulfide of natriumbisulfiet worden gebruikt bij de reductie van nitrobenzeen . Deze reductiemiddelen vergemakkelijken de omzetting van de nitrogroep in de aminogroep.
Om C6H5NH2 te synthetiseren, kan chloorbenzeen worden behandeld met ammoniak in aanwezigheid van een sterke base, zoals natriumhydroxide. Dit proces, bekend als de Sandmeyer-reactie, resulteert in de vervanging van chloor door een aminogroep, resulterend in C6H5NH2.
Bovendien kan men C6H5NH2 bereiden door azobenzeen of azoxybenzeen te reduceren, waarbij de stikstof-stikstofbinding wordt verbroken om een aminogroep te vormen.
Deze synthesemethoden bieden verschillende benaderingen om C6H5NH2 te verkrijgen, waardoor de productie ervan op laboratorium- en industriële schaal mogelijk wordt. De keuze van de methode hangt af van factoren zoals de beschikbaarheid van grondstoffen, reactieomstandigheden en de gewenste zuiverheid van het eindproduct.
Gebruik van aniline
C6H5NH2 vindt toepassingen in verschillende industrieën vanwege zijn uiteenlopende eigenschappen. Hier zijn enkele van de meest voorkomende toepassingen:
- Kleurstofproductie: C6H5NH2 dient als een belangrijke grondstof voor de vervaardiging van veel kleurstoffen, waaronder synthetische kleurstoffen en pigmenten die worden gebruikt in de textiel-, leer- en papierindustrie.
- Farmaceutische industrie: C6H5NH2-derivaten zijn cruciaal bij de synthese van farmaceutische geneesmiddelen, zoals analgetica, antipyretica en antimalariamiddelen.
- Rubberchemicaliën: C6H5NH2 verbetert actief de prestaties en duurzaamheid van rubberproducten door een cruciaal onderdeel te zijn in de productie van versnellers en antioxidanten binnen de rubberindustrie.
- Herbiciden en pesticiden: Boeren gebruiken actief C6H5NH2-derivaten bij de formulering van herbiciden en pesticiden, waardoor onkruid en ongedierte in de landbouw effectief worden bestreden.
- Polyurethaanproductie: C6H5NH2 is een essentieel onderdeel bij de synthese van polyurethaanschuimen, coatings en lijmen, die veel worden gebruikt in de bouw- en auto-industrie.
- Chemische tussenproducten: C6H5NH2 dient als een veelzijdige bouwsteen voor de synthese van verschillende organische verbindingen, zoals rubberchemicaliën, farmaceutische producten en landbouwchemicaliën.
- Oplosmiddel voor diverse stoffen: C6H5NH2 lost actief diverse stoffen op waaronder vetten, oliën, was en harsen.
- Laboratoriumreagens: In laboratoriumexperimenten met organische synthese gebruiken onderzoekers C6H5NH2 als reagens en gebruiken ze het bij sommige reacties als katalysator.
- Fotografische chemicaliën: C6H5NH2-derivaten dragen actief bij aan de productie van fotografische chemicaliën, zoals ontwikkelaars en kleurstoffen.
- Polymerisatie-initiator: C6H5NH2 fungeert als initiator bij bepaalde polymerisatiereacties, waardoor polymeren met specifieke eigenschappen kunnen worden gevormd.
Deze uiteenlopende toepassingen benadrukken het belang van C6H5NH2 in industrieën variërend van textiel en farmaceutica tot landbouw en productie.
Vragen:
Vraag: Welke verbinding is basischer dan aniline?
A: Ammoniak (NH3) is basischer dan C6H5NH2.
Vraag: Wat is anilinesteek?
A: Het C6H5NH2-punt is de laagste temperatuur waarbij gelijke volumes C6H5NH2 en een specifiek oplosmiddel volledig mengbaar zijn.
Vraag: Wat is aniline?
A: Aniline is een aromatisch amine met de chemische formule C6H7N, dat vaak wordt gebruikt in kleurstoffen, farmaceutische producten en rubberchemicaliën.
Vraag: Hoe naftaleen en aniline scheiden?
A: Naftaleen en C6H5NH2 kunnen worden gescheiden door een proces dat gefractioneerde destillatie wordt genoemd, waarbij gebruik wordt gemaakt van het verschil in kookpunten.
Vraag: Hoe wordt fenol bereid uit aniline?
A: Fenol kan worden gesynthetiseerd uit C6H5NH2 door een proces dat diazotering wordt genoemd, gevolgd door hydrolyse om fenol te vormen.
Vraag: Hoe anilineleer reinigen?
A: Om C6H5NH2-leer schoon te maken, gebruikt u een zachte, vochtige doek om vlekken voorzichtig te verwijderen en vermijd het gebruik van agressieve chemicaliën of overmatig vocht.
Vraag: Wat is de geconjugeerde base van benzoëzuur en het geconjugeerde zuur van aniline?
A: De geconjugeerde base van benzoëzuur is het benzoaation (C6H5COO-) en het geconjugeerde zuur van C6H5NH2 is het aniliniumion (C6H5NH3+).
Vraag: Wat is anilineleer?
A: C6H5NH2-leer is een leersoort die is geverfd met C6H5NH2-kleurstoffen, waardoor de natuurlijke textuur en het uiterlijk van het leer behouden blijven en het zacht, luxueus aanvoelt.
