Heptaan is een kleurloze, brandbare vloeistof die gewoonlijk als oplosmiddel wordt gebruikt. Het heeft de molecuulformule C7H16 en wordt aangetroffen in benzine. Heptaan heeft zeven koolstofatomen en 16 waterstofatomen.
| IUPAC-naam | Heptaan |
| Moleculaire formule | C7H16 |
| CAS-nummer | 142-82-5 |
| Synoniemen | n-heptaan, dipropylmethaan, heptylhydride, enz. |
| InChi | InChI=1S/C7H16/c1-3-5-7-6-4-2/h3-7H2.1-2H3 |
Eigenschappen van heptaan
Heptaan-formule
De chemische formule voor heptaan is C7H16. Het bestaat uit zeven koolstofatomen en zestien waterstofatomen, gerangschikt in een rechte keten. De rechte ketenstructuur van heptaan maakt het tot een belangrijk lid van de alkaanfamilie van koolwaterstoffen.
Heptaan molaire massa
De molaire massa van C7H16 is 100,20 g/mol. Deze waarde wordt berekend door de atoommassa’s van alle atomen die aanwezig zijn in een enkel C7H16-molecuul op te tellen. De molaire massa van C7H16 is een belangrijke parameter in veel chemische berekeningen, waaronder stoichiometrie, thermodynamica en kinetiek.
Kookpunt van heptaan
C7H16 heeft een kookpunt van 98,42°C (209,16°F). Dit relatief lage kookpunt maakt het een nuttig oplosmiddel voor een verscheidenheid aan toepassingen, zoals in het laboratorium en bij de benzineproductie. Het kookpunt van C7H16 wordt beïnvloed door verschillende factoren, waaronder de sterkte van intermoleculaire krachten en het molecuulgewicht van de verbinding.
Heptaan Smeltpunt
Het smeltpunt van C7H16 is -91°C (-132°F). Dit lage smeltpunt geeft aan dat C7H16 bij kamertemperatuur vloeibaar is en zeer vluchtig. Het lage smeltpunt van C7H16 is te wijten aan zwakke Van der Waals-krachten tussen de moleculen.
Heptaandichtheid g/ml
De dichtheid van C7H16 is 0,684 g/ml bij 20°C (68°F). De dichtheid van C7H16 is een maatstaf voor de hoeveelheid massa die in een bepaald volume aanwezig is. Deze waarde wordt beïnvloed door factoren zoals temperatuur, druk en zuiverheid van het monster.
Moleculair gewicht van heptaan
Het molecuulgewicht van C7H16 is 100,20 g/mol. Deze waarde wordt berekend door de atoommassa’s van alle atomen die aanwezig zijn in een enkel C7H16-molecuul op te tellen. Het molecuulgewicht van C7H16 is een cruciale parameter bij veel chemische reacties, omdat het helpt bij het bepalen van de hoeveelheid reactanten en producten die in een reactiemengsel aanwezig zijn.
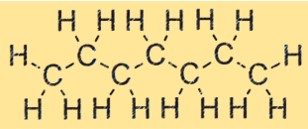
Structuur van heptaan
C7H16 heeft een rechte ketenstructuur, met zeven koolstofatomen en 16 waterstofatomen die lineair zijn gerangschikt. Deze structuur is kenmerkend voor alkanen, een familie van koolwaterstoffen. De structuur van C7H16 beïnvloedt de fysische en chemische eigenschappen ervan, inclusief het kookpunt, smeltpunt en reactiviteit.
Oplosbaarheid van heptaan
C7H16 is een niet-polair molecuul en slecht oplosbaar in polaire oplosmiddelen zoals water. C7H16 is echter zeer oplosbaar in niet-polaire oplosmiddelen zoals hexaan, benzeen en tolueen. Dit oplosbaarheidsgedrag komt doordat like oplost: niet-polaire moleculen hebben de neiging op te lossen in niet-polaire oplosmiddelen, terwijl polaire moleculen de neiging hebben op te lossen in polaire oplosmiddelen.
| Verschijning | Kleurloze vloeistof |
| Specifieke dichtheid bij 25°C | 0,684 g/ml |
| Kleur | Kleurloos |
| Geur | Geur van benzine |
| Molaire massa | 100,20 g/mol |
| Dichtheid bij 25°C | 0,684 g/ml |
| Fusie punt | -91°C (-132°F) |
| Kookpunt | 98,42°C (209,16°F) |
| Flitspunt | -4°C (25°F) |
| Oplosbaarheid in water bij 25°C | 0,004 g/100 ml |
| Oplosbaarheid in andere oplosmiddelen | Zeer oplosbaar in niet-polaire oplosmiddelen (hexaan, tolueen, benzeen) |
| Dampspanning bij 20°C | 25,31 mmHg |
| Dampdichtheid bij 20°C | 3,46 (lucht = 1) |
| pKa | 50 (geschat) |
| pH | Niet toepasbaar |
Heptaanveiligheid en gevaren
C7H16 brengt verschillende veiligheidsrisico’s met zich mee, voornamelijk vanwege de licht ontvlambare aard ervan. Het kan gemakkelijk vlam vatten en ontvlambare dampen vrijgeven bij blootstelling aan hitte of vlammen. C7H16-dampen kunnen ook de ogen, de huid en het ademhalingssysteem irriteren, waardoor hoesten, piepende ademhaling en kortademigheid ontstaan. Bovendien kan C7H16 schadelijk zijn bij inslikken en misselijkheid, braken en buikpijn veroorzaken. Daarom moeten passende voorzorgsmaatregelen worden genomen bij de omgang met C7H16, zoals het gebruik van geschikte beschermende uitrusting, het zorgen voor goede ventilatie in de werkruimte en het uit de buurt houden van warmtebronnen en open vuur. Het is ook essentieel om de juiste protocollen voor opslag, verwerking en verwijdering van C7H16 te volgen om mogelijke risico’s tot een minimum te beperken.
| Gevarensymbolen | F, Xi |
| Beveiligingsbeschrijving | Licht ontvlambare vloeistof en damp. Veroorzaakt huidirritatie. |
| VN-identificatienummers | VN 1206 |
| HS-code | 2902.41.000 |
| Gevarenklasse | 3 (Ontvlambare vloeistoffen) |
| Verpakkingsgroep | II |
| Toxiciteit | Kan schadelijk zijn bij inslikken en kan huid- en oogirritatie veroorzaken |
Heptaansynthesemethoden
Er zijn verschillende methoden om C7H16 te synthetiseren, maar de belangrijkste methode is de gefractioneerde destillatie van aardolie of ruwe olie. Deze methode scheidt koolwaterstoffen op basis van hun kookpunt, en door het destilleren van het deel van het mengsel dat kookt bij een temperatuur tussen 90 en 100°C ontstaat C7H16.
Een andere methode voor het synthetiseren van C7H16 omvat het katalytisch hydrogeneren van hexeen of andere olefinen met behulp van een palladiumkatalysator bij verhoogde temperaturen en drukken.
Met behulp van het Fischer-Tropsch-proces kan men C7H16 synthetiseren door koolmonoxide en waterstofgas te laten reageren over een ijzer- of kobaltkatalysator bij hoge temperaturen en drukken. Bij dit proces ontstaat een mengsel van koolwaterstoffen, waaronder C7H16, dat kan worden gescheiden door gefractioneerde destillatie.
Om C7H16 te synthetiseren kan een platinakatalysator bij hoge temperaturen en drukken worden gebruikt om methylcyclohexaan te dehydrocycliseren. Bovendien kan het combineren van kleinere koolwaterstoffen, verkregen door het kraken van nafta of andere aardoliefracties, C7H16 produceren.
Over het geheel genomen omvat de synthese van C7H16 verschillende methoden, waarbij voornamelijk aardolie of ruwe olie als grondstof wordt gebruikt, en omvat het verschillende chemische reacties zoals destillatie, hydrogenering en dehydrocyclisatie.
Gebruik van heptaan
C7H16 heeft verschillende industriële en commerciële toepassingen, waaronder:
- Oplosmiddel: Wordt vaak gebruikt als oplosmiddel in verschillende industrieën, zoals de productie van olie en gas, rubber en lijm. Lost een breed scala aan verbindingen op, waaronder vetten, oliën en harsen.
- Brandstof: Gebruikt als referentiebrandstof voor benzinemotoren. Vaak gebruikt in onderzoekslaboratoria voor motortesten en -ontwikkeling.
- Extractie: Gebruikt als extractiemiddel voor natuurlijke producten, zoals plantaardige oliën, plantenextracten en essentiële oliën.
- Reiniging: Gebruikt als reinigingsmiddel in de elektronica-industrie. Wordt gebruikt om verontreinigingen uit elektronische componenten te verwijderen.
- Laboratoriumreagens: Gebruikt als reagens in verschillende laboratoriumprocedures, waaronder DNA-extractie, chromatografie en spectroscopie.
- Verfverdunner: Wordt gebruikt als verfverdunner voor het verdunnen van verf op oliebasis en voor het reinigen van verfapparatuur.
- Lijm: Wordt gebruikt als lijm bij diverse toepassingen, zoals lamineren, lijmen en afdichten.
Vragen:
Vraag: Wat is de waarde van n in ch3(ch2)nch3 als de naam van de koolwaterstof heptaan is?
A: De waarde van n in ch3(ch2)nch3 voor heptaan is 5.
Vraag: Is heptaan oplosbaar in water?
A: Nee, C7H16 is niet oplosbaar in water omdat het een niet-polaire koolwaterstof is en water een polair molecuul.
Vraag: Is heptaan polair?
A: Nee, C7H16 is een niet-polaire koolwaterstof vanwege de symmetrische moleculaire structuur en de gelijke verdeling van elektronen tussen koolstof- en waterstofatomen.
Vraag: Wat is heptaan?
A: C7H16 is een alkaankoolwaterstof met rechte keten met de chemische formule C7H16. Het is een kleurloze vloeistof met een karakteristieke geur en wordt vaak gebruikt als referentiebrandstof voor benzinemotoren.
Vraag: Wat is de naam van deze koolwaterstof? C7H16
A: De naam van deze koolwaterstof is C7H16.
Vraag: Hoeveel heptaan-isomeren?
A: C7H16 heeft negen mogelijke isomeren, waaronder isomeren met rechte en vertakte keten.
Vraag: Is heptaan vluchtig?
A: Ja, C7H16 is een vluchtige vloeistof met een laag kookpunt van 98,4°C en een hoge dampdruk.
Vraag: Wat is de molecuulformule van heptaan?
A: De molecuulformule van heptaan is C7H16.
Vraag: Wat is meer polair hexaan of heptaan?
A: Hexaan en C7H16 zijn beide niet-polaire koolwaterstoffen, maar C7H16 is iets polairder dan hexaan vanwege de grotere moleculaire omvang en de grotere London-dispersiekrachten.
Vraag: Valt heptaan onder de PSM?
A: Ja, C7H16 is een stof die valt onder de Process Safety Management (PSM)-voorschriften, die van toepassing zijn op faciliteiten waar bepaalde gevaarlijke chemicaliën boven een bepaalde drempelhoeveelheid worden verwerkt, gebruikt of opgeslagen.
