Kaliummetabisulfiet (K2S2O5), ook bekend als kaliumpyrosulfiet, is een conserveermiddel dat veel wordt gebruikt bij de wijnbereiding en voedselverwerking. Het werkt door het vrijgeven van zwaveldioxide, dat de groei van bacteriën en gisten remt, waardoor de houdbaarheid van producten wordt verlengd.
| Naam van IUPAC | Kaliumpyrosulfiet |
| Moleculaire formule | K2S2O5 |
| CAS-nummer | 16731-55-8 |
| Synoniemen | Kaliumdisulfiet, pyrozwavelzuur, dikaliumzout, kaliummetabisulfiet |
| InChi | InChI=1S/2K.H2O5S2/c;;1-6(2)7(3,4)5/h;;(H,1,2)(H,3,4,5)/q2*+1; /p-2 |
Eigenschappen van kaliummetabisulfiet
Kaliummetabisulfietformule
De chemische formule voor kaliummetabisulfiet is K2S2O5. Dit betekent dat elk kaliummetabisulfietmolecuul twee kaliumionen, twee zwavelatomen en vijf zuurstofatomen bevat. De formule is belangrijk bij het bepalen van de chemische eigenschappen en het gedrag van K2S2O5 in verschillende reacties en processen.
Kaliummetabisulfiet Molaire massa
K2S2O5 heeft een molaire massa van 222,31 g/mol. Dit wordt berekend door de atoommassa’s van de samenstellende elementen op te tellen: twee kaliumatomen (elk 39,10 g/mol), twee zwavelatomen (elk 32,06 g/mol) en vijf zuurstofatomen (elk 16,00 g/mol). . De molaire massa is belangrijk bij het bepalen van de hoeveelheid K2S2O5 die nodig is voor een bepaalde reactie of proces.
Kookpunt van kaliummetabisulfiet
K2S2O5 heeft geen gedefinieerd kookpunt omdat het ontleedt voordat het een kookpunt bereikt. Bij hoge temperaturen wordt K2S2O5 afgebroken, waarbij zwaveldioxide vrijkomt, het actieve ingrediënt dat als conserveermiddel werkt.
Kaliummetabisulfiet Smeltpunt
K2S2O5 heeft een smeltpunt van ongeveer 190°C (374°F). Bij deze temperatuur smelt de vaste verbinding en verandert in een heldere vloeistof. Het smeltpunt is belangrijk bij het bepalen van de juiste hanterings- en opslagomstandigheden voor K2S2O5.
Dichtheid van kaliummetabisulfiet g/ml
De dichtheid van K2S2O5 is ongeveer 2,34 g/ml. Dit betekent dat een bepaald volume K2S2O5 2,34 keer meer weegt dan hetzelfde volume water. De dichtheid is belangrijk bij het bepalen van de juiste hoeveelheid K2S2O5 die in een bepaald proces moet worden gebruikt.
Kaliummetabisulfiet Molecuulgewicht
Het molecuulgewicht van K2S2O5 is 222,31 g/mol. Dit wordt berekend door de atoommassa’s van de samenstellende elementen op te tellen: twee kaliumatomen, twee zwavelatomen en vijf zuurstofatomen. Het molecuulgewicht is belangrijk bij het bepalen van de hoeveelheid K2S2O5 die nodig is voor een bepaalde reactie of proces.
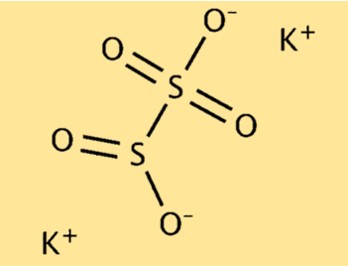
Structuur van kaliummetabisulfiet
K2S2O5 heeft een moleculaire structuur die bestaat uit twee kaliumionen (K+) en één pyrosulfietion (S2O5^2-). Het pyrosulfietion bestaat uit twee zwavelatomen en vijf zuurstofatomen. De twee kaliumionen worden aangetrokken door het negatief geladen pyrosulfietion en vormen een stabiele ionische verbinding.
Oplosbaarheid van kaliummetabisulfiet
K2S2O5 is oplosbaar in water, alcohol en glycerol. De oplosbaarheid in water varieert afhankelijk van de temperatuur en de concentratie. Bij kamertemperatuur is het zeer oplosbaar in water, met een oplosbaarheid van ongeveer 70 g/100 ml. Bij hogere concentraties kan het echter minder oplosbaar worden en neerslagen vormen.
| Verschijning | Wit of lichtgeel kristallijn poeder |
| Soortelijk gewicht | 2,34 bij 20°C |
| Kleur | Wit tot lichtgeel |
| Geur | Zwavelachtig, kruidig |
| Molaire massa | 222,31 g/mol |
| Dikte | 2,34 g/ml bij 25°C |
| Fusie punt | 190-240°C |
| Kookpunt | Breekt af voordat het kookt |
| Flitspunt | Niet van toepassing (vast) |
| oplosbaarheid in water | Oplosbaar in water |
| Oplosbaarheid | Oplosbaar in ethanol en glycerol, enigszins oplosbaar in ether |
| Dampdruk | Verwaarloosbaar bij kamertemperatuur |
| Dampdichtheid | Niet van toepassing (vast) |
| pKa | 4.34 |
| pH | 4,5-5,5 in 10% oplossing |
Veiligheid en gevaren van kaliummetabisulfiet
K2S2O5 kan veiligheidsrisico’s met zich meebrengen als het niet op de juiste manier wordt behandeld. Bij inademing kan het huidirritatie, oogirritatie en ademhalingsproblemen veroorzaken. Direct contact met de stof kan roodheid, jeuk en een branderig gevoel veroorzaken. Het kan ook spijsverteringsproblemen veroorzaken als het wordt ingeslikt. Bij verhitting kan de stof giftig zwaveldioxidegas vrijgeven. Adequate ventilatie is daarom noodzakelijk tijdens hantering en opslag. Het is belangrijk om geschikte persoonlijke beschermingsmiddelen te dragen, zoals handschoenen en een veiligheidsbril, bij het hanteren van K2S2O5. Een goede opslag is ook van cruciaal belang, omdat het kan reageren met zuren, metalen en andere chemicaliën.
| Gevarensymbolen | Xi (irriterend) |
| Beveiligingsbeschrijving | Houd de container goed gesloten en droog; Niet inslikken; Draag geschikte beschermende kleding, handschoenen en oog-/gezichtsbescherming; Bij contact met de ogen onmiddellijk met veel water afspoelen en een arts raadplegen; Bij inslikken onmiddellijk een arts raadplegen en de verpakking of het etiket tonen. |
| VN-identificatienummers | VN 2676 |
| HS-code | 2832.10.00 |
| Gevarenklasse | 8 – Bijtende stoffen |
| Verpakkingsgroep | III |
| Toxiciteit | LD50 (rat, oraal) – 2.000 mg/kg; LC50 (rat, inademing) – 17 ppm/4 uur |
Methoden voor de synthese van kaliummetabisulfiet
Verschillende methoden kunnen K2S2O5 synthetiseren.
Een gebruikelijke methode omvat de reactie tussen kaliumhydroxide en zwaveldioxide. Het reactievat combineert de twee chemicaliën en verwarmt ze. Het resulterende gas stroomt door het water en produceert kaliumsulfiet . Waterstofperoxide oxideert kaliumsulfiet en vormt kaliumsulfaat. Zwaveldioxide reageert met kaliumsulfaat en produceert K2S2O5.
Een andere methode omvat de reactie van kaliumcarbonaat en zwaveldioxide. Het reactievat mengt de twee chemicaliën en verwarmt ze. Het mengsel produceert een gas dat door een oplossing van kaliumsulfiet gaat, waardoor kaliumbisulfiet ontstaat. Waterstofperoxide oxideert kaliumbisulfiet en vormt kaliumsulfaat. Zwaveldioxide reageert met kaliumsulfaat en produceert K2S2O5.
Gebruik van kaliummetabisulfiet
K2S2O5 heeft een breed scala aan toepassingen in diverse industrieën. Enkele veel voorkomende toepassingen zijn:
- Voedselbehoud: Gebruikt als voedselconserveermiddel om bederf te voorkomen en de houdbaarheid te verlengen. Veel gebruikt bij de productie van wijn, bier en vruchtensappen.
- Fotografie: Gebruikt in de fotografie als ontwikkelaar en fixeermiddel voor films en afdrukken.
- Textielindustrie: Gebruikt in de textielindustrie om overtollig verven en bleken uit stoffen te verwijderen.
- Waterbehandeling: Gebruikt als chemische stof voor waterbehandeling om chloor en andere onzuiverheden te verwijderen.
- Farmaceutische industrie: Gebruikt in de farmaceutische industrie als antioxidant om afbraak van geneesmiddelen te voorkomen.
- Goudwinning: Gebruikt in de goudwinning om goud te scheiden van andere metalen en onzuiverheden.
- Chemische productie: Gebruikt bij de productie van verschillende chemicaliën zoals kleurstoffen, harsen en kunststoffen.
- Pulp- en papierindustrie: Gebruikt in de pulp- en papierindustrie om papierproducten witter te maken.
Vragen:
Vraag: Hoeveel kaliummetabisulfiet per gallon?
A: De benodigde hoeveelheid K2S2O5 per gallon varieert afhankelijk van het beoogde gebruik. Voor het maken van wijn is de aanbevolen hoeveelheid 1/16 tot 1/4 theelepel per gallon. Voor het maken van cider is de aanbevolen hoeveelheid 1/4 theelepel per gallon. Het is belangrijk om de aanbevolen dosering nauwgezet te respecteren om het gewenste effect te garanderen en overconsumptie, die schadelijk kan zijn, te voorkomen.
Vraag: Wanneer moet ik kaliumsorbaat of kaliummetabisulfiet gebruiken?
A: Kaliumsorbaat en K2S2O5 worden beide gebruikt als conserveermiddel in de voedingsmiddelen- en drankenindustrie. Kaliumsorbaat wordt gebruikt om de groei van gist en schimmels te voorkomen, terwijl K2S2O5 wordt gebruikt om de groei en oxidatie van bacteriën te remmen. Kaliumsorbaat wordt doorgaans gebruikt in niet-zure producten, zoals siropen en jam, terwijl K2S2O5 wordt gebruikt in zure producten zoals wijn en cider. De keuze tussen de twee condooms is afhankelijk van het specifieke product en de vereisten ervan.
Vraag: Waar kan ik kaliummetabisulfiet kopen?
A: K2S2O5 kan worden gekocht bij chemische winkels, online winkels en thuisbrouwwinkels. Het is belangrijk om ervoor te zorgen dat het product van hoge kwaliteit is en bedoeld is voor het beoogde gebruik.
Vraag: Hoeveel kaliummetabisulfiet per gallon cider?
A: De aanbevolen hoeveelheid K2S2O5 voor het maken van cider is 1/4 theelepel per gallon. Deze hoeveelheid wordt na de gisting toegevoegd om oxidatie en bacteriegroei te voorkomen en om de smaak en kwaliteit van de cider te behouden.
Vraag: Wat is het verschil tussen K2S2O5 en K2S2O8?
A: K2S2O5 en K2S2O8 zijn beide kaliumzouten, maar ze hebben verschillende structuren en chemische eigenschappen. K2S2O5 is een wit kristallijn poeder dat wordt gebruikt als conserveermiddel en antioxidant, terwijl K2S2O8 een sterk oxidatiemiddel is dat wordt gebruikt bij chemische reacties zoals organische synthese en afvalwaterzuivering. Het belangrijkste verschil tussen de twee zijn hun chemische eigenschappen en het beoogde gebruik.
