2-Buteen (CH3CHCHCH3) is een kleurloos gas dat wordt gebruikt bij de productie van verschillende chemicaliën. Het is brandbaar en verspreidt een lichte geur. 2-Buteen wordt vaak gebruikt bij de vervaardiging van synthetisch rubber en andere polymeren.
| Naam van IUPAC | Mais-2-ène |
| Moleculaire formule | C4H8 of CH3CHCHCH3 |
| CAS-nummer | 624-64-6 |
| Synoniemen | 2-Buteen, Buteen, Ethylethyleen, But-2-een, B-Buteen, Buteen-2 |
| InChi | InChI=1S/C4H8/c1-3-4-2/h3-4H,1-2H3 |
Eigenschappen van 2-buteen
Formule 2-Buteen
De chemische formule voor 2-buteen is C4H8. Dit betekent dat het molecuul vier koolstofatomen en acht waterstofatomen bevat. De formule geeft informatie over de soorten en aantallen atomen die in het molecuul aanwezig zijn, maar geeft geen informatie over de structuur of eigenschappen ervan.
2-Buteen molaire massa
But-2-een heeft een molaire massa van 56,11 g/mol. Molaire massa is de massa van één mol van een stof en wordt berekend door de atoommassa’s van alle atomen in het molecuul bij elkaar op te tellen. Voor but-2-een zijn er vier koolstofatomen en acht waterstofatomen, wat een totaal oplevert van 56,11 g/mol.
Kookpunt van 2-buteen
Het kookpunt van but-2-een is 0,88°C. Het kookpunt is de temperatuur waarbij een vloeistof in een gas verandert. In het geval van but-2-een is het bij kamertemperatuur een kleurloos gas, maar het kan tot een vloeistof worden gecondenseerd door de temperatuur te verlagen. Bij 0,88°C begint but-2-een te koken en verandert in een gas.
2-Buteen smeltpunt
But-2-een heeft geen duidelijk smeltpunt omdat het bij kamertemperatuur als gas bestaat. Als het echter wordt afgekoeld tot een temperatuur die laag genoeg is, kan het condenseren tot een vloeistof. Op dit punt zal de temperatuur waarbij het stolt afhangen van de omstandigheden van het experiment.
Dichtheid van 2-buteen g/ml
De dichtheid van but-2-een is 0,614 g/ml bij kamertemperatuur en druk. Dichtheid is de hoeveelheid massa per volume-eenheid. In het geval van but-2-een betekent dit dat er voor elke milliliter but-2-een 0,614 gram massa is.
Molecuulgewicht 2-buteen
Het molecuulgewicht van but-2-een is 56,11 g/mol. Het molecuulgewicht is de som van de atoomgewichten van alle atomen in een molecuul. In het geval van but-2-een zijn er vier koolstofatomen en acht waterstofatomen, wat een totaal oplevert van 56,11 g/mol.
2-buteenstructuur
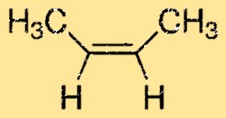
But-2-een heeft een lineaire structuur en behoort tot de alkeengroep. Het heeft twee dubbele koolstof-koolstofbindingen, waardoor het zijn karakteristieke reactiviteit krijgt. Het molecuul heeft een centraal koolstofatoom met twee methylgroepen eraan vast en twee waterstofatomen aan elk van de koolstofatomen aan de uiteinden van het molecuul.
| Verschijning | Kleurloos gas |
| Specifieke dichtheid | 0,614 bij 25°C |
| Kleur | Kleurloos |
| Geur | Goedaardig |
| Molaire massa | 56,11 g/mol |
| Dikte | 0,614 g/ml bij 25°C |
| Fusie punt | -139,8°C |
| Kookpunt | 0,88°C |
| Flitspunt | -19°C |
| oplosbaarheid in water | Onoplosbaar |
| Oplosbaarheid | Oplosbaar in organische oplosmiddelen |
| Dampdruk | 276,8 kPa bij 25°C |
| Dampdichtheid | 2,5 (lucht = 1) |
| pKa | 44 |
| pH | Niet toepasbaar |
Veiligheid en gevaren van 2-buteen
But-2-een kan verschillende veiligheidsrisico’s met zich meebrengen als het niet op de juiste manier wordt behandeld. Het is licht ontvlambaar en kan gemakkelijk ontbranden bij blootstelling aan hitte, vlammen of vonken. Het is ook irriterend voor de luchtwegen en de ogen en kan bij inademing duizeligheid, hoofdpijn en misselijkheid veroorzaken. Bovendien is het schadelijk bij inslikken en kan het interne organen beschadigen. Bij het hanteren van but-2-een moeten de juiste veiligheidsmaatregelen worden gevolgd, zoals het gebruik van beschermende uitrusting en goede ventilatie. Het is belangrijk om de juiste training en kennis van de potentiële gevaren te hebben voordat u met de chemische stof omgaat.
| Gevarensymbolen | Brandbaar |
| Beveiligingsbeschrijving | Verwijderd houden van hitte/vonken/open vuur/hete oppervlakken. Gebruik explosieveilige elektrische/ventilatie/verlichtingsapparatuur. Gebruik uitsluitend vonkvrij gereedschap. Neem voorzorgsmaatregelen tegen statische ontladingen. Houd de container goed gesloten. Opslaan in een goed geventileerde ruimte. |
| VN-identificatienummers | UN1012 |
| HS-code | 290110 |
| Gevarenklasse | 3 |
| Verpakkingsgroep | II |
| Toxiciteit | Schadelijk bij inslikken, irriterend voor de luchtwegen en de ogen. |
Methoden voor de synthese van 2-buteen
Verschillende methoden kunnen but-2-een synthetiseren, waaronder kraken van koolwaterstoffen, dehydratatie van 2-butanol en katalytische dehydrogenering van butanen.
Bij de kraakmethode worden koolwaterstoffen zoals nafta, diesel of kerosine op hoge temperaturen verhit, waardoor ze worden afgebroken tot kleinere moleculen, waaronder but-2-een. De werkwijze kan worden uitgevoerd door thermisch of katalytisch kraken.
Om but-2-een te produceren, gebruiken mensen dehydratatie van 2-butanol als een andere methode. Bij deze methode verwarmen ze 2-butanol met een dehydraterend middel, zoals zwavelzuur of fosforzuur , om but-2-een en water te creëren. De reactie is omkeerbaar en ze kunnen water uit het reactiemengsel verwijderen om de reactie in de richting van de vorming van but-2-een te duwen.
Een andere methode die wordt gebruikt om but-2-een te synthetiseren is de katalytische dehydrogenering van butanen. Dit proces omvat het verwarmen van butaan over een katalysator zoals chroomaluminiumoxide of platina om but-2-een en waterstof te produceren. De reactie heeft een hoge exothermiciteit en scheikundigen kunnen deze uitvoeren in een vastbed- of wervelbedreactor.
Gebruik van 2-buteen
But-2-een heeft een breed scala aan industriële en commerciële toepassingen vanwege zijn unieke chemische eigenschappen. Hier zijn enkele veelvoorkomende toepassingen van but-2-een:
- Butadieenproductie: Het is een voorloper van butadieen, een chemische stof die wordt gebruikt bij de productie van synthetisch rubber en andere elastomeren.
- Kunststofproductie: Gebruikt bij de productie van kunststoffen met hoge dichtheid polyethyleen (HDPE) en lineaire polyethyleen met lage dichtheid (LLDPE).
- Brandstofadditief: gebruikt als brandstofadditief om het octaangetal van benzine te verhogen.
- Oplosmiddel: Gebruikt als oplosmiddel in verschillende industrieën, zoals verven, coatings en lijmen.
- Chemisch tussenproduct: gebruikt als tussenproduct bij de productie van verschillende chemicaliën zoals butanol, butyraldehyde en boterzuur.
- Koelmiddel: Wordt in sommige toepassingen als koelmiddel gebruikt vanwege het lage kookpunt en de goede warmteoverdrachtseigenschappen.
- Onderzoek en ontwikkeling: Wordt ook gebruikt bij onderzoek en ontwikkeling om de reactiekinetiek en thermodynamica van verschillende chemische reacties te bestuderen.
Vragen:
Vraag: Wat beschrijft het beste de structuur van 2-buteen?
A: But-2-een is een onverzadigde koolwaterstof met een keten van vier koolstofatomen en een dubbele binding tussen het tweede en derde koolstofatoom.
Vraag: Wat is de hybridisatie aan de twee centrale koolstofatomen van 2-buteen?
A: De twee centrale koolstofatomen van but-2-een zijn sp²-gehybridiseerd, wat betekent dat ze elk drie gehybridiseerde orbitalen en één ongehybridiseerde p-orbitaal hebben.
Vraag: Welke reagentia kunnen worden gebruikt om cis-2-buteen om te zetten in trans-2-buteen?
A: Reagentia zoals broom of waterstofgas kunnen worden gebruikt om cis-but-2-een om te zetten in trans-but-2-een via een proces dat cis-trans-isomerisatie wordt genoemd.
Vraag: Waarom zou het moeilijk kunnen zijn om de scheiding van cis- en trans-2-buteen door TLC te visualiseren?
A: Het kan moeilijk zijn om de scheiding van cis- en trans-but-2-een te visualiseren met dunnelaagchromatografie (TLC), omdat de twee isomeren zeer vergelijkbare fysieke eigenschappen hebben, zoals polariteit en punt van oorsprong. koken, waardoor het moeilijk is om ze te onderscheiden met behulp van TLC.
Vraag: Hoeveel unieke stereo-isomeren resulteren uit de reactie waarbij trans-but-2-een betrokken is?
A: De reactie waarbij trans-but-2-een betrokken is, geeft aanleiding tot twee unieke stereo-isomeren, omdat er slechts twee mogelijke configuraties van substituenten rond de dubbele binding zijn: trans en cis.
