Isopropanol (isopropylalcohol), ook wel ontsmettingsalcohol genoemd, is een kleurloze, brandbare chemische verbinding. Het wordt veel gebruikt als oplosmiddel, ontsmettingsmiddel en antiseptisch middel vanwege de sterke en effectieve eigenschappen.
| IUPAC-naam | Propaan-2-ol |
| Moleculaire formule | C3H8O |
| CAS-nummer | 67-63-0 |
| Synoniemen | Isopropylalcohol, 2-propanol, droge propylalcohol, dimethylcarbinol, IPA, ontsmettingsalcohol |
| InChi | InChI=1S/C3H8O/c1-3(2)4/h3-4H,1-2H3 |
Eigenschappen van isopropanol
Structuur van isopropylalcohol
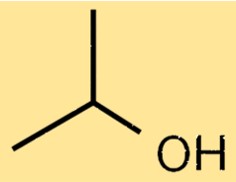
De structuur van isopropylalcohol bestaat uit een propaanketen met een hydroxylgroep (-OH) bevestigd aan het centrale koolstofatoom. De hydroxylgroep geeft isopropylalcohol zijn karakteristieke eigenschappen als alcohol, waaronder het vermogen om in water op te lossen en als oplosmiddel voor veel organische verbindingen te fungeren. De aanwezigheid van een methylgroep (-CH3) op het eerste koolstofatoom van de propaanketen geeft isopropylalcohol zijn unieke eigenschappen, waaronder zijn relatief lage kook- en smeltpunten.
Isopropylalcohol Molaire massa
De molaire massa van isopropylalcohol, ook wel ontsmettingsalcohol genoemd, is 60,1 g/mol. Molaire massa is de massa van één mol van een stof, die overeenkomt met de hoeveelheid van een stof die hetzelfde aantal entiteiten bevat als er atomen zijn in 12 gram koolstof-12. In het geval van isopropylalcohol bevat één mol stof 60,1 gram. Molaire massa is een belangrijke parameter in veel chemische berekeningen, vooral voor het bepalen van de hoeveelheid van een stof die nodig is voor een reactie of de concentratie van een oplossing.
Isopropylalcohol Kookpunt
Het kookpunt van isopropylalcohol is 82,6°C (180,7°F) bij atmosferische druk. Het kookpunt is de temperatuur waarbij een stof verandert van een vloeistof in een gas, en het is een fysieke eigenschap die wordt bepaald door de intermoleculaire krachten van de stof. Isopropylalcohol heeft een relatief laag kookpunt in vergelijking met andere alcoholen, zoals ethanol, vanwege de kleine omvang en de aanwezigheid van een methylgroep.
Isopropylalcohol Smeltpunt
Het smeltpunt van isopropylalcohol is -89°C (-128,2°F). Het smeltpunt is de temperatuur waarbij een stof verandert van een vaste stof in een vloeistof, en het is ook een fysische eigenschap die wordt bepaald door de intermoleculaire krachten van de stof. Isopropylalcohol heeft een relatief laag smeltpunt in vergelijking met andere alcoholen vanwege de kleine omvang en de aanwezigheid van een methylgroep.
Isopropylalcohol Dichtheid g/ml
De dichtheid van isopropylalcohol is 0,786 g/ml bij kamertemperatuur (20°C of 68°F). Dichtheid is de massa van een stof per volume-eenheid en is een fysieke eigenschap die wordt bepaald door de atomaire en moleculaire structuur van de stof. Isopropylalcohol heeft een lagere dichtheid dan water, dat bij kamertemperatuur een dichtheid heeft van 1 g/ml.
Isopropylalcohol Molecuulgewicht
Het molecuulgewicht van isopropylalcohol is 60,1 g/mol. Het molecuulgewicht is de som van de atoomgewichten van alle atomen in een molecuul en is een karakteristieke eigenschap van de stof. Isopropylalcohol heeft een relatief laag molecuulgewicht vergeleken met andere alcoholen, zoals ethanol, dat een molecuulgewicht heeft van 46,1 g/mol.
Isopropylalcoholformule
De chemische formule voor isopropylalcohol is C3H8O. Deze formule vertegenwoordigt het aantal en de soorten atomen waaruit het isopropylalcoholmolecuul bestaat. De formule laat zien dat isopropylalcohol drie koolstofatomen, acht waterstofatomen en één zuurstofatoom bevat. Deze formule is nuttig bij het bepalen van het molecuulgewicht en andere fysische en chemische eigenschappen van isopropylalcohol.
| Verschijning | Heldere, kleurloze vloeistof |
| Soortelijk gewicht | 0,786 g/ml bij 20°C |
| Kleur | Kleurloos |
| Geur | Karakteristiek, alcoholisch |
| Molaire massa | 60,1 g/mol |
| Dikte | 0,786 g/ml bij 20°C |
| Fusie punt | -89°C (-128,2°F) |
| Kookpunt | 82,6°C (180,7°F) bij atmosferische druk |
| Flitspunt | 12,2°C (54°F) |
| oplosbaarheid in water | Volledig mengbaar |
| Oplosbaarheid | Mengbaar met organische oplosmiddelen |
| Dampdruk | 33,8 mmHg bij 20°C |
| Dampdichtheid | 2,07 (lucht = 1) |
| pKa | 16.5 |
| pH | 7 (neutraal) |
Veiligheid en gevaren van isopropanol
Isopropanol is een licht ontvlambare en vluchtige vloeistof met een laag vlampunt en er moet voorzichtig mee worden omgegaan. Het kan irritatie aan de huid en ogen veroorzaken, en langdurige of herhaalde blootstelling kan leiden tot uitdroging en gebarsten huid. Isopropanol kan bij inademing ook irritatie van de luchtwegen en duizeligheid veroorzaken, en inslikken kan misselijkheid, braken en buikpijn veroorzaken. Het is belangrijk om geschikte beschermende uitrusting te gebruiken, zoals handschoenen, een veiligheidsbril en een gasmasker, wanneer u met isopropanol werkt. Opslag moet plaatsvinden in een koele, droge, goed geventileerde ruimte, uit de buurt van warmtebronnen en onverenigbare materialen.
| Gevarensymbolen | F, Xi |
| Beveiligingsbeschrijving | Licht ontvlambare vloeistof en damp. Veroorzaakt ernstige oogirritatie. Veroorzaakt huidirritatie. Schadelijk bij inslikking. Verdacht van het veroorzaken van genetische afwijkingen. Verdacht van schade aan de vruchtbaarheid of het ongeboren kind. Kan slaperigheid of duizeligheid veroorzaken. |
| AN-identificaties | VN1219 |
| HS-code | 2905.12.0000 |
| Gevarenklasse | 3 |
| Verpakkingsgroep | II |
| Toxiciteit | LD50 (oraal, rat): 5.630 mg/kg |
Methoden voor de synthese van isopropanol
Isopropanol, ook bekend als isopropylalcohol, kan op verschillende manieren worden gesynthetiseerd.
Een gebruikelijke methode omvat het hydrateren van propeen met behulp van een katalysator zoals zwavelzuur of fosforzuur. Het proces omvat de reactie van propeen met water in aanwezigheid van de katalysator, waarbij isopropanol en diisopropylether als bijproduct worden geproduceerd.
Een andere methode omvat de hydrogenering van aceton met behulp van een katalysator zoals koperchromiet of nikkel. Het proces maakt gebruik van waterstofgas en de katalysator om aceton te reduceren tot isopropanol.
Sommige bacteriestammen kunnen isopropanol produceren door koolhydraten, zoals maïs of suikerriet, te fermenteren. Het proces omvat het omzetten van koolhydraten in glucose, die vervolgens door bacteriën wordt gefermenteerd om isopropanol te produceren.
Een andere methode voor het synthetiseren van isopropanol omvat de reactie van een Grignard-reagens met formaldehyde , gevolgd door zuurgekatalyseerde hydrolyse. Deze methode is vooral nuttig voor het produceren van isopropanol met een hoge zuiverheidsgraad.
Ongeacht de gebruikte methode moet het resulterende isopropanol worden gezuiverd door destillatie of andere methoden om alle onzuiverheden te verwijderen en het gewenste zuiverheidsniveau te bereiken.
Gebruik van isopropanol
Isopropanol, ook bekend als isopropylalcohol, heeft vele toepassingen in verschillende industrieën en toepassingen. Enkele veel voorkomende toepassingen van isopropanol zijn:
- Oplosmiddel: Een effectief oplosmiddel voor een verscheidenheid aan stoffen, waaronder oliën, harsen en gommen. Gebruikt als oplosmiddel bij de vervaardiging van coatings, inkten en lijmen.
- Desinfectiemiddel: Gebruikt als desinfectiemiddel in gezondheidszorginstellingen, laboratoria en andere omgevingen. Het is effectief tegen veel ziekteverwekkers, waaronder bacteriën, virussen en schimmels.
- Antiseptisch: Gebruikt als antisepticum in verschillende plaatselijke toepassingen, zoals handdesinfecterende middelen en desinfecterende doekjes. Wordt ook gebruikt bij het voorbereiden van de huid op medische procedures.
- Reinigingsmiddel: gebruikt in diverse reinigingstoepassingen, zoals het reinigen van elektronische componenten, optische lenzen en precisie-instrumenten.
- Brandstof: Gebruikt als brandstofadditief in benzine- en dieselmotoren. Het wordt ook gebruikt als brandstof in sommige raceauto’s.
- Extractiemiddel: gebruikt als extractiemiddel bij de productie van essentiële oliën, smaakstoffen en parfums.
- Chemisch tussenproduct: gebruikt als chemisch tussenproduct bij de productie van verschillende chemicaliën, zoals aceton, isopropylacetaat en glycerol.
Vragen:
Vraag: Is isopropylalcohol polair?
A: Ja, isopropylalcohol is een polair molecuul. Het heeft een hydroxylgroep (-OH) bevestigd aan een keten van drie koolstofatomen, waardoor het een polair molecuul is. Deze polariteit maakt het voor veel stoffen een goed oplosmiddel.
Vraag: Is isopropylalcohol hetzelfde als ontsmettingsalcohol?
A: Ontsmettingsalcohol is een soort alcohol gemaakt van isopropylalcohol of ethanol. Isopropylalcohol is een van de hoofdingrediënten van ontsmettingsalcohol, samen met water en andere verbindingen. Dus hoewel isopropylalcohol niet precies hetzelfde is als ontsmettingsalcohol, is het wel een belangrijk onderdeel van ontsmettingsalcohol.
Vraag: Waar kan ik isopropylalcohol kopen?
A: Isopropylalcohol kan bij verschillende bronnen worden gekocht, waaronder apotheken, supermarkten en online winkels. Het wordt gewoonlijk verkocht in concentraties variërend van 70% tot 99%, waarbij 70% de meest voorkomende is. Het is belangrijk op te merken dat isopropylalcohol vanwege de grote vraag en tekorten in sommige gebieden moeilijk te vinden kan zijn.
