Chloordioxide of ClO2 is een zeer effectief, snelwerkend bleekmiddel dat wordt gebruikt bij de waterbehandeling en het bewaren van voedsel. Het is een geelachtig groen gas met een scherpe geur.
| IUPAC-naam | Chloordioxide |
| Moleculaire formule | ClO2 |
| CAS-nummer | 10049-04-4 |
| Synoniemen | Chloorperoxide, ClO2, chloor(IV)oxide |
| InChi | InChI=1S/ClO2/c2-1-3 |
Chloordioxide formule
De formule voor chloordioxide is ClO2. Het is een zeer reactief gas dat bestaat uit één chlooratoom en twee zuurstofatomen. De formule van chloordioxide weerspiegelt de moleculaire structuur, die cruciaal is voor het begrijpen van de fysische en chemische eigenschappen ervan, inclusief de reactiviteit, stabiliteit en oplosbaarheid.
ClO2 Molaire massa
ClO2 heeft een molaire massa van 67,45 g/mol. Het is een zeer reactief oxidatiemiddel, bekend om zijn sterke witmakende eigenschappen. ClO2 wordt veel gebruikt als desinfectie- en ontsmettingsmiddel in verschillende industriële en huishoudelijke toepassingen, waaronder waterbehandeling, papierbleken en voedselconservering. De molaire massa van een stof speelt een cruciale rol bij het bepalen van de fysische en chemische eigenschappen ervan, inclusief de dichtheid, het kookpunt en de oplosbaarheid.
Kookpunt van ClO2
Het kookpunt van ClO2 is 11,3°C (52,3°F). ClO2 bestaat als een geelachtig groen gas bij standaardtemperatuur en -druk. Het heeft een scherpe geur en is zeer reactief, waardoor het een uitstekend oxidatiemiddel is. Het kookpunt van een stof is een belangrijke fysieke eigenschap die de stabiliteit, vluchtigheid en transporteerbaarheid ervan helpt bepalen.
ClO2 Smeltpunt
Het smeltpunt van ClO2 is -51,5°C (-60,7°F). Als gas bij standaardtemperatuur en -druk heeft het geen vaste toestand. ClO2 is zeer oplosbaar in water en wordt vaak gebruikt als desinfectiemiddel en ontsmettingsmiddel bij waterbehandeling en toepassingen voor het bewaren van voedsel. Het smeltpunt van een stof is een belangrijke eigenschap die het fysische en chemische gedrag ervan kan beïnvloeden, vooral bij reacties die een toestandsverandering met zich meebrengen.
ClO2-dichtheid g/ml
De dichtheid van ClO2 is 1,97 g/ml bij standaardtemperatuur en -druk. Het is een zeer reactief gas dat vaak wordt gebruikt als bleekmiddel en ontsmettingsmiddel in verschillende industriële toepassingen. De dichtheid van een stof is een belangrijke fysieke eigenschap die het gedrag ervan in verschillende processen kan beïnvloeden, waaronder transport, opslag en behandeling.
ClO2 Molecuulgewicht
Het molecuulgewicht van ClO2 bedraagt 67,45 g/mol. Het is een oxidatiemiddel dat veel wordt gebruikt bij waterbehandeling, papierbleken en voedselconservering. Het molecuulgewicht van een stof is een belangrijke eigenschap die het fysische en chemische gedrag ervan beïnvloedt, inclusief de dichtheid, het kookpunt en de oplosbaarheid.
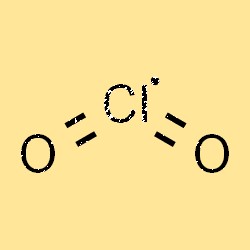
Structuur van ClO2
De structuur van ClO2 wordt weergegeven door de molecuulformule ClO2. Het is een zeer reactief gas dat bestaat uit één chlooratoom en twee zuurstofatomen. Het molecuul heeft een gebogen vorm en is polair van aard, wat betekent dat het een positief uiteinde en een negatief uiteinde heeft. De structuur van ClO2 speelt een cruciale rol in de chemische reactiviteit, stabiliteit en oplosbaarheid ervan in verschillende oplosmiddelen.
| Verschijning | Geelachtig groen gas |
| Soortelijk gewicht | 1,97 g/ml |
| Kleur | geelachtig groen |
| Geur | Akko |
| Molaire massa | 67,45 g/mol |
| Dikte | 1,97 g/ml |
| Fusie punt | -51,5°C (-60,7°F) |
| Kookpunt | 11,3°C (52,3°F) |
| Flitspunt | Niet van toepassing (gas) |
| oplosbaarheid in water | Zeer oplosbaar |
| Oplosbaarheid | Oplosbaar in water en organische oplosmiddelen |
| Dampdruk | Niet gespecificeerd |
| Dampdichtheid | Niet gespecificeerd |
| pKa | Niet gespecificeerd |
| pH | Niet gespecificeerd |
Opmerking Sommige van de vermelde waarden zijn schattingen op basis van beschikbare gegevens. Voor specifieke en nauwkeurige informatie over de eigenschappen van een stof kunt u altijd het beste een betrouwbare bron raadplegen.
Veiligheid en gevaren van chloordioxide
ClO2 is een zeer reactieve en giftige stof die, als er niet op de juiste manier mee wordt omgegaan, aanzienlijke gezondheids- en veiligheidsrisico’s kan opleveren. Blootstelling aan hoge concentraties ClO2-gas kan irritatie van de ogen, neus en keel veroorzaken, evenals ademhalingsproblemen en ademhalingsmoeilijkheden. Het innemen van ClO2 kan ernstige spijsverteringsproblemen veroorzaken, waaronder misselijkheid, braken en diarree. Huidcontact met ClO2 kan irritatie en chemische brandwonden veroorzaken. Bovendien is ClO2 brandbaar en kan ontbranden in aanwezigheid van hitte of vonken. Om de risico’s die met ClO2 gepaard gaan tot een minimum te beperken, is het belangrijk om bij de omgang met ClO2 geschikte persoonlijke beschermingsmiddelen te gebruiken, zoals handschoenen, een veiligheidsbril en een gasmasker. Het is ook belangrijk om veilige opslag- en hanteringspraktijken te volgen om het vrijkomen van ClO2 in het milieu te voorkomen.
| Gevarensymbolen | Oxidatiemiddel, giftig |
| Beveiligingsbeschrijving | S2- Buiten bereik van kinderen bewaren. S22- Stof niet inademen. S26- Bij aanraking met de ogen onmiddellijk met veel water afspoelen en een arts raadplegen. |
| AN-identificaties | VN 1479 |
| HS-code | 2828.90.90 |
| Gevarenklasse | 5.1 |
| Verpakkingsgroep | III |
| Toxiciteit | Chloordioxide is zeer giftig bij inademing, inslikken of bij contact met de huid. Dit kan ademhalingsproblemen, spijsverteringsproblemen, oogirritatie en chemische brandwonden veroorzaken. |
Synthesemethoden voor chloordioxide
ClO2 wordt doorgaans op twee manieren gesynthetiseerd: het chloraat-chlorietproces en het elektrolyseproces.
Het chloraat-chlorietproces omvat de reactie van natriumchloraat met een zuur, zoals zwavelzuur, om ClO2 te produceren. Dit proces kan op industriële schaal worden uitgevoerd en wordt veel gebruikt voor de productie van ClO2 voor waterbehandeling en andere toepassingen.
Bij het elektrolyseproces wordt gebruik gemaakt van elektrische stroom om ClO2 te genereren. Dit proces wordt meestal in het laboratorium uitgevoerd en wordt gebruikt voor de productie van kleine hoeveelheden ClO2 voor onderzoek en experimenten.
Ongeacht de gebruikte synthesemethode is het belangrijk om de juiste veiligheidsprotocollen te volgen en geschikte beschermende uitrusting te gebruiken bij het hanteren van ClO2. Dit omvat het dragen van handschoenen, oogbescherming en een gasmasker om blootstelling aan het zeer giftige gas te voorkomen.
Naast deze methoden kan chloordioxide ook worden gegenereerd door de reactie van natriumchloriet met een zuur of door de reactie van natriumchloraat met zoutzuur. De keuze van de synthesemethode zal afhangen van de specifieke toepassing en de gewenste eigenschappen van het eindproduct.
Gebruik van chloordioxide
Chloordioxide is een veelzijdige chemische stof met een breed scala aan toepassingen, waaronder waterbehandeling, conservering van voedsel en bleken. Enkele van de meest voorkomende toepassingen van chloordioxide zijn onder meer
Chloordioxide voor waterbehandeling wordt vaak gebruikt als desinfectiemiddel bij de behandeling van drinkwater, afvalwater en industrieel proceswater. Het is zeer effectief tegen een breed scala aan ziekteverwekkers, waaronder bacteriën, virussen en parasieten, en wordt vaak gebruikt als alternatief voor chloor of ozon.
Chloordioxide voor het conserveren van voedsel wordt gebruikt als antimicrobieel middel bij het conserveren van fruit, groenten, vlees en andere voedingsproducten. Het is effectief tegen een verscheidenheid aan micro-organismen, waaronder bacteriën, gisten en schimmels, en helpt de houdbaarheid van voedingsmiddelen te verlengen.
Chloordioxide wordt gebruikt om houtpulp en andere vezels te bleken om heldere, uniforme kleuren te produceren. Het wordt ook gebruikt bij het bleken van textiel, zoals katoen en wol, om onzuiverheden te verwijderen en de witheid te verbeteren.
Andere toepassingen Chloordioxide wordt ook gebruikt bij de behandeling van industrieel en gemeentelijk afval, maar ook bij de productie van andere chemicaliën, zoals chloraten, chlooramines en andere ontsmettingsmiddelen. In al zijn toepassingen is chloordioxide zeer effectief en biedt het vele voordelen ten opzichte van andere chemische behandelingen. Het is echter belangrijk om voorzichtig te zijn bij het hanteren en gebruiken van chloordioxide, aangezien het een zeer reactieve en giftige stof is die aanzienlijke gezondheids- en veiligheidsrisico’s kan opleveren als er niet op de juiste manier mee wordt omgegaan.
