Sucrose is een soort suiker die algemeen bekend staat als tafelsuiker. Het is een disaccharide bestaande uit glucose en fructose en komt van nature voor in veel groenten en fruit.
| IUPAC-naam | α-D-glucopyranosyl-(1 → 2)-β-D-fructofuranoside |
| Moleculaire formule | C12H22O11 |
| CAS-nummer | 57-50-1 |
| Synoniemen | Sucrose, bietsuiker, rietsuiker, dodecakoolstofmonodechydraat, ((2R,3R,4S,5S,6R)-2-[(2S,3S,4S,5R)-3,4-dihydroxy-2,5-bis (hydroxymethyl )oxapent-2-yl]oxy-6-(hydroxymethyl)oxahexaan-3,4,5-triol) |
| InChi | InChI=1S/C12H22O11/c13-1-4-6-10(16)15-12(19)18-7(2-14)8(3-15)9(17)5-11(6)20/ h2-19,13-20H,1H2/t10-,11+,12-/m1/s1 |
Eigenschappen van sucrose
Kookpunt van sucrose
Het kookpunt van sucrose is ongeveer 320 ° F (160 ° C) bij standaarddruk. Deze waarde wordt bepaald door de intermoleculaire krachten die in de stof aanwezig zijn en wordt gebruikt om deze te identificeren en te scheiden van andere stoffen.
Smeltpunt van sucrose
Het smeltpunt van sucrose is ongeveer 186°F (86°C). Deze waarde is ook een belangrijk kenmerk dat wordt gebruikt om sucrose te identificeren en te scheiden van andere stoffen.
Molaire massa van sucrose
De molaire massa van sucrose is 342,3 g/mol. Deze waarde wordt berekend op basis van het aantal atomen van elk element (koolstof, waterstof en zuurstof) in een sucrosemolecuul.
Sacharosedichtheid g/ml
De dichtheid van sucrose is ongeveer 1,58 g/ml, wat iets hoger is dan de dichtheid van water. Deze waarde kan worden gebruikt om de concentratie sucrose in een oplossing te bepalen.
Molecuulgewicht van sucrose
Het molecuulgewicht van C12H22O11 is 342,3 g/mol. Deze waarde wordt gebruikt om de hoeveelheid sucrose in een monster te berekenen op basis van de massa.
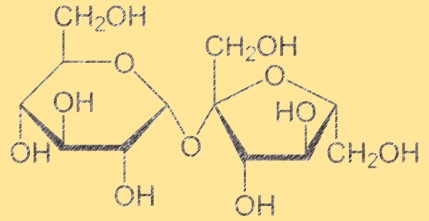
Structuur van sucrose
Sucrose, een disaccharide bestaande uit twee eenvoudige suikers – glucose en fructose – verbonden door een glycosidische binding, heeft een lineaire structuur en een moleculaire formule van C12H22O11. De 1:2 verhouding van glucose en fructose in sucrose kan gemakkelijk door sucrose tot individuele suikers worden gehydrolyseerd. De structuur van sucrose speelt een cruciale rol bij het bepalen van de fysische en chemische eigenschappen ervan, evenals de functie ervan als energiebron in het lichaam.
| Verschijning | Witte kristallijne vaste stof |
| Soortelijk gewicht | 1,58 g/ml |
| Kleur | Wit |
| Geur | Geurloos |
| Molaire massa | 342,3 g/mol |
| Dikte | 1,58 g/ml |
| Fusie punt | 186°F (86°C) |
| Kookpunt | 320°F (160°C) |
| Flitspunt | Niet toepasbaar |
| oplosbaarheid in water | Zeer oplosbaar in water |
| Oplosbaarheid | Oplosbaar in ethanol, methanol en ethyleenglycol |
| Dampdruk | Niet toepasbaar |
| Dampdichtheid | Niet toepasbaar |
| pKa | Niet toepasbaar |
| pH | Neutrale |
Sucroseveiligheid en gevaren
Sucrose wordt over het algemeen als veilig beschouwd voor matige consumptie. Overconsumptie kan leiden tot tandbederf en bijdragen aan zwaarlijvigheid en daarmee samenhangende gezondheidsproblemen. Sucrose kan ook vocht aantrekken en vasthouden, waardoor voedselproducten kunnen bederven. Bij hoge concentraties kan sucrose huidirritatie en andere schadelijke effecten veroorzaken. Het hanteren van grote hoeveelheden droge sucrose moet met voorzichtigheid gebeuren om inademing en huidirritatie te voorkomen.
| Gevarensymbolen | Geen |
| Beveiligingsbeschrijving | Veilig voor matige consumptie. Overconsumptie kan tot gezondheidsproblemen leiden. |
| VN-identificatienummers | Niet toepasbaar |
| HS-code | 1701.99.90 |
| Gevarenklasse | Niet geclassificeerd als gevaarlijke stof |
| Verpakkingsgroep | Niet toepasbaar |
| Toxiciteit | Lage toxiciteit. Overconsumptie kan tot gezondheidsproblemen leiden. |
Methoden voor synthese van sucrose
Sucrose kan op een aantal manieren worden gesynthetiseerd, waaronder:
- Glucosestroop-inversie: Invertase hydrolyseert glucosestroop om glucose en fructose te produceren, die vervolgens opnieuw kunnen worden veresterd om sucrose te vormen.
- Fructose-isomerisatie: Aldolase isomeriseert fructose tot glucose en verestert het vervolgens opnieuw om sucrose te vormen.
- Chemische synthese: De Will-merkreactie synthetiseert sucrose uit glucose en fructose via een chemische reactie waarbij glucose wordt behandeld met fructose in aanwezigheid van een zure katalysator.
- Enzymatische synthese: Sucrosesynthase synthetiseert sucrose uit glucose en fructose.
Deze methoden worden gebruikt om sucrose op industriële schaal te produceren voor gebruik in voedsel- en drankproducten, evenals voor andere toepassingen waarbij sucrose nodig is. De keuze voor de synthesemethode is afhankelijk van verschillende factoren, waaronder het gewenste eindproduct en de beschikbaarheid van grondstoffen en technologie.
Gebruik van sucrose
Sucrose wordt veel gebruikt in verschillende toepassingen, waaronder:
- Voedings- en drankenindustrie: Voedings- en drankproducten zoals snoep, gebak en frisdranken gebruiken gewoonlijk sucrose als zoetstof.
- Farmaceutische industrie: Bij de productie van tabletten en capsules wordt sucrose als vulmiddel gebruikt, en er worden siropen en andere vloeibare doseringsvormen mee bereid.
- Landbouw: Planten halen energie uit sucrose, en ethanol en andere biobrandstoffen worden ook geproduceerd door het als substraat te gebruiken.
- Industriële toepassingen: Bij de productie van lijmen, harsen en andere industriële producten wordt sucrose als grondstof gebruikt.
- Onderzoek en laboratoriumgebruik: Biologische en chemische analyses gebruiken sucrose als referentiestandaard, en studies naar het cellulaire metabolisme gebruiken het ook als energiebron.
Sucrose is een veelzijdige stof met een breed scala aan toepassingen vanwege de zoete smaak, oplosbaarheid en andere eigenschappen. Het is ook overal verkrijgbaar en relatief goedkoop, waardoor het in veel industrieën een populaire keuze is.
