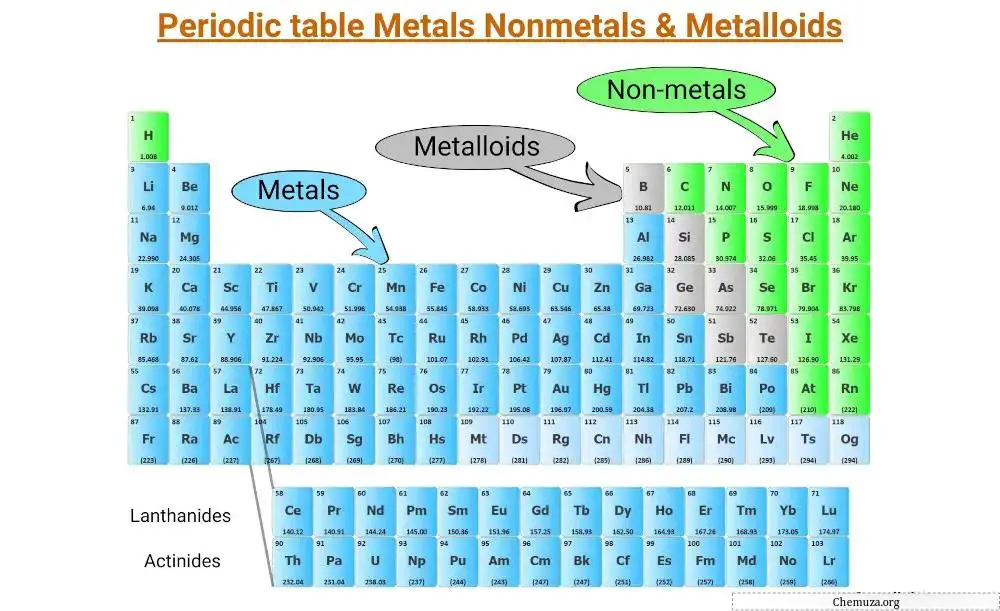
Alle elementen van het periodiek systeem kunnen worden ingedeeld in 3 hoofdcategorieën;
- Metalen
- Niet-metalen en
- Metalloïden
Metalen zijn over het algemeen glanzend, geleidend en taai en vormen de meeste elementen aan de linkerkant van het periodiek systeem.
Niet-metalen daarentegen zijn vaak kwetsbaar (sommige zijn gassen) en slechte geleiders, en bevinden zich voornamelijk aan de rechterkant van de tafel.
Metalloïden delen eigenschappen met metalen en niet-metalen en bevinden zich langs de “trap” die metalen en niet-metalen scheidt.
Laten we meer ontdekken over de metalen, niet-metalen en metalloïden van het periodiek systeem.
Metalen
Metalen vormen het merendeel van de elementen in het periodiek systeem en bevinden zich aan de linkerkant van de “trappenlijn” die metalen van niet-metalen scheidt.
Metalen delen bepaalde kenmerken, zoals hoge elektrische geleidbaarheid, glans, ductiliteit en kneedbaarheid .
Er zijn vijf hoofdsoorten metalen:
- Alkalimetalen , gelegen in groep 1 van het periodiek systeem, zijn zachte, zeer reactieve metalen die heftig reageren met water .
- Aardalkalimetalen , gelegen in groep 2, zijn ook behoorlijk reactief, maar minder dan alkalimetalen . Het zijn belangrijke bestanddelen van mineralen in de aardkorst.
- Overgangsmetalen , gelegen in de groepen 3 tot en met 11, zijn enkele van de meest bekende metalen, waaronder ijzer, goud en zilver. Ze hebben hoge smeltpunten en bevatten vaak gekleurde verbindingen. [1]
- Lanthaniden en actiniden , gelegen in blok f, staan bekend als “zeldzame aardmetalen”. Ze hebben unieke eigenschappen zoals magnetische en luminescerende eigenschappen. [2]
- Post-overgangsmetalen , die zich buiten de d- en f-blokken bevinden, omvatten metalen zoals aluminium , tin , lood , enz. Ze worden gebruikt voor een breed scala aan toepassingen, zoals de bouw, transport en elektronica.
Over het algemeen hebben metalen veel belangrijke toepassingen in ons dagelijks leven, van bouwconstructies en machines tot essentiële componenten van moderne technologie.
Niet-metalen
Niet-metalen zijn een groep chemische elementen die geen metallische eigenschappen vertonen. Ze bevinden zich aan de rechterkant van het periodiek systeem, behalve waterstof, dat zich in de linkerbovenhoek bevindt.
Niet-metalen kunnen worden onderverdeeld in verschillende categorieën, waaronder:
- Edelgassen: Dit zijn stabiele en inerte elementen, dat wil zeggen dat ze niet gemakkelijk reageren met andere elementen. Edelgassen zijn onder meer helium, neon, argon, krypton, xenon en radon.
- Halogenen: Dit zijn zeer reactieve niet-metalen die gemakkelijk verbindingen vormen met andere elementen. Halogenen omvatten fluor, chloor, broom, jodium en astatine.
- Andere niet-metalen: Deze omvatten elementen zoals waterstof, koolstof, stikstof, zuurstof, fosfor, zwavel en selenium.
Niet-metalen hebben verschillende fysische en chemische eigenschappen die hen onderscheiden van metalen.
Niet-metalen zijn bijvoorbeeld vaak slechte geleiders van warmte en elektriciteit en hebben lagere smelt- en kookpunten dan metalen.
Niet-metalen hebben ook de neiging negatieve ionen te vormen bij reactie met metalen, terwijl metalen de neiging hebben positieve ionen te vormen. [3]
Metalloïden
Metalloïden zijn elementen die eigenschappen delen met metalen en niet-metalen.
Ze bevinden zich langs de “trap” die de twee categorieën van het periodiek systeem scheidt.
Metalloïden omvatten elementen zoals:
Metalloïden hebben doorgaans eigenschappen die ze bruikbaar maken in technologische en industriële toepassingen.
Zo is silicium een belangrijk onderdeel van halfgeleiders, terwijl boor wordt gebruikt bij de productie van sterke en lichtgewicht legeringen. [4]
Arseen is in een verscheidenheid aan toepassingen gebruikt, onder meer als houtconserveringsmiddelen en insecticiden, hoewel het nu wordt erkend als een giftige stof. [5]
Een van de belangrijkste eigenschappen van metalloïden is hun vermogen om onder bepaalde omstandigheden elektriciteit te geleiden.
Silicium is bijvoorbeeld een halfgeleider, wat betekent dat het kan worden gebruikt om de elektriciteitsstroom in elektronische apparaten te regelen.
Metalloïden zijn over het algemeen ook bros en kunnen onder spanning breken, net als vaste niet-metalen.
Over het algemeen maken de unieke eigenschappen van metalloïden ze tot belangrijke elementen in verschillende toepassingen, waaronder technologie en elektronica.
Samenvatting
Het periodiek systeem bevat drie hoofdcategorieën elementen: metalen, niet-metalen en metalloïden.
Metalen bevinden zich aan de linkerkant van het periodiek systeem en hebben eigenschappen zoals hoge elektrische geleidbaarheid, glans, ductiliteit en kneedbaarheid.
Niet-metalen bevinden zich daarentegen aan de rechterkant van het periodiek systeem en zijn over het algemeen kwetsbaar en slechte geleiders.
Metalloïden delen eigenschappen met metalen en niet-metalen en bevinden zich langs de “trap” die de twee categorieën scheidt.
