Calciumhypochloriet (Ca(ClO)2) is een chemische verbinding die vaak wordt gebruikt als ontsmettingsmiddel en bleekmiddel. Het is effectief in het doden van bacteriën, virussen en algen in waterbehandeling en sanitaire voorzieningen.
| IUPAC-naam | Calciumhypochloriet |
| Moleculaire formule | Ca(ClO)2 |
| CAS-nummer | 7778-54-3 |
| Synoniemen | Calciumzout van onderchloorzuur, Bleekpoeder, Gechloreerde kalk, Calciumoxychloride, HTH, Cal hypo |
| InChi | InChI=1S/Ca.2ClO/c;2 1-2/q+2;2 -1 |
Eigenschappen van calciumhypochloriet
Calciumhypochlorietformule
Calciumhypochloriet heeft de chemische formule Ca(ClO)2. Het is een witte kristallijne vaste stof die een sterke chloorgeur afgeeft. Uit de formule voor calciumhypochloriet blijkt dat het één Ca+2-ion en twee ClO-ionen bevat. Het hypochlorietion heeft een negatieve lading en is verantwoordelijk voor de sterk oxiderende eigenschappen van de verbinding.
Calciumhypochloriet Molaire massa
De molaire massa van Ca(ClO)2 is 142,98 g/mol. Het wordt berekend door de atoommassa’s van calcium, chloor en zuurstof op te tellen die aanwezig zijn in een molecuul Ca(ClO)2. De molaire massa van Ca(ClO)2 is een belangrijke parameter die wordt gebruikt in verschillende chemische berekeningen.
Kookpunt van calciumhypochloriet
Ca(ClO)2 ontleedt voordat het zijn kookpunt bereikt. Het kookpunt is daarom niet goed gedefinieerd. Wanneer Ca(ClO)2 wordt verwarmd, ondergaat het thermische ontleding waarbij calciumchloride, zuurstof en chloorgas worden gevormd.
Calciumhypochloriet Smeltpunt
Het smeltpunt van Ca(ClO)2 is 100°C. Bij deze temperatuur smelt Ca(ClO)2 en vormt een heldere vloeistof. Ca(ClO)2 is zeer oplosbaar in water en als het in water oplost, komen er hypochlorietionen vrij, waardoor het een effectief desinfectiemiddel is.
Dichtheid van calciumhypochloriet g/ml
De dichtheid van Ca(ClO)2 bedraagt 2,35 g/ml. Het is een relatief dichte verbinding en zwaarder dan water. De hoge dichtheid van Ca(ClO)2 is te danken aan de aanwezigheid van calciumionen in het kristalrooster.
Calciumhypochloriet Molecuulgewicht
Het molecuulgewicht van Ca(ClO)2 bedraagt 142,98 g/mol. Het wordt berekend door de atoommassa’s van calcium, chloor en zuurstof op te tellen die aanwezig zijn in een molecuul Ca(ClO)2. Het molecuulgewicht van Ca(ClO)2 is een belangrijke parameter die wordt gebruikt bij verschillende chemische berekeningen.
Structuur van calciumhypochloriet
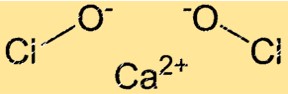
Ca(ClO)2 heeft een kristallijne structuur. Het Ca(ClO)2-kristalrooster is samengesteld uit Ca+2-ionen en ClO-ionen. De ClO-ionen zijn gerangschikt in een tetraëdrische geometrie rond de Ca+2-ionen. De kristalroosterstructuur van Ca(ClO)2 geeft het zijn sterke oxiderende eigenschappen.
Oplosbaarheid van calciumhypochloriet
Ca(ClO)2 is zeer goed oplosbaar in water. Het lost op in water en vormt een hypochlorietion en een calciumion. De oplosbaarheid van Ca(ClO)2 in water neemt toe bij toenemende temperatuur. Ca(ClO)2 is ook oplosbaar in organische oplosmiddelen zoals aceton en ethanol.
| Verschijning | Witte kristallijne vaste stof |
| Soortelijk gewicht | 2.35 |
| Kleur | Wit |
| Geur | Chloor geur |
| Molaire massa | 142,98 g/mol |
| Dikte | 2,35 g/cm³ |
| Fusie punt | 100°C |
| Kookpunt | Breekt af voordat het kookt |
| Flitspunt | Niet toepasbaar |
| oplosbaarheid in water | 21g/100ml (20°C) |
| Oplosbaarheid | Oplosbaar in aceton, ethanol, glycerol en water |
| Dampdruk | Niet toepasbaar |
| Dampdichtheid | Niet toepasbaar |
| pKa | 7.5 |
| pH | ~11 |
Veiligheid en gevaren van calciumhypochloriet
Ca(ClO)2 kan gevaarlijk zijn als er niet op de juiste manier mee wordt omgegaan. Het is een krachtig oxidatiemiddel dat heftig kan reageren met organische verbindingen, waarbij giftige gassen vrijkomen. Het kan huid- en oogirritatie veroorzaken en langdurige blootstelling kan leiden tot ademhalingsproblemen. Het moet worden bewaard op een koele, droge en goed geventileerde plaats, uit de buurt van organisch materiaal, reductiemiddelen en zuren. Er moet voorzichtig met Ca(ClO)2 worden omgegaan en bij het hanteren ervan moet beschermende uitrusting, zoals handschoenen en een veiligheidsbril, worden gedragen. Het mag niet worden gemengd met andere chemicaliën, inclusief zuren of reductiemiddelen, omdat dit een explosie kan veroorzaken.
| Gevarensymbolen | O, Xi, N |
| Beveiligingsbeschrijving | Schadelijk bij inslikken, veroorzaakt huidirritatie, veroorzaakt ernstige oogirritatie, kan kanker veroorzaken |
| VN-identificatienummers | VN1748 |
| HS-code | 2828.90.00 |
| Gevarenklasse | 5.1 (Oxidatiemiddelen) |
| Verpakkingsgroep | II |
| Toxiciteit | LD50 (oraal, rat) = 850 mg/kg; LC50 (inhalatie, rat) = 10,8 mg/m³ (blootstelling van 4 uur) |
Methoden voor de synthese van calciumhypochloriet
Er zijn verschillende methoden om Ca(ClO)2 te synthetiseren.
Eén methode bestaat uit het mengen van chloorgas met gebluste kalk, ook wel calciumhydroxide genoemd, in water. Bij de reactie ontstaan Ca(ClO)2, calciumchloride en water. Een andere methode is het laten reageren van chloorgas met droog calciumhydroxide, wat resulteert in Ca(ClO)2 en waterdamp.
Het grootschalige Ca(ClO)2-productieproces omvat doorgaans de reactie van natriumhypochloriet met calciumchloride , waarbij Ca(ClO)2 en natriumchloride ontstaan.
Een andere methode omvat het laten reageren van calciumcarbonaat met chloorgas in aanwezigheid van water of azijnzuur. De reactie produceert Ca(ClO)2, kooldioxide, water of calciumacetaat en zoutzuur.
Deze methoden vereisen zorgvuldige behandeling en geschikte apparatuur om de veiligheid en effectiviteit te garanderen. De keuze van de werkwijze is afhankelijk van de productieschaal en de gewenste zuiverheid van het eindproduct.
Gebruik van calciumhypochloriet
Ca(ClO)2 heeft een breed scala aan toepassingen vanwege de sterke oxiderende en desinfecterende eigenschappen. Hier zijn enkele veelvoorkomende toepassingen van Ca(ClO)2:
- Waterbehandeling: veel gebruikt voor het desinfecteren van water in zwembaden, drinkwatersystemen en afvalwaterzuiveringsinstallaties.
- Bleekmiddel: Gebruikt als bleekmiddel voor katoen, linnen en papierpulp, maar ook bij de papier- en textielproductie.
- Desinfectie: Veel gebruikt voor het desinfecteren van oppervlakken en apparatuur in de voedingsindustrie.
- Ontgeuring: Wordt gebruikt om onaangename geuren uit stoffen, tapijten en andere materialen te verwijderen.
- Desinfectiemiddel: Effectief desinfectiemiddel voor ziekenhuizen, laboratoria en andere zorginstellingen.
- Algenbestrijding: Wordt gebruikt om de groei van algen in waterlichamen, zoals vijvers en meren, te beheersen.
- Chemische synthese: Gebruikt bij de synthese van verschillende organische en anorganische verbindingen.
- Huishoudelijk gebruik: Gebruikt als huishoudelijk desinfectiemiddel, vooral voor het reinigen en desinfecteren van toiletten en leidingen.
- Boren van oliebronnen: Wordt ook gebruikt bij het boren van oliebronnen om de groei van bacteriën en andere micro-organismen te voorkomen.
Vragen:
Vraag: Kun je calciumhypochloriet gebruiken om een tatoeage te verwijderen?
A: Nee, Ca(ClO)2 mag niet worden gebruikt om een tatoeage te verwijderen. Het is een sterk oxidatiemiddel dat ernstige huidbeschadiging en littekens kan veroorzaken.
Vraag: Hoe bewaar ik calciumhypochloriet?
A: Ca(ClO)2 moet worden opgeslagen in een koele, droge, goed geventileerde ruimte, uit de buurt van direct zonlicht, warmtebronnen en onverenigbare stoffen. Het moet worden bewaard in een goed gesloten container en beschermd tegen vocht en water.
Vraag: Waar kan ik calciumhypochloriet kopen?
A: Ca(ClO)2 kan worden gekocht bij chemische toeleveringsbedrijven, zwembadwinkels en online retailers.
Vraag: Hoeveel calciumhypochloriet voor drinkwater?
A: De hoeveelheid Ca(ClO)2 die nodig is voor de drinkwaterbehandeling hangt af van de concentratie van de oplossing en het te behandelen watervolume. De aanbevolen dosering ligt doorgaans tussen 0,2 en 0,5 ppm (parts per million) voor regelmatige desinfectie.
Vraag: Hoeveel calciumhypochloriet kan ik veilig innemen?
A: Ca(ClO)2 mag nooit worden ingenomen, omdat het zeer giftig is en ernstige gezondheidsproblemen of zelfs de dood kan veroorzaken.
Vraag: Waterzuivering met calciumhypochloriet?
A: Ca(ClO)2 wordt vaak gebruikt voor waterzuivering en desinfectie in verschillende omgevingen, waaronder zwembaden, drinkwatersystemen en afvalwaterzuiveringsinstallaties.
Vraag: Calciumhypochloriet shock?
A: Ca(ClO)2 shock is een proces waarbij een hogere concentratie Ca(ClO)2 aan een zwembad of spa wordt toegevoegd om het chloorgehalte snel te verhogen en schadelijke bacteriën en verontreinigingen te elimineren.
Vraag: Calciumhypochloriet om water te desinfecteren?
A: Ca(ClO)2 is een krachtig desinfectiemiddel dat vaak wordt gebruikt voor waterbehandeling en -zuivering om bacteriën, virussen en andere schadelijke micro-organismen te elimineren.
Vraag: Is Ca(OCl)2 een zuur of een base?
A: Calciumhypochloriet (Ca(OCl)2) is een base omdat het een proton kan accepteren om een hydroxide-ion te vormen.
Vraag: Welke gereduceerde vorm van Ca(OCl)2 blijft er over aan het einde van het experiment?
A: De gereduceerde vorm van Ca(OCl)2 die overblijft aan het einde van een experiment hangt af van de specifieke reactie die plaatsvindt. In sommige gevallen kan het calciumchloride (CaCl2) of calciumcarbonaat (CaCO3) zijn.
