Le nitrate d’argent (AgNO3) est un composé chimique composé d’argent, d’azote et d’oxygène. Il est couramment utilisé en photographie, en médecine et comme réactif de laboratoire pour diverses réactions.
| Nom UICPA | Nitrate d’argent |
| Formule moléculaire | AgNO3 |
| Numero CAS | 7761-88-8 |
| Synonymes | Mononitrate d’argent, sel d’argent (1+) d’acide nitrique, nitrate d’argent (I) |
| InChI | InChI=1S/Ag.NO3/c;2-1(3)4/q+1;-1 |
Propriétés du nitrate d’argent
Formule au nitrate d’argent
La formule du mononitrate d’argent est AgNO3. Il se compose d’un atome d’argent (Ag), d’un atome d’azote (N) et de trois atomes d’oxygène (O). La formule représente le rapport des atomes dans une molécule de mononitrate d’argent.
Nitrate D’argent Masse molaire
La masse molaire du mononitrate d’argent est calculée en additionnant les masses atomiques de ses éléments constitutifs. L’argent a une masse atomique de 107,87 g/mol, l’azote a une masse de 14,01 g/mol et chaque atome d’oxygène a une masse de 16,00 g/mol. Leur addition donne une masse molaire d’environ 169,87 g/mol pour le mononitrate d’argent.
Point d’ébullition du nitrate d’argent
Le mononitrate d’argent a un point d’ébullition d’environ 440 degrés Celsius (824 degrés Fahrenheit). A cette température, le composé subit une transition de phase d’un état liquide à un état gazeux. Le point d’ébullition indique la température à laquelle la pression de vapeur de la substance est égale à la pression atmosphérique.
Nitrate d’argent Point de fusion
Le point de fusion du mononitrate d’argent est d’environ 209 degrés Celsius (408 degrés Fahrenheit). C’est la température à laquelle la forme solide du mononitrate d’argent se transforme en liquide. Le point de fusion est une propriété caractéristique d’une substance et permet de déterminer son comportement physique dans différentes conditions.
Densité du nitrate d’argent g/mL
La densité du mononitrate d’argent est d’environ 4,35 g/mL. La densité est une mesure de la quantité de masse contenue dans un volume donné. Il se calcule en divisant la masse d’une substance par son volume. La densité du mononitrate d’argent indique sa compacité ou sa concentration dans un espace spécifique.
Argent Nitrate Poids moléculaire
Le poids moléculaire du mononitrate d’argent, également appelé masse molaire, est d’environ 169,87 g/mol. Il représente la somme des masses atomiques de tous les atomes d’une molécule de mononitrate d’argent. Le poids moléculaire est utilisé dans divers calculs et conversions impliquant des quantités du composé.
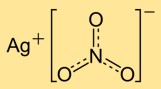
Structure du nitrate d’argent
Le mononitrate d’argent a une structure cristalline composée de cations d’argent (Ag+) et d’anions nitrate (NO3-). Les ions argent sont entourés d’ions nitrate, formant un réseau régulier. Cette structure ionique contribue à la stabilité et aux propriétés du composé.
Solubilité du nitrate d’argent
Le mononitrate d’argent est très soluble dans l’eau. Il se dissout facilement dans l’eau pour former une solution claire et incolore. La solubilité du mononitrate d’argent dans l’eau est une caractéristique essentielle et joue un rôle crucial dans diverses applications, comme en médecine, en photographie et dans les réactions chimiques.
| Apparence | Solide cristallin blanc |
| Gravité spécifique | 4,35 g/ml |
| Couleur | Incolore |
| Odeur | Inodore |
| Masse molaire | 169,87 g/mole |
| Densité | 4,35 g/ml |
| Point de fusion | 209 °C (408 °F) |
| Point d’ébullition | 440 °C (824 °F) |
| Point d’éclair | N’est pas applicable |
| Solubilité dans l’eau | Soluble |
| Solubilité | Soluble dans l’eau et les solvants organiques tels que l’éthanol |
| Pression de vapeur | 0,26 mmHg à 25 °C (77 °F) |
| Densité de vapeur | N’est pas applicable |
| pKa | – |
| pH | Acide (environ pH 5-6 en solution aqueuse) |
Sécurité et dangers du nitrate d’argent
Le mononitrate d’argent présente certains risques pour la sécurité et des précautions doivent être prises lors de la manipulation du composé. Il est considéré comme nocif s’il est ingéré, inhalé ou s’il entre en contact avec la peau ou les yeux. Des mesures de protection telles que des gants, des lunettes de sécurité et des blouses de laboratoire doivent être utilisées. Cela peut provoquer des irritations, des brûlures et des taches sur la peau et d’autres surfaces. Lorsqu’il est chauffé, il peut libérer des oxydes d’azote toxiques. Il doit être conservé dans un endroit frais et sec, à l’écart des substances incompatibles. Les déversements doivent être nettoyés rapidement et l’élimination des déchets doit suivre les directives appropriées pour éviter la contamination de l’environnement.
| Symboles de danger | Corrosif, Comburant |
| Description de la sécurité | Provoque de graves brûlures de la peau et des lésions oculaires. |
| Identifiants des Nations Unies | UN 1493 (Mononitrate d’argent solide) |
| Code HS | 2843.10.00 |
| Classe de danger | Classe 5.1 (Matières comburantes) |
| Groupe d’emballage | GE II (intermédiaire) |
| Toxicité | Toxique pour la vie aquatique avec des effets à long terme. |
Méthodes de synthèse du nitrate d’argent
Il existe différentes méthodes pour synthétiser le mononitrate d’argent.
Une méthode courante implique la réaction entre l’argent métallique et l’acide nitrique . Dans ce processus, l’acide nitrique dilué dissout l’argent pour produire du mononitrate d’argent. Une autre méthode implique la réaction de l’oxyde d’argent ou du carbonate d’argent avec de l’acide nitrique, entraînant la formation de mononitrate d’argent.
De plus, la réaction entre le chlorure d’argent et l’acide nitrique peut également produire du mononitrate d’argent. L’acide nitrique dissout le chlorure d’argent, déplaçant les ions chlorure et formant du mononitrate d’argent.
De plus, la réaction du sulfate d’argent avec un sel nitrate soluble, comme le nitrate de sodium, permet l’acquisition de mononitrate d’argent. Le sulfate d’argent réagit avec le sel nitrate dans une solution aqueuse, conduisant à la formation de mononitrate d’argent et d’un sel sulfate soluble.
Lors de la mise en œuvre de ces méthodes de synthèse, il est important de prendre des mesures de sécurité appropriées et d’utiliser des acides corrosifs et des composés potentiellement toxiques. Il convient également de suivre les protocoles et les directives du laboratoire pour garantir une préparation et une manipulation précises du mononitrate d’argent.
Utilisations du nitrate d’argent
Le mononitrate d’argent a de nombreuses utilisations dans différents domaines. Voici quelques applications courantes :
- Photographie : La photographie traditionnelle en noir et blanc utilise du mononitrate d’argent comme composé sensible à la lumière qui réagit avec la lumière, formant des particules d’argent et développant des images photographiques.
- Médecine : Les applications médicales utilisent le mononitrate d’argent pour ses propriétés antiseptiques dans le soin des plaies. Son application topique prévient les infections, stimule la guérison et traite les brûlures, les ulcères et autres plaies cutanées.
- Réactif de laboratoire : Le mononitrate d’argent sert de réactif de laboratoire polyvalent, permettant diverses réactions chimiques et étant utilisé en chimie analytique pour détecter la présence d’halogénures et d’autres composés.
- Placage d’argent : les processus de galvanoplastie utilisent du mononitrate d’argent pour déposer activement une fine couche d’argent sur différentes surfaces. Cette utilisation est courante à des fins décoratives et pour assurer la résistance à la corrosion.
- Coloration et teinture : L’histologie et la microscopie utilisent le mononitrate d’argent comme colorant pour améliorer activement la visibilité de structures spécifiques dans les échantillons biologiques. L’industrie textile l’utilise pour teindre les tissus.
- Gravure : La nature corrosive du mononitrate d’argent permet son utilisation active dans la gravure de motifs sur le verre et les miroirs. Il supprime sélectivement les couches de surface, créant ainsi des motifs complexes.
- Enseignement de la chimie : les établissements d’enseignement utilisent activement le mononitrate d’argent pour réaliser des expériences et des démonstrations chimiques, en raison de ses réactions et effets visuels distincts.
- Catalyseur d’argent : Dans certaines réactions chimiques, le mononitrate d’argent agit activement comme un catalyseur, facilitant la conversion des réactifs en produits souhaités.
Des questions:
Q : AgNO3 est-il soluble dans l’eau ?
R : Oui, AgNO3 est soluble dans l’eau.
Q : Qu’est-ce que l’AgNO3 ?
R : AgNO3 est du mononitrate d’argent, un composé chimique composé d’argent, d’azote et d’oxygène.
Q : Quels sont les ions spectateurs dans la réaction entre KCl(aq) et AgNO3(aq) ?
R : Dans la réaction entre KCl(aq) et AgNO3(aq), les ions spectateurs sont K+ et NO3-.
Q : Quels ions, le cas échéant, sont des ions spectateurs dans la réaction AgNO3(aq) + NaCl(aq) → AgCl(s) + NaNO3(aq) ?
R : Dans la réaction AgNO3(aq) + NaCl(aq) → AgCl(s) + NaNO3(aq), les ions spectateurs sont Na+ et NO3-.
Q : Combien de moles de Cu sont nécessaires pour réagir avec 5,8 moles d’AgNO3 ?
R : L’équation équilibrée est nécessaire pour déterminer le nombre de moles de Cu nécessaires pour réagir avec 5,8 moles d’AgNO3.
Q : Lequel des composés suivants produira un précipité avec AgNO3 ?
R : Les composés contenant des ions Cl-, Br- ou I- produiront un précipité avec AgNO3.
Q : AgNO3 est-il un composé ionique ?
R : Oui, AgNO3 est un composé ionique.
Q : AgNO3 est-il un électrolyte puissant ?
R : Oui, AgNO3 est un électrolyte puissant.
Q : AgNO3 conduit-il l’électricité ?
R : Oui, AgNO3 conduit l’électricité lorsqu’il est dissous dans l’eau.
Q : Le nitrate d’argent est-il un sel ?
R : Oui, le mononitrate d’argent est un sel.
Q : Puis-je acheter du nitrate d’argent ?
R : Oui, le mononitrate d’argent est disponible dans le commerce à l’achat.
Q : Le nitrate d’argent est-il une solution ?
R : Le mononitrate d’argent peut exister sous forme solide ou sous forme de solution, selon son état.
Q : Comment enlever la tache de nitrate d’argent ?
R : Les taches de mononitrate d’argent peuvent être éliminées en traitant la zone affectée avec un agent réducteur doux, tel que le peroxyde d’hydrogène ou le thiosulfate de sodium.
Q : Le nitrate d’argent est-il soluble dans l’eau ?
R : Oui, le mononitrate d’argent est soluble dans l’eau.
Q : Quel précipité se forme lorsque des solutions de nitrate d’argent et de chromate de potassium sont mélangées ?
R : Lorsque des solutions de mononitrate d’argent et de chromate de potassium sont mélangées, un précipité jaune de chromate d’argent (Ag2CrO4) se forme.
Q : Quelle est la masse molaire du nitrate d’argent ?
R : La masse molaire du mononitrate d’argent (AgNO3) est d’environ 169,87 g/mol.
Q : De l’argent métallique est ajouté à une solution de nitrate de plomb (II). Quelle est la réaction chimique équilibrée ?
R : La réaction chimique équilibrée est 2Ag + Pb(NO3)2 → 2AgNO3 + Pb.
