암모니아란 무엇입니까?
암모니아 또는 NH3는 질소와 수소로 구성된 무색의 자극성 가스로 업계에서 냉매, 세척제, 비료로 널리 사용됩니다.
| IUPAC 이름 | 암모니아 |
| 분자식 | NH3 |
| CAS 번호 | 7664-41-7 |
| 동의어 | 아잔, 삼수소화질소, 하트쇼른 알코올 |
| 인치 | InChI=1S/NH3/c1-2 |
암모니아의 성질
암모니아의 루이스 구조
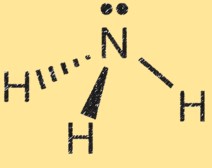
암모니아(NH3)의 루이스 구조는 분자 내 전자 배열을 보여줍니다. 루이스 구조에서 점은 전자를 나타내고 선은 원자 사이의 결합을 나타냅니다.
암모니아의 루이스 구조는 세 개의 수소 원자와 질소와 수소 원자 사이에 공유되는 한 쌍의 전자로 둘러싸인 질소 원자를 보여줍니다. 이는 분자의 공유 결합을 나타냅니다. 질소 원자에는 5개의 원자가 전자가 있고, 수소 원자에는 각각 1개의 원자가 전자가 있습니다. 암모니아의 루이스 구조에서 질소 원자는 수소 원자와 3개의 단일 결합을 형성하고 하나의 비공유 전자쌍을 갖습니다.
암모니아 공식
암모니아의 화학식은 NH3입니다. 이 공식은 각 암모니아 분자에 3개의 수소 원자와 1개의 질소 원자가 있음을 나타냅니다. 공식은 물질의 구성을 나타내며 물질의 특성과 거동에 대한 중요한 정보를 제공합니다.
NH3 몰 질량
물질의 몰질량은 물질 1몰의 질량이며, 몰당 그램으로 표시됩니다. 암모니아(NH3)의 몰 질량은 17.0307 g/mol입니다. 이는 암모니아 1몰의 질량이 17.0307g임을 의미합니다. 물질의 몰 질량은 주어진 샘플의 몰 수를 결정하는 데 중요하며 화합물의 공식 질량을 결정하는 데 사용될 수 있습니다.
암모니아의 끓는점
NH3의 끓는점은 -33.34°C(-28.012°F)입니다. 물질의 끓는점은 증기압이 대기압과 같아지고 액체에서 기체로 변하기 시작하는 온도입니다. NH3의 끓는점은 다른 화학물질에 비해 상대적으로 낮기 때문에 냉각 및 냉동 시스템에 유용한 냉매입니다.
NH3 녹는점
NH3의 녹는점은 -77.73°C(-107.87°F)입니다. 물질의 녹는점은 고체에서 액체로 변하는 온도입니다. NH3의 낮은 융점은 가스에서 액체로 쉽게 응축될 수 있고 상태가 변할 때 열을 흡수할 수 있기 때문에 유용한 냉매로 만듭니다.
NH3 밀도 g/ml
물질의 밀도는 단위 부피당 샘플의 질량입니다. NH3의 밀도는 0.769g/mL입니다. 이는 NH3 1밀리리터의 질량이 0.769g이라는 것을 의미합니다. 물질의 밀도는 주어진 부피에 존재하는 물질의 양을 결정하는 데 사용될 수 있으며 물질이 다양한 상태에서 어떻게 행동하는지 이해하는 데 중요한 특성입니다.
NH3 분자량
물질의 분자량은 물질의 단일 분자에 포함된 모든 원자의 원자량의 합입니다. NH3(NH3)의 분자량은 17.0307g/mol입니다. 이는 NH3 분자의 분자량이 몰당 17.0307g임을 의미합니다. 물질의 분자량은 주어진 샘플의 몰수를 결정하는 데 중요하며 화합물의 공식 질량을 결정하는 데 사용될 수 있습니다.
NH3 구조
NH3는 수소 원자 3개와 질소 원자 1개로 구성된 분자입니다. 질소 원자는 공유 결합을 통해 수소 원자에 연결되어 있으며 분자는 삼각뿔 모양을 가지고 있습니다. 분자의 결합각은 약 107°입니다. NH3는 극성 분자입니다. 즉, 양극과 음극이 있으며 일반적으로 화학 반응에서 용매 및 시약으로 사용됩니다.
| 모습 | 무색 가스 |
| 비중 | 0.59(공기=1) |
| 색상 | 무색 |
| 냄새가 나다 | 자극적이고 강한 냄새 |
| 몰 질량 | 17.0307g/몰 |
| 밀도 | 0.769g/mL |
| 융합점 | -77.73°C |
| 비점 | -33.34°C |
| 플래시 도트 | 해당 없음(가스) |
| 물에 대한 용해도 | 매우 용해성 |
| 용해도 | 물과 대부분의 유기용매에 용해됨 |
| 증기압 | 20°C에서 50.7kPa |
| 증기 밀도 | 0.59(공기=1) |
| pKa | 4.75 |
| pH | 11.6(포화용액) |
암모니아 안전 및 위험
NH3는 적절하게 취급하지 않을 경우 인체 건강과 환경에 심각한 해를 끼칠 수 있는 독성이 높고 부식성이 높은 가스입니다. NH3는 눈, 피부, 호흡기에 심한 화상을 일으킬 수 있으며, 고농도 흡입 시 치명적일 수도 있습니다. 또한 NH3는 반응성이 매우 높아 특정 화학물질이나 물질과 접촉하면 발화되거나 폭발할 수 있습니다.
NH3를 취급하거나 작업할 때 안전 예방 조치를 취하는 것이 중요합니다. 여기에는 장갑, 고글, 안면 마스크와 같은 보호복을 착용하는 것뿐만 아니라 가스 흡입을 피하기 위해 적절한 환기를 제공하는 것도 포함됩니다. NH3를 열원이나 기타 가연성 물질로부터 멀리 떨어진 통풍이 잘 되는 곳에 보관하는 것도 중요합니다. NH3에 노출된 경우, 오염된 의복을 벗고 해당 부위를 다량의 물로 헹구는 것이 중요합니다. 노출 증상이 나타나면 즉시 의사의 진료를 받으십시오.
| 위험 기호 | T+, N |
| 보안 설명 | 환경에 위험하고 흡입하면 유해하며 자극적입니다. |
| AN 식별자 | 유엔 1005 |
| HS 코드 | 2814.1 |
| 위험등급 | 2.3 |
| 포장그룹 | II |
| 독성 | 독성이 높고 치사량(흡입) – 33-66ppm |
암모니아 합성 방법
암모니아를 합성하는 방법에는 Haber 공정, Ostwald 공정, Birkeland-Eyde 공정 등 여러 가지 방법이 있습니다.
Haber-Bosch 공정으로도 알려진 Haber 공정은 암모니아의 산업적 합성에 가장 널리 사용되는 방법입니다. 이 과정에서 공기 중의 질소 가스는 철 촉매 위에서 수소 가스와 반응하여 암모니아를 형성합니다. 반응은 고압(약 150기압) 및 450~500°C의 온도에서 진행됩니다. Haber 공정은 매우 효율적이며 높은 수율로 대량의 암모니아를 생산하며 비료 및 기타 화학 물질 생산을 위한 주요 암모니아 공급원으로 사용됩니다.
질소 고정 공정으로도 알려진 오스트왈드 공정은 질소 가스를 산화질소로 산화시킨 다음 산화질소와 더 많은 질소 가스를 반응시켜 암모니아를 형성하는 오래된 암모니아 합성 방법입니다. 이 프로세스는 효율성이 떨어지며 Haber 프로세스로 대체되었습니다.
플라즈마 공정이라고도 알려진 Birkeland-Eyde 공정은 플라즈마 방전을 사용하여 질소와 수소 가스를 분리하고 암모니아를 형성하는 새로운 암모니아 합성 방법입니다. 이 공정은 아직 개발 단계에 있어 산업용으로 널리 채택되지는 않았습니다.
요약하면, Haber 공정은 암모니아 합성에 가장 일반적으로 사용되는 방법인 반면, Ostwald 공정과 Birkeland-Eyde 공정은 오래되었거나 덜 널리 사용되는 방법입니다.
암모니아의 용도
암모니아는 산업과 농업에서 광범위하게 사용되는 다용도 화학물질입니다. 암모니아의 주요 용도는 다음과 같습니다.
- 비료 생산: 질소 비료 생산의 주요 성분인 암모니아는 작물 수확량을 늘리고 토양 비옥도를 향상시킵니다.
- 냉동: 산업용 및 가정용 냉동 시스템은 냉장고 및 냉동고를 포함하여 암모니아를 냉매로 사용합니다.
- 청소: 가정용 청소 제품에는 기름기와 먼지를 용해시키는 능력 때문에 암모니아가 포함되어 있는 경우가 많습니다.
- 의약품: 제산제, 기침 시럽 등 다양한 의약품을 생산할 때 암모니아를 원료로 사용합니다.
- 섬유 생산: 섬유 염색 및 인쇄, 합성 섬유 생산에는 암모니아가 사용됩니다.
- 폐기물 처리: 하수 처리장의 폐수 처리 및 악취 제어에는 암모니아를 사용합니다.
- 난연제: 암모니아는 플라스틱, 고무 등의 재료 생산 시 난연제로 작용합니다.
- 석유 및 가스 생산: 석유 및 가스 산업에서는 암모니아를 사용하여 계면활성제 및 항유화제를 포함한 다양한 화학 물질을 생산합니다.
결론적으로, 암모니아는 농업, 냉동, 청소, 의약품, 섬유 생산, 폐기물 처리, 난연제, 석유 및 가스 생산을 포함한 다양한 산업 및 응용 분야에서 광범위하게 사용되는 다용도 화학 물질입니다.
질문:
암모니아는 산인가요, 염기인가요?
암모니아는 염기로 간주됩니다. 수용액에서는 용해되어 수산화물 이온(OH-)을 형성하고 약염기 역할을 합니다. 암모니아는 일반적으로 약 11의 염기성(알칼리성) pH를 갖습니다. 암모니아 용액은 산을 중화하여 염과 물을 형성할 수 있는데, 이는 염기의 특징 중 하나입니다. 화학 반응에서 암모니아는 친핵체로 작용할 수 있으며 암모니아의 파생물이며 아민과 아미드의 특성인 질소-탄소 결합을 포함하는 아미드를 형성하는 반응에 참여할 수 있습니다.
암모니아는 극성인가요?
예, 암모니아는 극성입니다. 이는 3개의 수소 원자로 둘러싸인 중앙 질소 원자를 가진 곡선형 분자 구조를 가지고 있습니다. 이 모양은 영구 쌍극자 모멘트를 생성하며, 쌍극자의 양극 끝은 수소 원자에 위치하고 음극 끝은 질소 원자에 위치합니다. 암모니아의 극성 특성으로 인해 물과 같은 극성 용매에 용해될 수 있는데, 이는 극성 분자의 특성입니다. 암모니아의 극성 특성으로 인해 극성 분자 사이에서 발생하는 일종의 분자간 힘인 수소 결합에도 참여할 수 있습니다. 이러한 수소 결합은 비슷한 크기의 비극성 분자보다 끓는점과 녹는점이 더 높아질 수 있습니다.
