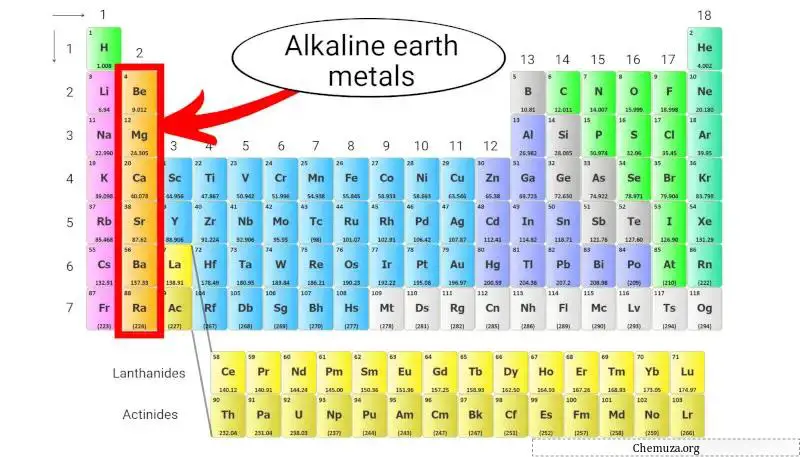
알칼리 토금속은 주기율표 의 두 번째 열에 위치한 원소 그룹입니다. 여기에는 베릴륨 (Be), 마그네슘 (Mg), 칼슘 (Ca), 스트론튬 (Sr), 바륨 (Ba) 및 라듐 (Ra)이 포함됩니다.
이 금속은 가장 바깥 껍질에 두 개의 전자를 가지고 있어 [1] 화학적으로 반응성을 가지지만 첫 번째 열에 있는 알칼리 금속 만큼 반응성은 없습니다.
주기율표의 알칼리 토금속에 대해 더 자세히 살펴보겠습니다.
알칼리 토금속이란 무엇입니까?

알칼리 토금속은 주기율표의 2족에 속하며 두 가지 특별한 특성을 가지고 있습니다.
- 물과 반응하면 본질적으로 알칼리성 또는 염기성인 수산화물을 생성합니다.
- 이들의 산화물 광물(BeO, 마그네사이트, MgO, 베릴 등)은 주로 지각에서 발견되며 열에 안정적입니다.
설명
알칼리 토금속(Mg, Ca, Sr, Ba 및 Ra)이 물과 반응하면 본질적으로 알칼리성(또는 염기성)인 수산화물을 형성합니다. [2]
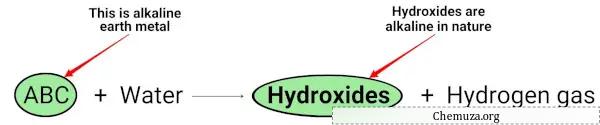
위의 화학 방정식에서 알칼리 금속은 본질적으로 염기성(pH > 7)인 수산화물을 제공하고 수소 가스를 방출한다는 것을 알 수 있습니다.
예를 들어:
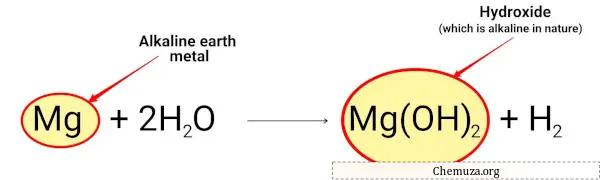
마그네슘은 물과 반응하여 알칼리성인 수산화마그네슘을 형성합니다.
또한 이러한 금속은 주로 지각(산화물)에서 발견되며 이러한 산화된 광물은 열에 안정적입니다. [2]
이 두 가지 기준에 따라 이들 금속에 “알칼리 토금속”이라는 이름이 부여됩니다.
(참고: 2족 원소이기도 한 베릴륨은 물과 반응할 때 알칼리성 용액을 형성하지 않는다는 점에 유의하는 것이 중요합니다. 대신 베릴륨의 수산화물은 양쪽성 거동을 나타내며 이는 산이나 염기처럼 거동할 수 있음을 의미합니다. 따라서 베릴륨은 같은 족에 속하더라도 알칼리토금속으로 간주되지 않습니다.)
모든 알칼리 토금속에 공통적으로 적용되는 것은 무엇입니까?
알칼리 토금속은 몇 가지 공통된 특성을 공유합니다.
예를 들어, 둘 다 가장 바깥쪽 에너지 수준에 두 개의 원자가 전자를 가지고 있어 반응성이 매우 높습니다.
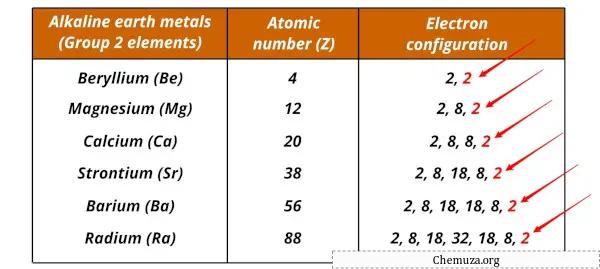
이러한 반응성은 화학 반응 중에 전자를 잃어 +2 전하를 갖는 양이온을 형성하는 경향이 있기 때문입니다.
또한 모든 알칼리 토금속은 반짝이는 은백색 외관을 가지고 있습니다.

이것이 알칼리 토금속의 두 가지 주요 공통점입니다.
알칼리 금속 목록 및 전자 구성
알칼리 토금속과 그 전자 구성은 다음과 같습니다.
| 요소 | 전자 구성 |
| 베릴륨(Be) | [그] 2대 2 |
| 마그네슘(Mg) | [마] 3초 2 |
| 칼슘(Ca) | [Ar] 4s 2 |
| 스트론튬(Sr) | [크르] 5초 2 |
| 바륨(Ba) | [Xe] 6s 2 |
| 라듐(Ra) | [Rn] 7초 2 |
알칼리 토금속의 주기적인 추세
주기율표의 알칼리 토금속족이 아래로 내려갈수록 다음과 같은 경향이 관찰됩니다.
- 원자가 : 모든 알칼리 토금속은 +2의 동일한 원자가를 갖습니다. 따라서 그룹 아래로 내려갈 때 원자가에는 변화가 없습니다.
- 원자 크기: 알칼리 토금속의 원자 크기는 그룹 아래로 내려갈수록 증가합니다. 이는 전자층(또는 궤도 )의 수가 증가하고 내부 전자의 차폐 효과가 핵과 최외각 전자 사이의 인력을 감소시키기 때문입니다.
- 금속 특성: 알칼리 토금속의 금속 특성은 그룹 아래로 내려갈수록 증가합니다. 원자가 더 커지고 더 많은 전자를 포함하게 되어 더 쉽게 전자를 잃고 양이온을 형성할 수 있기 때문입니다.
- 전기 음성도 : 알칼리 토금속의 전기 음성도는 그룹이 내려갈수록 감소합니다. 이는 원자가 더 커지고 더 많은 전자 껍질을 갖게 되어 전자를 끌어당기기가 더 어려워지기 때문입니다.
- 전자 친화력: 알칼리 토금속의 전자 친화력은 일반적으로 낮으며 그룹 아래로 내려갈수록 감소합니다.
- 이온화 에너지: 알칼리 토금속의 이온화 에너지는 족 아래로 내려갈수록 감소합니다. 이는 원자가 클수록 더 많은 전자 껍질을 갖고 가장 바깥쪽 전자가 핵에서 더 멀리 떨어져 있어 제거하기가 더 쉽기 때문입니다.
요약
알칼리 토금속에는 베릴륨, 마그네슘, 칼슘, 스트론튬, 바륨 및 라듐이 포함됩니다. 그들은 가장 바깥 껍질에 두 개의 전자를 가지고 있어 반응성이 있지만 알칼리 금속보다 덜 반응합니다.
이들 금속은 물과 반응할 때 알칼리성 수산화물을 생성하고 열에 안정한 산화 미네랄을 함유하고 있습니다. 모든 알칼리 토금속의 공통적인 주요 특징은 두 개의 원자가 전자를 가지며, 은백색이고 반짝이며, +2 전하를 갖는 양이온을 형성한다는 것입니다.
원자가는 그룹 아래로 이동해도 동일하게 유지되지만 원자 크기와 금속 특성은 증가하는 반면 전기 음성도, 전자 친화력 및 이온화 에너지는 감소합니다.
