아세트산칼슘(Ca(C2H3O2)2)은 칼슘과 아세트산으로 구성된 화합물입니다. 이는 일반적으로 신장 질환이 있는 사람들의 인산염 수치를 낮추는 약물로 사용됩니다.
| IUPAC 이름 | 아세트산칼슘 |
| 분자식 | 칼슘(C2H3O2)2 |
| CAS 번호 | 62-54-4 |
| 동의어 | 아세트산, 칼슘염; 아세트산칼슘(프랑스산); 칼슘디아세테이트; 칼슘에타노에이트; E263 |
| 인치 | InChI=1S/2C2H4O2.Ca/c2 1-2(3)4;/h2 1H3,(H,3,4);/q;;+2/p-2 |
아세트산칼슘의 성질
칼슘 아세테이트 공식
아세트산 칼슘의 공식은 Ca(C2H3O2)2입니다. 이 공식은 1몰의 아세트산 칼슘에 1몰의 칼슘 이온(Ca2+)과 2몰의 아세트산 이온(C2H3O2-)이 포함되어 있음을 나타냅니다. 아세트산 칼슘의 공식은 이 화합물과 관련된 화학 반응의 화학량론을 결정하는 데 필수적입니다.
칼슘 아세트산 몰 질량
Ca(C2H3O2)2의 몰 질량은 158.17 g/mol입니다. 이 값은 Ca(C2H3O2)2 1몰의 질량을 나타내며, 이는 분자량과 같습니다. 몰 질량은 Ca(C2H3O2)2와 관련된 화학 반응의 화학량론을 결정하는 데 중요한 매개변수입니다. 이 값은 Ca(C2H3O2)2 1몰에 존재하는 모든 원자의 원자 질량을 더하여 계산됩니다.
아세트산칼슘의 끓는점
Ca(C2H3O2)2의 끓는점은 160°C(320°F)입니다. 이 값은 Ca(C2H3O2)2가 액체에서 기체로 상태가 변하는 온도를 나타냅니다. Ca(C2H3O2)2의 끓는점은 100°C(212°F)에서 끓는 물의 끓는점보다 상당히 높습니다. 이렇게 높은 끓는점은 Ca(C2H3O2)2의 이온 성질과 강한 분자간 힘에 기인합니다.
아세트산칼슘 녹는점
Ca(C2H3O2)2의 녹는점은 160~170°C(320~338°F)입니다. 이 값은 Ca(C2H3O2)2가 고체에서 액체로 상태가 변하는 온도를 나타냅니다. Ca(C2H3O2)2의 녹는점은 0°C(32°F)에서 녹는 물의 녹는점보다 약간 높습니다. Ca(C2H3O2)2의 높은 융점은 화합물의 이온 특성과 강한 분자간 힘에 기인합니다.
아세트산칼슘의 밀도 g/mL
Ca(C2H3O2)2의 밀도는 1.5g/mL입니다. 이 값은 용액 1밀리리터에 존재하는 Ca(C2H3O2)2의 질량을 나타냅니다. Ca(C2H3O2)2의 밀도는 밀도가 1g/mL인 물의 밀도보다 큽니다. Ca(C2H3O2)2의 높은 밀도는 이온성 특성과 화합물에 칼슘 이온이 존재하기 때문입니다.
아세트산칼슘의 분자량
Ca(C2H3O2)2의 분자량은 158.17g/mol입니다. 이 값은 Ca(C2H3O2)2 분자에 존재하는 모든 원자의 원자량의 합을 나타냅니다. 분자량은 Ca(C2H3O2)2의 특성과 화학 반응에서의 거동을 결정하는 데 중요한 매개변수입니다.
아세트산칼슘의 구조
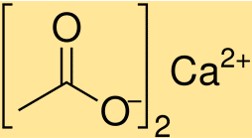
Ca(C2H3O2)2의 구조는 Ca2+ 이온이 두 개의 C2H3O2- 이온으로 둘러싸인 이온 화합물입니다. C2H3O2- 이온은 두자리 리간드 역할을 하며 Ca2+ 이온과 배위 결합을 형성합니다. Ca(C2H3O2)2의 구조는 결정질이며 입방체 모양을 가지고 있습니다.
| 모습 | 백색 결정성 분말 |
| 비중 | 1.5g/ml |
| 색상 | 하얀색 |
| 냄새가 나다 | 냄새 없는 |
| 몰 질량 | 158.17g/몰 |
| 밀도 | 1.5g/ml |
| 융합점 | 160~170°C(320~338°F) |
| 비점 | 160°C(320°F) |
| 플래시 도트 | 해당 없음 |
| 물에 대한 용해도 | 녹는 |
| 용해도 | 물, 에탄올, 아세톤에 용해됨 |
| 증기압 | 해당 없음 |
| 증기 밀도 | 해당 없음 |
| pKa | 9.24 |
| pH | 7-8 (5% 용액) |
아세트산칼슘의 안전성과 위험성
Ca(C2H3O2)2는 일반적으로 지시대로 사용할 때 안전한 것으로 간주됩니다. 그러나 다량의 Ca(C2H3O2)2에 노출되면 피부, 눈, 호흡기에 자극을 줄 수 있습니다. Ca(C2H3O2)2를 다량 섭취하면 배탈, 구토, 설사를 유발할 수 있습니다. Ca(C2H3O2)2를 주의해서 취급하고 물질을 흡입하거나 섭취하지 않는 것이 중요합니다. Ca(C2H3O2)2는 또한 환경, 특히 수생생물에 위험을 초래할 수 있으므로 적절하게 폐기해야 합니다. 모든 화학물질과 마찬가지로 Ca(C2H3O2)2를 취급할 때는 라벨의 안전 지침을 읽고 준수하며 적절한 보호 장비를 사용하는 것이 중요합니다.
| 위험 기호 | 없음 |
| 보안 설명 | 흡입, 섭취, 피부 및 눈 접촉을 피하십시오. 통풍이 잘되는 곳에서 사용하고 적절한 보호 장비를 착용하십시오. |
| UN 식별 번호 | 해당 없음 |
| HS 코드 | 291529 |
| 위험 등급 | OSHA 위험 통신(29 CFR 1910.1200)에 따라 유해 물질로 분류되지 않습니다. |
| 포장그룹 | 해당 없음 |
| 독성 | 낮은 독성. 피부와 눈에 자극을 일으킬 수 있습니다. 다량 섭취시 위장장애를 일으킬 수 있습니다. |
아세트산칼슘의 합성 방법
Ca(C2H3O2)2를 합성하는 데에는 다양한 방법이 사용될 수 있습니다.
일반적인 방법은 탄산칼슘 과 아세트산의 반응을 포함합니다. 탄산칼슘을 아세트산 용액에 첨가하고 혼합물을 가열하여 환류시킨다. 혼합물을 여과하고 여액을 식힌 후 결정화하여 Ca(C2H3O2)2를 형성합니다.
또 다른 방법은 수산화칼슘과 아세트산 의 반응을 포함합니다. 아세트산 용액에 수산화칼슘을 첨가합니다. 혼합물을 저어주고 가열하여 투명한 용액을 얻습니다. 용액을 여과하고 여액을 식힌 후 결정화하여 Ca(C2H3O2)2를 형성합니다.
또 다른 방법은 산화칼슘 과 아세트산 의 반응을 포함합니다. 아세트산 용액에 산화칼슘을 첨가합니다. 혼합물을 저어주고 가열하여 투명한 용액을 얻습니다. 용액을 여과하고 여액을 식힌 후 결정화하여 Ca(C2H3O2)2를 형성합니다.
합성 방법의 선택은 원하는 생성물 수율 및 순도뿐만 아니라 Ca(C2H3O2)2가 사용될 특정 용도와 같은 요인에 따라 달라질 수 있습니다.
칼슘 아세트산의 용도
Ca(C2H3O2)2는 다양한 분야에서 여러 가지 용도로 사용됩니다. Ca(C2H3O2)2의 일반적인 용도는 다음과 같습니다.
- 식품 첨가물: 질감을 개선하고 유통 기한을 연장하기 위해 특히 구운 식품에 식품 첨가물로 사용됩니다.
- 약용 응용: 만성 신장 질환 환자의 높은 혈중 인산염 수치를 치료하기 위한 약으로 사용됩니다. 이는 음식에서 발견되는 인산염과 결합하여 신체에 흡수되는 것을 방지함으로써 작동합니다.
- 수처리: 납 및 기타 중금속의 수준을 줄이기 위해 수처리에 사용됩니다.
- 실험실 시약: 실험실에서 다양한 화학 반응을 위한 시약으로 사용됩니다.
- 항진균제: 특정 피부 감염 치료에 항진균제로도 사용됩니다.
- 콘크리트 가속기: 콘크리트 가속기로 사용되어 콘크리트 설정 과정의 속도를 높이는 데 도움이 됩니다.
- 난연제 : 플라스틱, 섬유 등 다양한 소재의 난연제로 사용됩니다.
질문:
Q: 아세트산칼슘은 산성인가요, 염기성인가요, 아니면 중성인가요?
A: Ca(C2H3O2)2는 염기성 화합물입니다.
Q: 아세트산칼슘은 물에 용해되나요?
A: 네, Ca(C2H3O2)2는 물에 용해됩니다.
Q: 아세트산칼슘을 만드는 방법은 무엇입니까?
A: Ca(C2H3O2)2는 탄산칼슘이나 수산화칼슘을 아세트산과 반응시키는 등 다양한 방법으로 만들 수 있습니다. 이어서 생성된 혼합물을 여과하고 여액을 냉각시킨 후 결정화시켜 Ca(C2H3O2)2를 형성합니다.
Q: 아세트산칼슘은 어디서 구입하나요?
A: Ca(C2H3O2)2는 화학물질 공급업체, 실험실 용품점, 온라인 소매점에서 구입할 수 있습니다.
Q: 아세트산칼슘은 이온성입니까, 공유성입니까?
A: Ca(C2H3O2)2는 칼슘 양이온과 아세테이트 음이온이 이온 결합으로 결합된 이온 화합물입니다.
