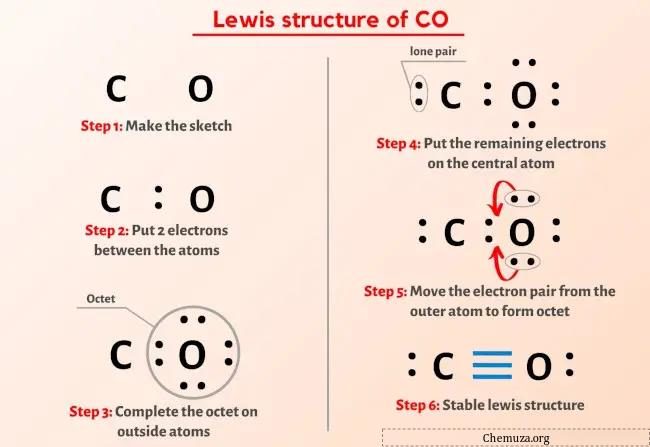
그럼 위 이미지는 이미 보셨죠?
위의 이미지를 간단히 설명하겠습니다.
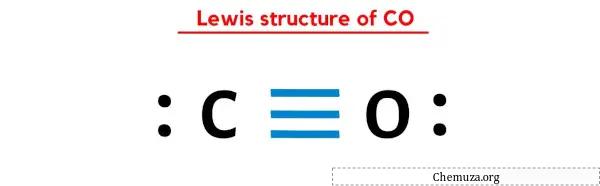
CO 루이스 구조는 탄소(C) 원자와 산소(O) 원자 사이에 삼중결합이 존재하는 구조입니다. 탄소(C) 원자와 산소(O) 원자에는 고립전자쌍이 1개 있습니다.
위의 CO 루이스 구조(일산화탄소) 이미지에서 아무것도 이해하지 못했다면 저와 함께 있으면 CO 루이스 구조를 그리는 방법에 대한 자세한 단계별 설명을 얻을 수 있습니다.
이제 CO의 루이스 구조를 그리는 단계로 넘어가겠습니다.
CO 루이스 구조를 그리는 단계
1단계: CO 분자의 총 원자가 전자 수 찾기
CO(일산화탄소) 분자 의 총 원자가 전자 수를 찾으려면 먼저 단일 탄소 원자 와 산소 원자에 존재하는 원자가 전자를 알아야 합니다.
(가전자는 모든 원자의 가장 바깥쪽 궤도 에 존재하는 전자입니다.)
여기에서는 주기율표를 이용하여 탄소와 산소의 원자가전자를 쉽게 찾는 방법을 알려드리겠습니다.
CO 분자의 총 원자가 전자
→ 탄소 원자에 의해 주어진 원자가 전자:
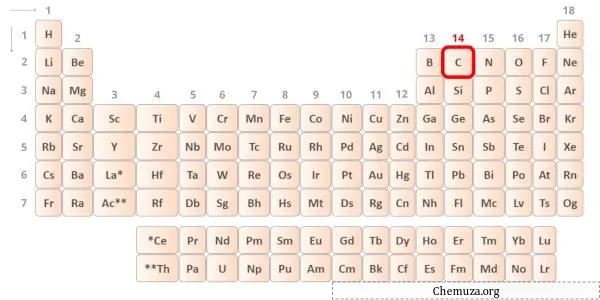
탄소 는 주기율표 14족에 속하는 원소이다. [1] 따라서 탄소에 존재하는 원자가 전자는 4 입니다.
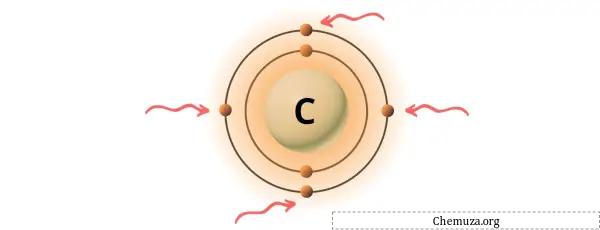
위 이미지와 같이 탄소 원자에 존재하는 4개의 원자가 전자를 볼 수 있습니다.
→ 산소 원자에 의해 주어진 원자가 전자:

산소 는 주기율표 16족의 원소이다. [2] 따라서 산소에 존재하는 원자가 전자는 6 입니다.
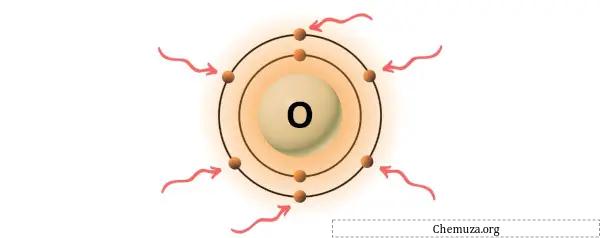
위 이미지와 같이 산소 원자에 존재하는 6개의 원자가 전자를 볼 수 있습니다.
그래서,
CO 분자의 총 원자가 전자 = 1개의 탄소 원자가 제공하는 원자가 전자 + 1개의 산소 원자가 제공하는 원자가 전자 = 4 + 6 = 10 .
2단계: 중심 원자 선택
중심 원자를 선택하려면 전기 음성도 가 가장 낮은 원자가 중심에 남아 있다는 것을 기억해야 합니다.
여기서 주어진 분자는 CO(일산화탄소)입니다. 두 개의 원자만 있으므로 그 중 하나를 중심 원자로 선택할 수 있습니다.

탄소 원자가 중심 원자라고 가정합니다.
(가장 전기 음성도가 낮은 원자를 중심 원자로 간주해야 합니다).
3단계: 각 원자 사이에 전자쌍을 배치하여 각 원자를 연결합니다.
이제 CO 분자에서 탄소 원자(C)와 산소 원자(O) 사이에 전자쌍을 배치해야 합니다.

이는 CO 분자 내에서 탄소(C) 원자와 산소(O) 원자가 화학적으로 결합되어 있음을 나타냅니다.
4단계: 외부 원자를 안정하게 만듭니다. 나머지 원자가 전자쌍을 중심 원자에 놓습니다.
이 단계에서는 외부 원자의 안정성을 확인해야 합니다.
여기 CO 분자 다이어그램에서 우리는 탄소 원자가 중심 원자라고 가정했습니다. 따라서 산소는 외부 원자입니다.
그래서 산소 원자를 안정하게 만들어야 합니다.
아래 이미지에서 산소 원자가 옥텟을 형성하여 안정적이라는 것을 볼 수 있습니다.
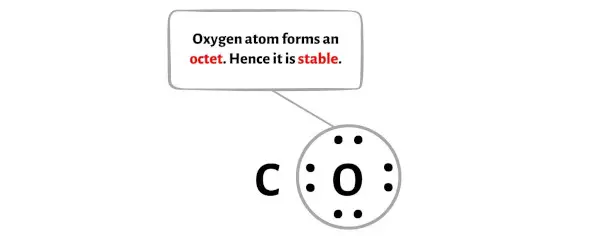
또한 1단계에서는 CO 분자에 존재하는 총 원자가 전자 수를 계산했습니다.
CO 분자에는 총 10개의 원자가 전자가 있으며 이 중 8개의 원자가 전자 만이 위 다이어그램에 사용되었습니다.
따라서 남은 전자의 수 = 10 – 8 = 2 .
위의 CO 분자 다이어그램에 있는 탄소 원자에 이 2개의 전자를 배치해야 합니다.

이제 다음 단계로 넘어가겠습니다.
5단계: 중심 원자의 옥텟을 확인합니다. 옥텟이 없으면 고립전자쌍을 이동하여 이중결합이나 삼중결합을 형성하세요.
이 단계에서는 중심 탄소원자(C)가 안정적인지 여부를 확인해야 합니다.
이 탄소(C) 원자의 안정성을 확인하기 위해서는 옥텟을 형성하는지 여부를 확인해야 한다.
불행하게도 이 탄소 원자는 여기서 옥텟을 형성하지 않습니다. 탄소는 전자가 4개밖에 없어 불안정합니다.

이제 이 탄소 원자를 안정하게 만들려면 산소 원자에서 전자쌍을 이동시켜야 합니다.
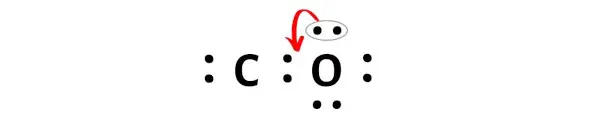
그러나 한 쌍의 전자를 이동시킨 후에도 탄소 원자는 6개의 전자만 갖고 있기 때문에 여전히 옥텟을 형성하지 않습니다.

다시 말하지만, 우리는 산소 원자로부터 여분의 전자쌍을 이동시켜야 합니다.
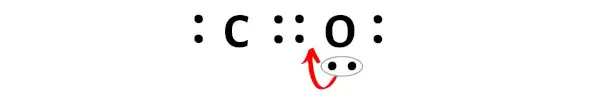
이 전자쌍을 이동시킨 후, 탄소 원자는 2개의 전자를 더 얻게 되어 총 전자는 8개가 됩니다.
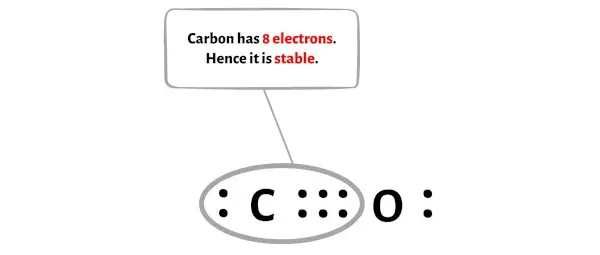
위의 이미지에서 탄소 원자와 산소 원자가 모두 옥텟을 형성하는 것을 볼 수 있습니다.
따라서 CO 분자의 위 루이스 도트 구조는 안정적입니다.
위 CO의 루이스 도트 구조에서는 각 결합전자쌍(:)을 단일결합 (|)으로 나타낼 수도 있습니다. 그렇게 하면 다음과 같은 CO 루이스 구조가 생성됩니다.
위의 모든 단계를 완전히 이해하셨기를 바랍니다.
더 많은 연습과 더 나은 이해를 위해 아래 나열된 다른 루이스 구조를 시도해 볼 수 있습니다.
더 나은 이해를 위해 다음 루이스 구조를 시도해 보세요(또는 적어도 확인하세요).
