황산철(ii)은 철과 황산염 이온을 함유한 화합물입니다. 일반적으로 수처리 및 식물 영양 보충제로 사용됩니다.
| IUPAC 이름 | 철(II) 황산염 |
| 분자식 | FeSO4 |
| CAS 번호 | 7720-78-7 |
| 동의어 | 황산철, 황산철, 녹색 황산철, 멜란테라이트, 쇼몰노카이트 |
| 인치 | InChI=1S/Fe·H2O4S/c;1-5(2,3)4/h;(H2,1,2,3,4)/q+2;/p-2 |
철(ii) 황산염의 성질
철(II) 황산염 공식
황산철(II)의 화학식은 FeSO4입니다. 이 공식은 황산제1철이 철 원자 1개, 황 원자 1개, 산소 원자 4개로 구성되어 있음을 나타냅니다. 황산제1철의 공식은 몰 질량, 분자량 등 화합물의 다양한 물리적, 화학적 특성을 계산하는 데 중요한 매개변수입니다.
철(II) 황산염 몰 질량
황산제1철의 몰 질량은 151.91 g/mol입니다. 이 값은 철 원자 1개, 황 분자 1개, 산소 분자 4개를 포함하는 황산제1철 1몰의 질량을 나타냅니다. 몰 질량은 황산제1철의 밀도, 농도 등 다양한 물리적, 화학적 특성을 계산하는 데 중요한 매개변수입니다.
황산철(II)의 끓는점
황산제일철은 끓는점에 도달하기 전에 분해되기 때문에 특정한 끓는점을 갖지 않습니다. 대기압에서는 약 300°C에서 분해되기 시작합니다. 이 분해에는 물과 삼산화황이 손실되어 산화철(III)이 남게 됩니다. 이러한 분해 거동으로 인해 고온 응용 분야에서 황산제1철의 사용이 제한됩니다.
황산철(II) 녹는점
황산제1철의 녹는점은 수화 정도에 따라 달라집니다. 무수 황산제1철은 695°C에서 녹는 반면, 칠수화물 형태는 64°C에서 녹습니다. 황산제1철은 다양한 수화 형태로 존재할 수 있으며, 각각은 서로 다른 융점을 가지고 있습니다. 황산제1철의 녹는점은 화합물을 준비하고 취급하기 위한 최상의 조건을 결정하는 중요한 매개변수입니다.
철(II) 황산염의 밀도 g/mL
황산제1철의 밀도는 수화 정도에 따라 달라집니다. 무수 황산제1철의 밀도는 3.65g/mL인 반면, 칠수화물 형태의 밀도는 1.897g/mL입니다. 황산제1철의 밀도는 주어진 화합물 질량의 부피를 계산하는 데 중요한 매개변수입니다.
철(II) 황산염 분자량
황산제1철의 분자량은 151.91g/mol입니다. 이 값은 황산제1철 분자를 구성하는 원자의 원자량의 합을 나타냅니다. 분자량은 황산제1철의 끓는점, 용해도 등 다양한 물리적, 화학적 특성을 계산하는 데 중요한 매개변수입니다.
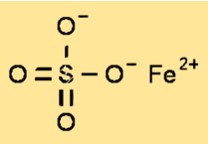
황산철(II)의 구조
황산제일철은 단사정계에 속하는 결정 구조를 가지고 있습니다. 황산제1철의 결정 구조는 6개의 물 분자와 황산염 음이온으로 둘러싸인 철(II) 양이온으로 구성됩니다. 황산제1철의 결정 구조는 화합물의 물리적, 화학적 특성을 이해하는 데 중요한 매개변수입니다.
| 모습 | 백색 또는 연녹색의 결정성 분말 |
| 비중 | 3.65g/cm3(무수물) |
| 색상 | 옅은 녹색 |
| 냄새가 나다 | 냄새 없는 |
| 몰 질량 | 151.91g/몰 |
| 밀도 | 3.65g/cm3(무수), 1.89g/cm3(7수화물) |
| 융합점 | 695°C(무수), 64°C(7수화물) |
| 비점 | 끓는점에 도달하기 전에 분해됨 |
| 플래시 도트 | 해당 없음 |
| 물에 대한 용해도 | 매우 용해성 |
| 용해도 | 물에 용해되고 에탄올에 용해되지 않음 |
| 증기압 | 해당 없음 |
| 증기 밀도 | 해당 없음 |
| pKa | 해당 없음 |
| pH | 4(0.1M 솔루션) |
황산철의 안전성과 위험성 (ii)
황산철은 인간의 건강과 안전에 특정 위험을 초래할 수 있습니다. 접촉 시 피부와 눈에 자극과 발적을 일으킬 수 있으며, 먼지를 흡입하면 기도 자극을 유발할 수 있습니다. 섭취하면 복통, 메스꺼움, 구토, 설사를 유발할 수 있습니다. 또한 황산제1철에 노출되면 취약한 개인에게 직업성 천식과 과민성 폐렴이 발생할 수 있습니다. 적절한 취급 및 보관 절차를 따르고, 적절한 개인 보호 장비를 착용하고, 화합물을 흡입하거나 섭취하지 않는 것이 중요합니다. 사고로 노출된 경우 즉시 의사의 진료를 받고 안전보건자료를 참조하여 조언을 구하십시오.
| 위험 기호 | Xn,N |
| 보안 설명 | 습기, 산, 산화제로부터 멀리 보관하십시오. 피부, 눈, 의복과의 접촉을 피하십시오. 섭취하지 마십시오. 적절한 환기를 통해 사용하십시오. 취급 후에는 손을 철저히 씻으십시오. |
| UN 식별 번호 | UN3077, UN1376 |
| HS 코드 | 2833.29.90 |
| 위험 등급 | 9 (기타 위험물) |
| 포장그룹 | III |
| 독성 | 삼키면 유해하며, 피부와 눈에 자극을 일으키고, 기도 자극을 일으킬 수 있습니다. 흡입이나 피부 접촉으로 인해 감작을 일으킬 수 있습니다. |
철(ii) 황산염의 합성 방법
황산제1철을 합성하는 방법에는 여러 가지가 있습니다.
일반적인 방법은 물과 산소가 있는 상태에서 철 침전물을 황산 과 반응시키는 것입니다. 이는 황산제1철 7수화물 용액을 생성하며, 이는 결정화를 통해 추가로 정제될 수 있습니다.
또 다른 방법은 고온에서 산화철과 황산을 반응시킨 후 생성된 용액을 냉각하고 여과하는 것입니다.
철분말이나 이산화황과 같은 환원제는 황산철(III)을 황산제1철로 환원시킬 수 있습니다. 이로 인해 황산제1철과 황산이 생성됩니다. 황산제1철을 제조하기 위해 철은 물이 있는 상태에서 이산화황 및 산소와 반응할 수 있습니다.
또 다른 방법은 과산화수소 존재 하에서 철을 묽은 황산 과 반응시키는 것입니다. 이로 인해 황산제1철과 물이 생성됩니다.
철(ii) 황산염의 용도
황산철(II)은 다음을 포함하여 다양한 산업 분야에서 광범위하게 응용됩니다.
- 수처리: 물에서 황화수소와 같은 불순물을 제거하기 위해 수처리에 일반적으로 사용됩니다.
- 비료: 식물에 필수 철분 영양소를 제공하기 위해 비료 생산에 사용됩니다.
- 안료 생산: 노란색, 갈색 안료 등 다양한 산화철 안료를 생산하기 위한 전구체로 사용됩니다.
- 영양 보충제: 인간과 동물의 철 결핍성 빈혈을 치료하기 위한 영양 보충제로 사용됩니다.
- 폐수 처리: 인산염 및 기타 오염 물질을 제거하기 위해 폐수 처리에 사용됩니다.
- 잉크 생산: 잉크 생산에 흑화제로 사용됩니다.
- 목재 방부제: 곰팡이 및 곤충 공격으로부터 목재를 보호하기 위해 목재 방부제로 사용됩니다.
- 실험실 시약: 다양한 화학 반응 및 분석에서 실험실 시약으로 사용됩니다.
질문:
황산철은 물에 용해되나요?
A: 황산철이라고도 알려진 황산철은 물에 적당히 용해됩니다.
Q: 황산철(ii) 화합물의 공식은 무엇입니까?
A: 황산제1철의 공식은 FeSO4입니다.
Q: 황산철(ii)의 화학식은 무엇입니까?
A: 황산제1철의 화학식은 FeSO4입니다.
Q: 황산철(ii)에 포함된 황의 비율은 얼마입니까?
A: 황산제1철의 황 함량은 18.5%입니다.
Q: 황산철(ii)은 물에 용해됩니까?
답변: 예, 황산제1철이라고도 알려진 황산철 II는 물에 용해됩니다.
Q: 황산제1철이란 무엇입니까?
A: 황산제1철은 황산제1철의 또 다른 이름으로, 다양한 산업 분야에서 일반적으로 사용되는 화합물입니다.
Q: 황산제1철은 어떤 용도로 사용되나요?
A: 황산제1철은 수처리, 비료생산, 색소생산, 영양보충제, 잉크생산, 목재방부제, 착색시약 등 다양한 용도로 사용됩니다. 실혐실.
