1-부탄올(C4H9OH)은 약간 달콤한 냄새가 나는 무색 알코올입니다. 이는 용매, 유기 합성 및 연료원으로 사용됩니다. 화장품 및 퍼스널 케어 제품에도 사용할 수 있습니다.
| IUPAC 이름 | 부탄-1-올 |
| 분자식 | C4H10O |
| CAS 번호 | 71-36-3 |
| 동의어 | n-부틸알코올, 부탄올, 부틸알코올, 1-부틸알코올, 1-부탄올, 부탄올렌, 부틸렌수화물, 부틸수화물 |
| 인치 | InChI=1S/C4H10O/c1-2-3-4-5/h5H,2-4H2,1H3 |
1-부탄올의 성질
포뮬라 1-부탄올
1-부탄올의 분자식은 C4H10O입니다. 이는 4개의 탄소 원자, 10개의 수소 원자 및 1개의 산소 원자를 포함한다는 것을 의미합니다. 이는 첫 번째 탄소 원자에 수산기(-OH)가 부착된 선형 구조를 가지고 있습니다.
1-부탄올 몰 질량
C4H9OH의 몰 질량은 74.12 g/mol입니다. 이는 C4H9OH 1몰의 무게가 74.12g임을 의미합니다. 몰 질량은 주어진 샘플에 존재하는 물질의 양을 결정하는 데 도움이 되기 때문에 물질의 중요한 특성입니다.
1-부탄올의 끓는점
C4H9OH의 끓는점은 117.7°C(243.9°F)입니다. 이는 이 온도에서 액체에서 기체로 변한다는 것을 의미합니다. C4H9OH의 끓는점은 여분의 탄소 원자의 존재로 인해 에탄올의 끓는점보다 높습니다.
1-부탄올 융점
C4H9OH의 녹는점은 -90.6°C(-131.1°F)입니다. 이는 이 온도에서 고체에서 액체로 변한다는 것을 의미합니다. C4H9OH의 녹는점은 비슷한 분자량을 갖는 부탄산의 녹는점보다 낮습니다.
1-부탄올 밀도 g/ml
C4H9OH의 밀도는 0.81g/mL입니다. 이는 C4H9OH 1밀리리터의 무게가 0.81그램임을 의미합니다. C4H9OH의 밀도는 1g/mL의 밀도를 갖는 물의 밀도보다 낮습니다.
1-부탄올 분자량
C4H9OH의 분자량은 74.12g/mol입니다. 이는 분자식에 있는 모든 원자의 원자량의 합입니다. 분자량은 물질의 물리적, 화학적 특성을 결정하는 데 도움이 되기 때문에 물질의 중요한 특성입니다.
1-부탄올의 구조
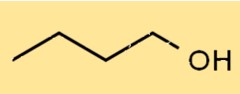
C4H9OH의 구조는 첫 번째 탄소 원자에 수산기(-OH)가 부착된 직쇄 알코올입니다. 그것은 4개의 탄소 원자, 10개의 수소 원자, 1개의 산소 원자로 구성된 선형 구조를 가지고 있습니다. 그 구조로 인해 다른 분자와 수소 결합을 형성할 수 있습니다.
1-부탄올의 용해도
C4H9OH는 물과 유기용매에 용해됩니다. 물에 대한 용해도는 온도가 증가함에 따라 감소합니다. 또한 에탄올이나 메탄올과 같은 극성용매에도 용해됩니다. 벤젠 및 에테르와 같은 유기 용매에서 C4H9OH의 용해도는 물보다 높습니다. 이는 유기 합성의 용매로 유용합니다.
| 모습 | 무색 액체 |
| 비중 | 25°C에서 0.810g/mL |
| 색상 | 무색 |
| 냄새가 나다 | 약간 달콤함 |
| 몰 질량 | 74.12g/몰 |
| 밀도 | 0.81g/ml |
| 융합점 | -90.6°C(-131.1°F) |
| 비점 | 117.7°C(243.9°F) |
| 플래시 도트 | 35°C(95°F) |
| 물에 대한 용해도 | 20°C에서 79g/L |
| 용해도 | 에탄올, 디에틸 에테르, 아세톤, 벤젠, 클로로포름에 용해됨 |
| 증기압 | 20°C에서 1.16kPa |
| 증기 밀도 | 2.55 (공기 대비) |
| pKa | 16.06 |
| pH | 중립 (7) |
1-부탄올의 안전성과 위험성
C4H9OH는 여러 가지 안전 위험을 초래하므로 주의 깊게 처리하는 것이 중요합니다. 열이나 스파크에 노출되면 쉽게 발화할 수 있는 가연성 액체입니다. 또한 눈, 호흡기, 피부에 자극과 손상을 일으킬 수 있는 유해한 증기를 방출합니다. 섭취하면 현기증, 혼란, 혼수상태 등 심각한 건강 문제를 일으킬 수 있습니다. 따라서 C4H9OH를 취급할 때는 장갑, 고글, 호흡기와 같은 보호 장비를 착용하는 것이 필수적입니다. 피부나 눈에 닿은 경우에는 물로 씻어내고 즉시 의사의 진료를 받으세요. 사고를 예방하고 안전을 보장하려면 C4H9OH의 적절한 보관, 취급 및 폐기가 필요합니다.
| 위험 기호 | F, 시 |
| 보안 설명 | 열/스파크/화염/뜨거운 표면으로부터 멀리 보관하십시오. 보호 장갑/보안경/안면 보호구를 착용하십시오. 피부(또는 머리카락)에 묻은 경우: 오염된 모든 의복을 즉시 벗으십시오. 물/샤워로 피부를 헹구십시오. 눈에 들어간 경우: 몇 분간 물로 조심스럽게 씻어내십시오. 가능하다면 콘택트렌즈를 제거하십시오. 계속해서 헹구세요. 혼합할 수 없는 물질로부터 멀리 떨어져 서늘하고 건조하며 통풍이 잘 되는 곳에 보관하십시오. |
| UN 식별 번호 | 유엔 1120 |
| HS 코드 | 2905.16.00 |
| 위험 등급 | 삼 |
| 포장그룹 | III |
| 독성 | LD50(경구, 쥐) 2.46g/kg; LC50(흡입, 쥐) 37,800ppm/4h |
1-부탄올의 합성 방법
C4H9OH는 부티르알데히드 환원, 옥소 가공 또는 발효를 포함한 여러 방법으로 합성될 수 있습니다.
발효는 바이오매스로부터 C4H9OH를 생산하는 일반적인 방법입니다. 발효 과정에서 Clostridium acetottyicum과 같은 미생물은 설탕, 전분 또는 셀룰로오스를 발효시켜 C4H9OH를 포함한 유기산과 알코올의 혼합물을 생성하는 역할을 합니다.
하이드로포밀화라고도 알려진 옥소 공정은 코발트나 로듐과 같은 촉매가 있는 상태에서 프로펜과 일산화탄소 및 수소의 반응을 포함합니다. 부티르알데히드의 수소화는 C4H9OH를 생성합니다. 부티르알데히드가 수소화되면 화합물 C4H9OH가 형성됩니다.
C4H9OH를 합성하는 또 다른 방법은 팔라듐이나 니켈과 같은 촉매 존재 하에서 부티르알데히드를 수소로 환원시키는 것입니다. 이 반응은 부산물로 물과 함께 C4H9OH를 생성합니다.
Fischer-Tropsch 공정은 화석 연료로부터 C4H9OH를 생산하는 방법입니다. 여기에는 촉매를 사용하여 일산화탄소와 수소를 반응시켜 C4H9OH를 포함한 다양한 탄화수소가 생성되는 과정이 포함됩니다.
1-부탄올의 용도
C4H9OH는 고유한 특성으로 인해 다양한 산업 분야에서 다양한 용도로 사용됩니다. C4H9OH의 일반적인 용도는 다음과 같습니다.
- 용제 : 수지, 지방, 오일, 왁스 등 다양한 물질의 용제로 사용됩니다.
- 중간체: 부틸 아크릴레이트 및 부틸 아세테이트와 같은 다른 화학 물질 생산에서 중간체로 사용됩니다.
- 첨가제: 옥탄가를 높이고 배출량을 줄이기 위해 휘발유 및 디젤 연료의 첨가제로 사용됩니다.
- 추출제: 항생제, 비타민, 호르몬 생산 시 추출제로 사용됩니다.
- 화장품 및 개인 관리 제품: 로션, 크림, 향수를 포함한 다양한 화장품 및 개인 관리 제품 생산에 사용됩니다.
- 향료 및 향료: 식품 및 음료 산업에서 향미 및 향 강화제로 사용됩니다.
- 의약품: 진정제, 수면제 등 다양한 의약품 생산에 사용됩니다.
- 살충제: 다양한 살충제와 제초제 생산의 구성 요소로 사용됩니다.
질문:
Q: 부탄올은 극성인가요?
A: 예, 부탄올은 쌍극자 모멘트를 제공하는 수산기(-OH)의 존재로 인해 극성입니다.
Q: 1-부탄올은 물에 용해되나요?
A: 예, C4H9OH는 물 분자와 수소 결합을 형성할 수 있는 하이드록실 그룹의 존재로 인해 물에 부분적으로 용해됩니다.
Q: 1-부탄올에는 수소결합이 있나요?
A: 예, C4H9OH는 다른 C4H9OH 분자 또는 물 분자와 수소 결합을 형성할 수 있는 수산기(-OH)의 존재로 인해 수소 결합을 가지고 있습니다.
Q: 이 용질의 0.350m 수용액 725ml를 제조하려면 몇 ml의 1-부탄올이 필요합니까?
A: 계산에는 74.12 g/mol인 C4H9OH의 몰 질량이 필요합니다. 0.350M C4H9OH 용액을 제조하려면 26.12g의 C4H9OH가 필요합니다. 공식: 몰 = 농도 x 부피를 사용하여 다음과 같이 필요한 C4H9OH의 부피를 계산할 수 있습니다: 부피 = 몰 / 농도. 따라서 0.350m 용액 725ml를 제조하는 데 필요한 C4H9OH의 부피는 (26.12/0.350) = 74.6ml입니다.
Q: 어떤 알코올이 물과 가장 반응이 좋나요? c2h5oh c4h9oh c10h21oh c7h15oh
A: 주어진 옵션 중에서 에탄올(C2H5OH)은 작은 분자 크기와 물 분자와 강한 수소 결합을 형성할 수 있는 수산기 그룹(-OH)의 존재로 인해 물과 가장 유사하게 작용합니다.
Q: c4h9oh의 연소에 대한 균형 방정식의 곱은 무엇입니까?
A: C4H9OH 연소의 균형 방정식은 C4H9OH + 6O2 → 4CO2 + 5H2O입니다. 반응 생성물은 이산화탄소(CO2)와 물(H2O)입니다.
Q: 부탄올(c4h9oh)의 몰 질량은 얼마입니까?
A: 부탄올(C4H9OH)의 몰 질량은 74.12 g/mol입니다.
Q: C4h9oh에는 수소결합이 있나요?
A: 예, C4H9OH는 수산기(-OH)의 존재로 인해 수소 결합을 갖고 있어 다른 C4H9OH 분자 또는 물 분자와 수소 결합을 형성할 수 있습니다.
Q: 2500ml 용액, 즉 2.22m에 몇 그램의 부틸 알코올(c4h9oh)이 들어있나요?
답변: 용액에 들어 있는 부틸 알코올의 그램 수를 계산하려면 다음 공식을 사용해야 합니다: 몰 = 농도 x 부피. 용액의 농도는 2.22moles/L이고 부피는 2.5L(2500ml를 L로 환산)이다. 따라서 용액 내 부틸 알코올의 몰수는 2.22 x 2.5 = 5.55몰입니다. 부틸알코올의 질량을 계산하려면 몰수에 몰질량(74.12 g/mol)을 곱하십시오: 5.55 x 74.12 = 411.4 g. 따라서 2,500ml 용액에는 411.4g, 즉 2.22M의 부틸 알코올이 있습니다.
