트리메틸아민(TMA)은 강한 비린내 냄새가 나는 화합물입니다. 생선, 썩은 생선 제품, 인간의 땀에서 발견됩니다. 이로 인해 구취와 체취가 발생할 수 있습니다.
| IUPAC 이름 | N,N-디메틸메탄아민 |
| 분자식 | C3H9N |
| CAS 번호 | 75-50-3 |
| 동의어 | TMA, 디메틸아민, 메틸디메틸아민, N,N-디메틸아민, 3차 메틸아민, 3차 메틸아민 |
| 인치 | InChI=1S/C3H9N/c1-4(2)3/h1-3H3 |
트리메틸아민의 특성
트리메틸아민 공식
트리메틸아민의 화학식은 C3H9N이며, 이는 분자에 탄소 원자 3개, 수소 원자 9개, 질소 원자 1개가 포함되어 있음을 나타냅니다. 이 공식은 트리메틸아민의 분자량과 기타 특성을 계산하는 데 사용될 수 있습니다.
트리메틸아민 몰 질량
TMA의 몰 질량은 59.11 g/mol입니다. 이 값은 분자에 존재하는 모든 원자의 원자 질량을 더하여 계산됩니다. 몰 질량은 화학적 계산, 특히 물질의 화학량론과 몰수를 결정하는 데 사용되는 중요한 매개변수입니다.
트리메틸아민의 끓는점
TMA의 끓는점은 -6.9°C 또는 19.6°F입니다. 이는 끓는점이 상대적으로 낮기 때문에 화합물이 휘발성이고 쉽게 증발할 수 있음을 의미합니다. TMA는 압력을 가하여 액화할 수 있으며 일반적으로 다양한 응용 분야에서 가스 형태로 사용됩니다.
트리메틸아민 융점
TMA의 녹는점은 -117.3°C 또는 -179.1°F입니다. 이는 녹는점이 매우 낮기 때문에 화합물이 일반적으로 실온에서 액체 또는 기체 상태로 발견된다는 의미입니다. 녹는점 이하의 온도로 냉각하면 응고될 수 있습니다.
트리메틸아민의 밀도 g/mL
TMA의 밀도는 실온에서 0.692g/mL입니다. 이 값은 단위 부피당 TMA의 질량을 결정하는 데 사용됩니다. 화합물의 밀도는 다른 액체에 비해 상대적으로 낮기 때문에 물보다 밀도가 낮습니다.
트리메틸아민 분자량
TMA의 분자량은 59.11g/mol입니다. 이 값은 분자를 구성하는 모든 원자의 원자량의 합입니다. 분자량은 특정 화학 반응이나 과정에 필요한 물질의 양을 계산하는 데 사용됩니다.
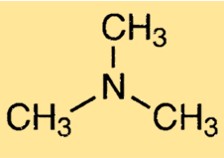
트리메틸아민의 구조
TMA는 질소 원자 주위에 삼각 피라미드 모양의 피라미드 분자 구조를 가지고 있습니다. 분자는 3개의 메틸 그룹에 연결된 중앙 질소 원자를 가지고 있습니다. 질소 원자에는 한 쌍의 비결합 전자가 있는데, 이는 분자의 특징적인 냄새에 영향을 줍니다.
트리메틸아민의 용해도
TMA는 물과 에탄올, 에테르, 아세톤을 포함한 유기용매에 용해됩니다. 물에 대한 TMA의 용해도는 25°C에서 1.8g/100mL입니다. 이 화합물은 극성 특성으로 인해 극성 용매에 잘 용해되므로 다양한 산업 응용 분야에 유용합니다.
| 모습 | 강한 비린내를 지닌 무색의 가스 |
| 비중 | 25°C에서 0.692 |
| 색상 | 무색 |
| 냄새가 나다 | 비린내 냄새가 강함 |
| 몰 질량 | 59.11g/몰 |
| 밀도 | 25°C에서 0.692g/ml |
| 융합점 | -117.3°C 또는 -179.1°F |
| 비점 | -6.9°C(19.6°F) |
| 플래시 도트 | -20°C |
| 물에 대한 용해도 | 녹는 |
| 용해도 | 유기 용매에 용해됨 |
| 증기압 | 20°C에서 542mmHg |
| 증기 밀도 | 25°C에서 2.1 |
| pKa | 9.79 |
| pH | 알칼리성 |
트리메틸아민의 안전성과 위험성
TMA는 주로 가연성이 높고 강한 비린내 냄새로 인해 여러 가지 안전 위험을 초래합니다. 이는 미국 환경 보호국(EPA)을 포함한 여러 규제 기관에 의해 유해 물질로 분류됩니다. TMA에 노출되면 피부와 눈 자극, 호흡기 문제 및 메스꺼움을 유발할 수 있습니다. 또한 다량으로 섭취하거나 흡입하면 독성이 있습니다. TMA를 취급할 때는 적절한 보호 장비를 착용하고 적절한 환기를 보장하는 등 적절한 예방 조치를 취해야 합니다. 노출된 경우 즉시 의료 조치를 받아야 합니다.
| 위험 기호 | 가연성, 부식성 |
| 보안 설명 | 열, 스파크 및 화염으로부터 멀리 보관하십시오. 가스를 흡입하지 마십시오. 적절한 환기가 이루어지는 곳에서만 사용하십시오. 적절한 보호 장비를 착용하십시오. |
| UN 식별 번호 | UN1083 |
| HS 코드 | 29211900 |
| 위험 등급 | 2.1 – 가연성 가스 |
| 포장그룹 | PG I |
| 독성 | 다량으로 삼키거나 흡입하면 유독합니다. 피부와 눈에 자극을 주고 호흡 문제와 메스꺼움을 유발합니다. |
트리메틸아민의 합성 방법
TMA를 합성하는 방법에는 여러 가지가 있지만 가장 일반적인 방법은 수산화칼슘 존재 하에서 포름알데히드 와 염화암모늄 을 반응시키는 것입니다. 우리는 이 과정을 Eschweiler-Clarke 반응으로 알고 있습니다.
또 다른 방법은 디메틸아민을 포름알데히드 와 반응시킨 후 촉매 존재 하에서 수소화시키는 방법입니다. 우리는 이 방법을 Leuckart-Wallach 반응이라고 부릅니다.
프랭클랜드 반응은 암모니아와 트리메틸보레이트의 반응 중에 수산화나트륨 또는 수산화칼륨이 존재할 때 TMA를 생성합니다.
TMA는 요오드화메틸을 암모니아와 반응시킨 후 아연분말로 환원시켜 생산할 수 있습니다. 화학자들은 이 방법을 호프만 분해라고 부릅니다.
TMA를 합성하는 덜 일반적인 다른 방법으로는 트리메틸 포스파이트를 암모니아와 반응시키는 것, TMA 산화물을 산과 반응시키는 것, 트리메틸 알루미늄을 암모니아 와 반응시키는 것 등이 있습니다.
전반적으로, TMA 합성에는 반응성 화학물질과 잠재적으로 위험한 화학물질을 주의 깊게 다루어야 할 뿐만 아니라 유기 화학에 대한 전문 지식도 필요합니다.
트리메틸아민의 용도
TMA는 강하고 뚜렷한 냄새를 비롯한 독특한 화학적 특성으로 인해 다양한 산업 분야에서 여러 용도로 사용됩니다. 다음은 TMA의 가장 일반적인 용도 중 일부입니다.
- 살충제 제조: 클로르피리포스 및 다이아지논을 포함한 여러 살충제 생산에 사용됩니다.
- 유기 합성: 유기 화학자들은 TMA를 널리 사용하여 4차 암모늄 염을 합성합니다. 이는 뛰어난 특성으로 인해 다양한 산업에서 폭넓게 응용됩니다.
- 가스 처리: 천연 가스 및 석유 제품에서 이산화탄소, 황화수소와 같은 산성 가스를 제거하는 데 사용됩니다.
- 제약 산업: 당뇨병 치료제인 메트포르민과 국소 마취제인 프로카인을 포함한 다양한 의약품 생산에 사용됩니다.
- 식품 산업: TMA는 일부 해산물에서 발견되는 비린내를 유발하고 일부 식품에 향미제로서 향미를 더합니다.
- 실험실 연구: 실험실 연구, 주로 단백질 구조 연구에도 사용됩니다.
질문:
Q: 트리메틸아민 염기 공액산(CH3)3N의 화학식은 무엇입니까?
A: TMA의 공액산의 화학식은 (CH3)3NH+입니다.
Q: 0.050M 수성 트리메틸아민의 pH는 11.24입니다. 이 베이스의 KB는 얼마입니까?
A: TMA의 Kb는 용액의 pH(11.24)를 사용하여 계산할 수 있습니다. KB 값은 1.8 x 10^-5입니다.
Q: 물 속 트리메틸아민의 초기 농도는 얼마입니까?
A: 물 속 TMA의 초기 농도는 사용된 특정 용액에 따라 다릅니다. 추가 정보가 없으면 초기 농도를 결정하는 것이 불가능합니다.
Q: 트리메틸아민은 강염기인가요?
A: TMA는 수용액에서 부분적으로만 해리되기 때문에 약염기입니다.
Q: 트리메틸아민은 극성인가요?
A: 예, TMA는 한 쌍의 고립 전자와 3개의 메틸 그룹을 가진 질소 원자의 존재로 인해 극성 분자입니다.
Q: 트리메틸아민은 산인가요, 염기인가요?
A: TMA는 산으로부터 양성자를 받아 짝산을 형성하기 때문에 염기입니다.
Q: 트리메틸아민이 탄소강에 응력 부식 균열을 유발합니까?
A: 예, TMA는 특정 조건에서 탄소강에 응력 부식 균열을 일으킬 수 있습니다.
Q: HPLC에서 트리메틸아민은 무엇에 사용되나요?
A: TMA는 피크 모양과 염기성 화합물의 분리를 개선하기 위해 HPLC에서 이동상 첨가제로 사용됩니다.
Q: 트리메틸아민과 피리딘 중 더 강한 염기는 무엇입니까?
A: 피리딘은 TMA보다 더 강한 염기입니다. 질소 원자가 방향족 고리의 일부이기 때문에 생성된 짝산을 안정화시킵니다.
