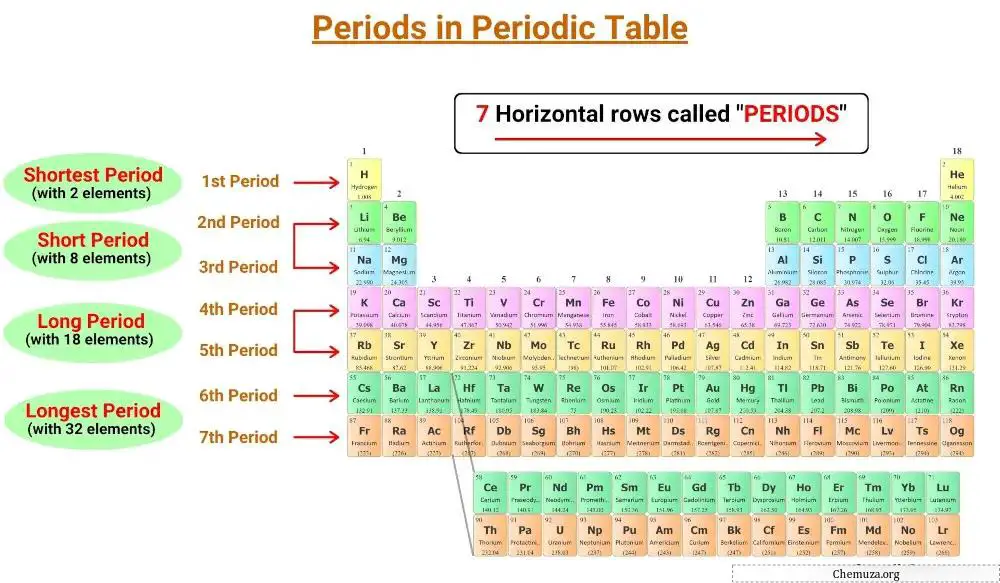
주기율표 의 수평선을 주기라고 하며, 주기율표에는 7개의 주기가 있습니다.
동일한 주기에 위치한 요소는 동일한 수의 전자 레이어를 갖습니다.
주기율표의 기간을 더 자세히 살펴보겠습니다.
주기율표에서 마침표는 무엇입니까?
주기율표에서 점은 왼쪽에서 오른쪽으로 수평으로 연장되는 선입니다.
주기율표는 비슷한 성질을 가진 원소들을 족 또는 족이라 불리는 열로 묶고, 같은 주기의 원소들은 같은 수의 전자껍질을 갖도록 구성되어 있습니다.
주기율표에는 1번부터 7번까지 7개의 주기가 있습니다 . [1]
요소의 껍질 수와 주기 번호
원소의 껍질 수에 따라 주기율표의 주기가 결정됩니다.
예를 들어, 주기 1 원소에는 전자 껍질이 하나만 있고, 주기 2 원소에는 전자 껍질이 두 개 있습니다.
이 조직은 화학자가 주기율표에서의 위치를 기반으로 원소의 특성을 예측하는 데 도움이 됩니다.
기간 요소의 특성
주기율표의 주기를 따라 이동하면 원소의 여러 특성이 예측 가능한 방식으로 변경됩니다. 이는 요소의 특성에서 관찰되는 주기적인 추세 때문입니다.
원자 반경:
일정 기간 동안 왼쪽에서 오른쪽으로 이동하면 일반적으로 원자 반경이 감소합니다. [2]
이는 핵의 양성자 수가 증가하여 핵과 가장 바깥쪽 에너지 준위의 전자 사이에 더 큰 인력을 유발하기 때문입니다. 이로 인해 원자 반경이 더 작아집니다.
전기음성도:
전기 음성도 는 화학 결합에서 자신을 향해 전자를 끌어당기는 원자의 능력을 측정한 것입니다.
일정 기간 동안 왼쪽에서 오른쪽으로 이동하면 일반적으로 전기 음성도가 증가합니다. [삼]
이는 원자 반경이 더 작고 핵의 양전하가 더 강해 음전하를 띤 전자에게 더 매력적이기 때문입니다.
이온화 에너지:
이온화 에너지는 원자에서 전자를 제거하는 데 필요한 에너지의 양입니다.
일정 기간 동안 왼쪽에서 오른쪽으로 이동하면 일반적으로 이온화 에너지가 증가합니다. [4]
이는 원자 반경이 더 작고 전자가 핵에 의해 더 단단히 고정되어 전자를 제거하기가 더 어렵기 때문입니다.
다른 기능들:
녹는점과 끓는점: 일반적으로 일정 기간 동안 왼쪽에서 오른쪽으로 증가하지만 일부 예외가 있습니다.
금속 특성: 비금속 특성이 점점 더 널리 퍼지면서 일정 기간이 지나면서 왼쪽에서 오른쪽으로 감소합니다.
반응성: 전자가 더 단단히 고정되어 화학 반응에 참여할 가능성이 적기 때문에 일정 기간 동안 왼쪽에서 오른쪽으로 이동할 때 요소의 반응성이 낮아집니다.
화학에서 기간의 중요성
주기율표의 주기는 원소의 전자 구성 및 다른 원소와 상호 작용하는 방식에 대한 정보를 제공하기 때문에 원소의 동작을 이해하는 데 필수적입니다. 화학에서 마침표가 중요한 이유는 다음과 같습니다.
- 속성 예측: 주기율표를 통해 과학자들은 주기율표에서의 위치를 기반으로 원소의 속성을 예측할 수 있습니다. 예를 들어, 같은 기간의 원소는 동일한 수의 전자 껍질을 갖고 있어 원자 크기, 반응성 및 기타 특성을 예측하는 데 도움이 될 수 있습니다.
- 추세 식별: 주기율표의 원소 배열을 통해 과학자들은 해당 속성의 추세를 식별할 수 있습니다. 예를 들어, 전기음성도와 이온화 에너지는 일정 기간 동안 왼쪽에서 오른쪽으로 증가하는 경향이 있는 반면 원자 크기는 감소하는 경향이 있습니다. 이 정보는 화학 반응에서 원소가 어떻게 행동하는지 예측하는 데 사용될 수 있습니다.
- 원소 그룹화: 주기율표는 원소를 금속, 비금속 및 준금속과 같은 속성에 따라 범주로 그룹화합니다. 이는 과학자들이 요소 간의 유사점과 차이점, 그리고 요소들이 서로 상호 작용하는 방식을 이해하는 데 도움이 됩니다.
- 새로운 원소 발견: 주기율표는 또한 과학자들이 새로운 원소의 존재와 특성을 예측하는 데 도움이 됩니다. 과학자들은 표의 간격을 조사함으로써 발견되지 않은 원소의 특성을 예측하고 실험실에서 연구할 수 있습니다.
요약
주기율표에는 주기라고 불리는 7개의 수평선이 있습니다. 같은 시대의 요소는 같은 수의 전자 레이어를 가지고 있습니다. 주기율표에는 1부터 7까지 7개의 주기가 있으며, 원소 껍질의 수에 따라 주기가 결정됩니다.
주기율표의 주기를 지날수록 일반적으로 원자 반경은 감소하고, 전기음성도와 이온화 에너지는 일반적으로 증가합니다. 녹는점과 끓는점, 금속 특성, 반응성과 같은 다른 특성도 시간이 지나면서 예측 가능하게 변합니다.
주기율표의 주기는 원소의 성질을 예측하고, 추세를 파악하고, 원소를 그룹화하고, 새로운 원소를 발견하는 데 중요합니다. 과학자들은 표의 간격을 조사함으로써 발견되지 않은 원소의 특성을 예측하고 실험실에서 연구할 수 있습니다.
