메타중아황산나트륨(Na2S2O5)은 식품 및 음료의 방부제 및 항산화제로 사용되는 화합물입니다. 또한 다양한 산업 분야에서 소독제 및 표백제로 사용할 수 있습니다.
| IUPAC 이름 | 피로아황산나트륨 |
| 분자식 | Na2S2O5 |
| CAS 번호 | 7681-57-4 |
| 동의어 | 이황산이나트륨, 피로아황산, 이나트륨염, 피로아황산나트륨, 이황산나트륨 |
| 인치 | InChI=1S/2Na·H2O5S2/c;;1-6(2)7(3,4)5/h;;(H,1,2)(H,3,4,5)/q2*+1; /p-2 |
메타중아황산나트륨의 특성
나트륨 Metabisulfite 공식
메타중아황산나트륨의 화학식은 Na2S2O5입니다. 나트륨 이온(Na+) 2개와 이황산 이온(S2O5-2) 1개로 구성됩니다. 이 화합물은 백색 또는 황색을 띠는 결정성 분말로 물에 용해되고 자극적인 냄새가 난다.
Metabisulfite 나트륨 몰 질량
Na2S2O5의 몰 질량은 190.107 g/mol입니다. 이 값은 화합물 원소의 원자 질량(나트륨의 경우 22.99g/mol, 황의 경우 32.06g/mol, 산소의 경우 15.99g/mol)을 더하여 계산됩니다. 몰 질량은 화학 반응에 필요한 물질의 양을 결정하는 데 도움이 되는 중요한 특성입니다.
메타중아황산나트륨의 끓는점
Na2S2O5는 녹는점이 150°C로 높지만 끓기 전에 분해됩니다. 이 화합물은 약 150°C의 온도에서 이산화황(SO2)과 아황산나트륨(Na2SO3)으로 분해됩니다. 따라서 Na2S2O5의 끓는점은 적용되지 않습니다.
메타중아황산나트륨 녹는점
Na2S2O5의 녹는점은 150°C입니다. 이 온도에서 화합물은 고체에서 액체로 상변화를 겪는다. 녹는점은 물질을 식별하고 특성화하는 데 도움이 되는 중요한 물리적 특성입니다.
메타중아황산나트륨 g/mL의 밀도
Na2S2O5의 밀도는 1.48g/mL입니다. 물에 가라앉는 비교적 밀도가 높은 화합물입니다. 물질의 밀도는 단위 부피당 질량으로, 주어진 부피에 물질이 얼마나 들어 있는지 결정하는 데 도움이 되는 중요한 물리적 특성입니다.
나트륨 메타중아황산염 분자량
Na2S2O5의 분자량은 190.107g/mol입니다. 이는 화합물을 구성하는 모든 원자의 원자량의 합입니다. 분자량은 화학 반응에 필요한 물질의 양을 계산하는 데 도움이 되는 중요한 특성입니다.
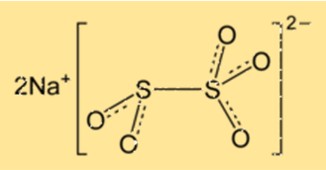
메타중아황산나트륨의 구조
Na2S2O5는 결정 구조를 가지며 사방정계 결정계에 속합니다. 결정 격자는 반복 패턴으로 배열된 나트륨 이온과 이황산염 이온으로 구성됩니다. 이 화합물은 사면체의 중심에 황 원자가 있는 사면체 분자 구조를 가지고 있습니다.
메타중아황산나트륨의 용해도
Na2S2O5는 물에 잘 녹으며, 용해도는 25°C에서 54g/100mL입니다. 또한 글리세롤에는 용해되고 에탄올에는 약간 용해됩니다. 물질의 용해도는 주어진 용매에 용해되는 능력을 결정하는 중요한 특성입니다.
| 모습 | 백색 또는 황색을 띠는 결정 성 분말 |
| 비중 | 1.48 |
| 색상 | 흰색에서 노란색을 띤다 |
| 냄새가 나다 | 에이커 |
| 몰 질량 | 190.107g/몰 |
| 밀도 | 1.48g/ml |
| 융합점 | 150°C |
| 비점 | 끓기 전에 분해됨 |
| 플래시 도트 | 해당 없음 |
| 물에 대한 용해도 | 25°C에서 54g/100mL |
| 용해도 | 글리세롤에 용해되고 에탄올에 약간 용해됨 |
| 증기압 | 사용 불가 |
| 증기 밀도 | 사용 불가 |
| pKa | 7.2 |
| pH | 4.5 (5% 용액) |
나트륨 메타중아황산염의 안전성과 위험성
Na2S2O5는 적절하게 취급하지 않으면 위험할 수 있습니다. 이는 노출 시 피부, 눈, 호흡기에 자극을 일으킬 수 있는 강력한 환원제입니다. 화합물을 섭취하면 심각한 위장 장애를 일으킬 수 있습니다. Na2S2O5는 부적합 물질로부터 멀리 떨어진 서늘하고 건조하며 통풍이 잘 되는 곳에 보관해야 합니다. 강산, 강산화제 또는 환원제와 혼합해서는 안됩니다. 화합물을 취급할 때는 장갑, 고글, 호흡기와 같은 보호 장비를 사용해야 합니다. 사고 발생 시 세안대, 소화기 등의 비상 조치를 즉시 이용할 수 있어야 합니다.
| 위험 기호 | 시 (짜증난다) |
| 보안 설명 | 피부와 눈에 닿지 않도록 하세요. 보호복과 장갑을 착용하십시오. 섭취하지 마십시오. 적절한 환기를 통해 사용하십시오. |
| UN 식별 번호 | 유엔 2676 |
| HS 코드 | 2832.10.00 |
| 위험등급 | 8 (부식성 물질) |
| 포장그룹 | III |
| 독성 | LD50(경구, 쥐): 1,000mg/kg; LC50(흡입, 쥐): 11mg/L(4시간) |
메타중아황산나트륨의 합성 방법
Na2S2O5는 과산화수소 와 같은 산화제 존재 하에서 중아황산나트륨을 이산화황과 반응시키는 것을 포함하여 다양한 방법으로 합성될 수 있습니다. 이 공정은 중아황산나트륨과 이산화황의 부가물을 가열하여 Na2S2O5를 형성합니다.
또 다른 방법은 수산화나트륨 을 이산화황 가스와 반응시킨 후 황산을 첨가하여 황산나트륨 과 Na2S2O5를 형성하는 것입니다.
또 다른 합성 방법은 탄산나트륨을 이산화황과 반응시킨 후 생성된 아황산나트륨을 공기 존재 하에서 가열하는 것입니다. 이 공정에서는 황산나트륨과 Na2S2O5가 생성됩니다.
과산화수소 나 질산과 같은 산화제가 있는 경우 황과 아황산나트륨을 반응시켜 Na2S2O5를 제조할 수 있습니다.
업계에서 Na2S2O5를 합성하는 가장 일반적인 방법은 이산화망간과 같은 촉매 존재 하에서 중아황산나트륨과 이산화황을 반응시키는 것입니다. 중아황산나트륨/이산화황 부가물을 가열하면 Na2S2O5가 형성됩니다.
메타중아황산나트륨의 용도
Na2S2O5는 강력한 환원 특성과 방부제 및 항산화제 역할을 하는 능력으로 인해 여러 산업에서 다양한 용도로 사용됩니다. Na2S2O5의 일반적인 용도는 다음과 같습니다.
- 식품 및 음료 산업: 와인, 맥주, 과일 주스 및 말린 과일과 같은 식품 및 음료 제품의 방부제 및 항산화제로 널리 사용됩니다. 이는 제품의 부패와 산화를 방지하여 유통기한을 연장하는 데 도움이 됩니다.
- 제약 산업: 크림, 연고, 정제 등 다양한 의약품의 항산화제로 사용됩니다. 이는 공기와 빛에 대한 노출로 인한 제품의 품질 저하를 방지하는 데 도움이 됩니다.
- 수처리: 수처리 공장에서 물의 염소를 제거하는 데 사용됩니다. 이는 수생 생물에 해로울 수 있는 과도한 염소와 클로라민을 제거하는 데 도움이 됩니다.
- 사진: 사진 업계에서 사진 현상업체 및 해결사로 사용됩니다. 이는 은 이온을 금속은으로 환원시켜 사진 이미지를 형성하는 데 도움이 됩니다.
- 섬유 산업: 섬유 산업에서 염색 및 인쇄 공정을 위한 환원제로 사용됩니다. 염료 용액에서 과잉 산소를 제거하는 데 도움을 주어 색상 강도와 균일성을 향상시킵니다.
질문:
Q: 메타중아황산나트륨은 현지 어디에서 구입할 수 있나요?
A: Na2S2O5는 일반적으로 화학제품 상점이나 온라인 소매점에서 찾을 수 있습니다. 식품 산업에서 일반적으로 방부제로 사용되기 때문에 일부 전문 식품점에서도 구입할 수 있습니다.
Q: 메타중아황산나트륨은 어디서 구입하나요?
A: Na2S2O5는 화학제품 판매점이나 온라인 특수 화학제품 소매점에서 구입할 수 있습니다. 일부 전문 식품점에서도 구입할 수 있습니다.
Q: 메타중아황산나트륨은 안전한가요?
A: Na2S2O5는 올바르게 취급하지 않으면 위험할 수 있습니다. 이 화합물을 취급할 때는 적절한 보호 장비를 착용하고 안전 예방조치를 따르는 것이 중요합니다. 피부와 눈에 자극을 유발할 수 있으며 산과 혼합되면 독성 이산화황을 방출할 수도 있습니다. 그러나 적절한 농도로 사용하고 조심스럽게 취급할 경우 Na2S2O5는 일반적으로 의도된 용도에 안전한 것으로 간주됩니다.
Q: 황산수소나트륨을 메타중아황산나트륨으로 바꿀 수 있나요?
A: 그렇습니다. 황산수소나트륨(NaHSO4)은 과산화수소와 같은 산화제가 있는 상태에서 고온으로 가열하면 Na2S2O5로 전환될 수 있습니다. 반응 결과 물이 방출되고 Na2S2O5가 형성됩니다.
Q: 중아황산나트륨과 메타중아황산나트륨의 차이점은 무엇입니까?
A: NaHSO3와 Na2S2O5의 주요 차이점은 화학 구조입니다. 중아황산나트륨에는 하나의 아황산염 그룹(-SO3)과 하나의 수소 이온(H+)이 있는 반면, Na2S2O5에는 두 개의 아황산염 그룹(-SO3)이 서로 결합되어 있습니다. Na2S2O5는 또한 중아황산나트륨보다 더 안정적이고 보관 수명이 더 깁니다.
Q: Na2S2O5에 포함된 S의 산화수는 얼마입니까?
A: Na2S2O5에 포함된 황(S)의 산화수는 +5입니다.
Q: KIO3 및 Na2S2O5에서 IO3- 농도를 찾는 방법은 무엇입니까?
A: IO3-의 농도는 전분을 지시약으로 사용하여 알려진 농도의 티오황산나트륨(Na2S2O3)으로 적정하여 결정할 수 있습니다. KIO3와 Na2S2O5 사이의 반응으로 요오드(I2)가 생성되고, 이는 Na2S2O3와 반응하여 NaI와 Na2S4O6를 형성합니다. 요오드와 반응하는 데 필요한 Na2S2O3의 부피를 측정하여 IO3-의 농도를 계산할 수 있습니다.
Q: Na2S2O5에는 어떤 이온이 포함되어 있나요?
A: Na2S2O5는 두 개의 나트륨 이온(Na+)과 한 개의 이황산염 이온(-S2O5)으로 구성됩니다.
