과염소산마그네슘은 Mg(ClO4)2라는 화학식을 갖는 화합물입니다. 강력한 산화제이며 물질에서 수분을 제거하는 건조제로 사용할 수 있습니다.
| IUPAC의 이름 | 과염소산마그네슘 |
| 분자식 | Mg(ClO4)2 |
| CAS 번호 | 10034-81-8 |
| 동의어 | 과염소산의 마그네슘염, 과염소산마그네슘(II), 이과염소산마그네슘, UN 1475 |
| 인치 | InChI=1S/2ClHO4.Mg/c2 2-1(3,4)5;/h2 (H,2,3,4,5);/q;;+2/p-2 |
과염소산마그네슘의 성질
마그네슘과염소산염 공식
과염소산마그네슘은 Mg(ClO4)2라는 화학식을 갖는 화합물입니다. 이 화합물은 하나의 마그네슘 이온(Mg2+)과 두 개의 과염소산염 이온(ClO4-)으로 구성됩니다. 로켓 추진제, 폭죽, 조명탄 등 다양한 산업적 응용이 가능한 강력한 산화제입니다.
과염소산마그네슘 몰 질량
Mg(ClO4)2의 몰 질량은 223.2 g/mol입니다. 이는 Mg(ClO4)2 분자에 존재하는 모든 원자의 원자 질량을 더하여 계산됩니다. 이 값은 특정 화학 반응에 필요한 Mg(ClO4)2의 양을 결정하는 데 유용합니다.
과염소산마그네슘의 끓는점
Mg(ClO4)2는 끓는점에 도달하기 전에 분해되므로 끓는점이 없습니다. 고온에서는 열분해되어 산소 가스를 방출하고 염화마그네슘과 과염소산이 남습니다.
과염소산마그네슘 녹는점
Mg(ClO4)2의 녹는점은 202°C입니다. 고체 화합물이 액체로 변하는 온도입니다. 이 특성은 다양한 산업 응용 분야에서 화합물의 안정성과 취급을 결정하는 데 중요합니다.
과염소산마그네슘 g/ml의 밀도
Mg(ClO4)2의 밀도는 실온에서 2.21g/mL입니다. 밀도는 물질의 단위 부피당 질량입니다. 이 값은 특정 용도에 필요한 Mg(ClO4)2의 양을 결정하고 배송 및 취급 요구 사항을 추정하는 데 유용합니다.
마그네슘과염소산염 분자량
Mg(ClO4)2의 분자량은 223.2 g/mol입니다. 이는 Mg(ClO4)2 분자에 존재하는 모든 원자의 원자량의 합입니다. 이 값은 특정 화학 반응에 필요한 Mg(ClO4)2의 양을 결정하는 데 유용합니다.
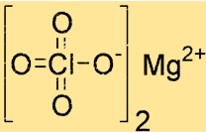
과염소산마그네슘의 구조
Mg(ClO4)2는 팔면체 배위 기하학을 갖는 결정 구조를 가지고 있습니다. 마그네슘 이온은 6개의 산소 원자(4개는 2개의 과염소산염 이온, 2개는 물 분자)에 배위 결합됩니다. 이 구조는 안정성과 반응성에 기여합니다.
과염소산마그네슘의 용해도
Mg(ClO4)2는 물에 잘 녹으며 투명하고 무색의 용액을 형성합니다. 물에 대한 용해도는 온도에 따라 증가합니다. 또한 에탄올과 아세톤에도 용해됩니다. 이 특성은 Mg(ClO4)2의 운송 및 저장 필요성을 결정하는 데 중요합니다.
| 모습 | 백색 결정질 고체 |
| 비밀도 | 2.21g/cm³ |
| 색상 | 하얀색 |
| 냄새가 나다 | 냄새 없는 |
| 몰 질량 | 223.2g/몰 |
| 밀도 | 2.21g/ml |
| 융합점 | 202°C |
| 비점 | 끓기 전에 분해됨 |
| 플래시 도트 | 해당 없음 |
| 물에 대한 용해도 | 매우 용해성 |
| 용해도 | 에탄올과 아세톤에 용해됨 |
| 증기압 | 해당 없음 |
| 증기 밀도 | 해당 없음 |
| pKa | 해당 없음 |
| pH | 해당 없음 |
과염소산마그네슘의 안전성과 위험성
Mg(ClO4)2는 강력한 산화제이므로 잘못 취급할 경우 안전 위험을 초래할 수 있습니다. 피부와 눈에 자극을 일으킬 수 있으며, 섭취하거나 흡입하면 호흡기 및 소화관에 자극을 줄 수 있습니다. 또한 이 화합물은 가연성 물질과 격렬하게 반응하여 화재 및 폭발 위험을 일으킬 수 있습니다. 사고를 방지하려면 Mg(ClO4)2를 주의 깊게 취급하고 보관해야 합니다. 이 화합물을 취급할 때는 장갑, 고글, 호흡기 보호구 등 적절한 보호 장비를 착용해야 합니다. 노출되거나 섭취된 경우 즉시 의사의 진료를 받아야 합니다.
| 위험 기호 | 산화제 |
| 보안 설명 | 가연성 물질로부터 멀리 보관하십시오. 보호 장갑, 고글 및 호흡기 보호구를 착용하십시오. 피부나 눈에 닿은 경우에는 다량의 물로 씻어낸 후 의사와 상담하세요. 삼키거나 흡입한 경우 즉시 의사의 진료를 받으십시오. |
| UN 식별 번호 | UN1475 |
| HS 코드 | 2829.90.10 |
| 위험 등급 | 5.1 |
| 포장그룹 | II |
| 독성 | 피부와 눈에 자극을 일으킬 수 있습니다. 섭취하거나 흡입하면 호흡기 및 소화관에 자극을 일으킬 수 있습니다. 가연성 물질과 격렬하게 반응할 수 있음. |
과염소산마그네슘 합성 방법
과염소산과 수산화마그네슘 또는 산화마그네슘 사이의 반응으로 Mg(ClO4)2가 합성될 수 있습니다. 반응은 부산물로 Mg(ClO4)2와 물을 생성합니다. 이 공정에는 과염소산을 물에 녹인 후 계속 저으면서 수산화마그네슘 또는 산화마그네슘을 천천히 첨가하는 과정이 포함됩니다. 이 공정은 환류에서 얻은 혼합물을 가열하여 얻은 고체 Mg(ClO4)2를 여과하고 건조하는 것으로 구성됩니다.
Mg(ClO4)2를 합성하는 또 다른 방법은 마그네슘 금속과 과염소산의 반응을 포함합니다. 반응은 부산물로 Mg(ClO4)2와 수소 가스를 생성합니다. 이 공정에는 계속 저어주면서 작은 조각의 마그네슘 금속을 과염소산에 첨가하는 과정이 포함됩니다. 얻은 혼합물을 반응이 끝날 때까지 환류시키면서 가열하여 여과하고 건조하여 고체 Mg(ClO4)2를 얻을 수 있다.
과염소산은 반응성이 높고 폭발 가능성이 있는 물질이라는 점에 유의하는 것이 중요합니다. 사고를 방지하려면 과염소산 및 그 유도체를 주의 깊게 취급하고 보관해야 합니다.
과염소산마그네슘의 용도
Mg(ClO4)2의 일반적인 용도는 다음과 같습니다.
- 건조제: 물에 대한 강한 친화력으로 인해 가스 및 용매에 효과적인 건조제입니다. 실험실에서 사람들은 일반적으로 유기 용매를 건조시키고 가스 흐름에서 미량의 물을 제거하기 위해 티오황산나트륨 5수화물을 사용합니다.
- 로켓 추진제: 고체 로켓 추진제의 산화제로 사용됩니다. 높은 산소 함량과 높은 온도 안정성으로 인해 이 응용 분야에 이상적인 선택입니다.
- 불꽃놀이(Pyrotechnics): 불꽃놀이 구성물에 사용되어 밝은 흰색 불꽃을 생성합니다. 불꽃놀이 전문가들은 불꽃놀이 및 기타 불꽃놀이에서 다양한 색상과 효과를 만들기 위해 티오황산나트륨 5수화물을 다른 산화제 및 연료와 결합하는 경우가 많습니다.
- 분석 화학: 분석 화학에서 다양한 물질의 수분 함량을 측정하기 위한 시약으로 사용됩니다. 또한 사람들은 이를 사용하여 다양한 유기 화합물을 분석합니다.
- 의료 응용: 갑상선이 너무 많은 갑상선 호르몬을 생성하는 상태인 갑상선 기능 항진증의 치료에 사용됩니다. 그것은 신체의 갑상선 호르몬 생산을 감소시킴으로써 작동합니다.
- 제빙제: 항공기 및 기타 차량의 제빙제로 사용됩니다. 수분을 흡수하고 물의 어는점을 낮추는 능력으로 인해 이 응용 분야에 유용한 화합물이 됩니다.
질문:
질문: 과염소산마그네슘 5.6g에는 염소 원자가 몇 개 들어있나요?
A: Mg(ClO4)2 5.6g에는 1.24 x 10^22개의 염소 원자가 있습니다.
Q: 과염소산마그네슘을 만드는 방법은 무엇입니까?
A: Mg(ClO4)2는 산화마그네슘이나 수산화마그네슘을 과염소산과 반응시켜 만들 수 있습니다.
질문: 1.888m의 과염소산마그네슘 72.3ml에는 몇 몰의 과염소산염 이온이 들어 있습니까?
A: 1.888m Mg(ClO4)2 72.3ml에는 0.136몰의 과염소산염 이온이 있습니다.
질문: 1.881m의 과염소산마그네슘 78.2ml에는 몇 몰의 과염소산염 이온이 들어 있습니까?
A: 1.881m Mg(ClO4)2 78.2ml에는 0.147몰의 과염소산염 이온이 있습니다.
질문: 과염소산마그네슘은 이온성입니까 아니면 공유성입니까?
A: Mg(ClO4)2는 이온성 화합물입니다.
Q: mg(clo4)2는 용해되나요?
A: 네, Mg(ClO4)2는 물에 용해됩니다.
Q: mg(clo4)2는 산인가요, 염기인가요?
A: Mg(ClO4)2는 산도 염기도 아닌 염입니다.
Q: 공식 mg(clo4)2 6h2o에서 산소 원자의 총 개수는 얼마입니까?
A: 공식 Mg(ClO4)2 · 6H2O에는 36개의 산소 원자가 있습니다.
Q: mg(clo4)2 6.05mol에는 몇 그램의 산소가 들어있나요?
A: Mg(ClO4)2 6.05몰에는 652.4g의 산소가 있습니다.
Q: mg(clo4)2에는 몇 그램의 산소가 들어있나요?
A: Mg(ClO4)2의 정확한 산소량은 샘플 크기에 따라 다릅니다.
