시클로헥산올 또는 C6H11OH는 약간의 냄새가 나는 무색 유성 액체입니다. 이는 일반적으로 용제로 사용되며 나일론 및 기타 화학 물질 생산에 사용됩니다.
| IUPAC 이름 | 사이클로헥산올 |
| 분자식 | C6H12O 또는 C6H11OH |
| CAS 번호 | 108-93-0 |
| 동의어 | 헥사히드로페놀; 하이드로페놀; 시클로헥실알코올; 헥살린; 사이클로헥사놀롤 |
| 화학 구조 | InChI=1S/C6H12O/c7-6-4-2-1-3-5-6/h6-7H,1-5H2 |
사이클로헥산올의 구조
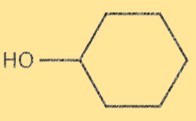
사이클로헥산올은 탄소 원자 중 하나에 수산기(-OH)가 부착된 6원 탄소 고리를 가지고 있습니다. 사이클로헥산올의 분자식은 C6H12O입니다. 사이클로헥산 고리는 축 방향 위치에 수산기가 있는 살 모양을 갖고 있습니다. 사이클로헥산올의 구조는 물리적, 화학적 특성을 결정하기 때문에 중요합니다.
사이클로헥산올 포뮬러
사이클로헥산올의 화학식은 C6H12O입니다. 이는 사이클로헥산올 분자의 원자 수와 유형을 나타냅니다. 이 공식은 반응에 필요한 사이클로헥산올의 양을 계산하는 데 사용되기 때문에 중요합니다. 또한 반응의 화학양론을 결정하는 데 사용됩니다.
사이클로헥산올의 IR 스펙트럼
사이클로헥산올의 IR 스펙트럼은 수산기(-OH)의 존재로 인해 약 3400cm-1에서 넓고 강한 피크를 나타냅니다. 이 피크는 알코올의 존재를 나타냅니다. 또한 스펙트럼은 사이클로헥산 고리의 존재로 인해 1000~1300cm-1 범위의 여러 피크를 보여줍니다. 사이클로헥산올의 IR 스펙트럼은 물질을 식별하고 특성화하는 데 사용될 수 있기 때문에 중요합니다.
시클로헥사놀 몰 질량
사이클로헥산올 분자의 모든 원자의 원자 질량의 합을 통해 몰 질량을 계산할 수 있으며, 이는 100.16 g/mol입니다. 몰 질량은 반응에 필요한 사이클로헥산올의 양을 결정하고 화학양론적 계산에서 그램과 몰을 변환하는 데 중요한 역할을 합니다.
사이클로헥산올 끓는점
사이클로헥산올의 끓는점은 161.5°C(322.7°F)입니다. 이는 사이클로헥산올의 액상이 기상으로 변하는 온도입니다. 끓는점은 혼합물의 다른 물질로부터 시클로헥사놀을 정제하고 분리하는 데 사용되기 때문에 중요한 물리적 특성입니다. 사이클로헥사놀은 상대적으로 높은 끓는점으로 인해 고온이 필요한 반응에서 용매로 유용합니다.
C6H11OH 녹는점
C6H11OH의 녹는점은 25.93°C(78.67°F)입니다. 이는 C6H11OH의 고체상이 액체상으로 변하는 온도입니다. 융점은 C6H11OH를 식별하고 특성화하는 데 사용되므로 중요한 물리적 특성입니다. 또한 C6H11OH의 순도를 결정하는 데에도 사용됩니다.
C6H11OH 밀도 g/mL
C6H11OH의 밀도는 25°C(77°F)에서 0.962g/mL입니다. 이는 물질의 단위 부피당 C6H11OH의 질량입니다. 밀도는 반응에 필요한 C6H11OH의 질량을 결정하는 데 사용되므로 중요한 물리적 특성입니다. 또한 용액 내 C6H11OH의 농도를 계산하는 데 사용됩니다.
C6H11OH 분자량
C6H11OH의 분자량은 100.16g/mol입니다. 이는 C6H11OH 분자에 있는 모든 원자의 원자량의 합입니다. 분자량은 반응에 필요한 C6H11OH의 양을 계산하는 데 사용되므로 중요한 특성입니다. 또한 화학양론적 계산에서 그램과 몰을 변환하는 데 사용됩니다.
| 모습 | 무색 액체 |
| 비중 | 0.962g/ml |
| 색상 | 무색 |
| 냄새가 나다 | 약간의 냄새 |
| 몰 질량 | 100.16g/몰 |
| 밀도 | 0.962g/ml |
| 융합점 | 25.93°C(78.67°F) |
| 비점 | 161.5°C(322.7°F) |
| 플래시 도트 | 70°C(158°F) |
| 물에 대한 용해도 | 혼용 가능 |
| 용해도 | 많은 유기용매에 용해됨 |
| 증기압 | 0.14kPa(25°C에서) |
| 증기 밀도 | 3.5(공기=1) |
| pKa | 16.1 |
| pH | 6 ~ 8 |
참고: 이 표에 제시된 값은 대략적인 값이며 정보 출처에 따라 다를 수 있습니다.
사이클로헥사놀의 안전성과 위험성
C6H11OH는 특정 안전 위험과 위험을 초래하므로 주의해서 취급해야 합니다. 이 화학물질에 노출되면 피부, 눈, 호흡기에 자극을 줄 수 있습니다. 또한 흡입하면 두통, 현기증, 메스꺼움을 유발할 수도 있습니다. C6H11OH를 섭취하면 복통, 구토, 설사를 유발할 수 있습니다. 이 화학물질은 가연성이며 열이나 화염에 노출되면 발화될 수 있습니다. 열이나 발화원으로부터 멀리 떨어진 서늘하고 건조한 곳에 보관하고 취급하는 것이 중요합니다. C6H11OH를 취급할 때는 장갑, 고글, 호흡기와 같은 보호 장비를 사용해야 합니다. 노출된 경우 즉시 의사의 진료를 받으십시오.
| 위험 기호 | 11 |
| 보안 설명 | S26 – 눈에 닿은 경우 즉시 다량의 물로 헹구고 의사의 진료를 받으십시오.<br> S36/37/39 – 적절한 보호복, 장갑 및 눈/눈 보호 장비를 착용하십시오. 얼굴.<br>S45 – 사고가 발생하거나 몸이 불편할 경우 즉시 의사와 상담하십시오(가능한 경우 의사에게 라벨을 보여 주십시오). |
| AN 식별자 | UN1986 |
| HS 코드 | 2907.13.00 |
| 위험등급 | 삼 |
| 포장그룹 | III |
| 독성 | 낮음에서 중간 정도의 독성 |
사이클로헥산올 합성 방법
C6H11OH는 여러 가지 방법으로 합성할 수 있습니다.
- C6H11OH를 생산하는 일반적인 방법은 니켈이나 백금과 같은 금속 촉매가 있는 상태에서 페놀을 촉매적으로 수소화하는 것입니다. 이 방법은 페놀의 방향족 고리를 환원시켜 C6H11OH를 형성하는 것을 포함합니다.
- 또 다른 방법은 구리나 코발트와 같은 촉매가 있는 상태에서 공기나 산소를 사용하여 시클로헥산을 산화시키는 것입니다. 이 공정은 추가로 산화되어 사이클로헥사논을 형성할 수 있는 중간 생성물로 C6H11OH를 생성합니다.
- C6H11OH는 산성 또는 염기성 촉매를 사용하여 시클로헥실 아세테이트를 가수분해하여 얻을 수도 있습니다. 이 방법은 시클로헥실 아세테이트의 에스테르 결합을 절단하여 C6H11OH와 아세트산을 형성하는 것을 포함합니다.
- 황산을 촉매로 사용하는 Beckmann의 시클로헥사논 옥심 재배열은 C6H11OH를 합성하는 또 다른 방법입니다. 이 공정에는 시클로헥사논 옥심의 옥심 그룹을 재구성하여 아미드 중간체를 형성하는 과정이 포함되며, 이 중간체는 가수분해되어 C6H11OH를 생성할 수 있습니다.
전반적으로 C6H11OH의 합성을 위해서는 개인이 다양한 화학 공정을 수행하고 적절한 안전 예방 조치와 장비를 사용해야 합니다.
사이클로헥산올의 용도
C6H11OH는 다양한 산업 분야에서 많은 응용 분야를 가지고 있습니다.
- 산업계에서는 C6H11OH를 래커, 바니시 및 수지를 생산하는 용매로 사용하고 제약 산업에서 약물을 제조하는 용매로 사용합니다.
- C6H11OH는 나일론 제조에 필요한 성분인 아디프산 생산에서 중요한 중간체 역할을 합니다. 또한 비스페놀A, 시클로헥사논, 카프로락탐 등 다양한 화학물질 합성의 원료로도 사용됩니다.
- 석유 산업에서는 파이프라인과 저장 탱크의 부식을 방지하기 위해 원유에 부식 억제제로 C6H11OH를 첨가합니다.
- 제조업체는 C6H11OH를 사용하여 플라스틱의 유연성과 내구성을 향상시키는 가소제를 생산합니다. 또한 향수와 화장품에도 흔히 사용되는 성분입니다.
- C6H11OH는 열전달 유체, 윤활제 및 살충제로 사용됩니다. 또한 유기 합성 및 실험실 실험에서 시약 역할을 합니다.
전반적으로 C6H11OH는 다양한 산업 분야에서 광범위하게 응용되며 다양한 특성으로 인해 많은 산업 공정에서 중요한 화학 물질로 사용됩니다.
질문:
사이클로헥산올은 물에 용해되나요?
사이클로헥산올은 물에 적당히 용해되지만 온도가 증가함에 따라 용해도가 감소합니다. 에탄올, 디에틸에테르, 아세톤과 같은 유기용매에 더 잘 녹습니다. 물에 대한 C6H11OH의 용해도는 C6H11OH의 수산기와 물 분자 사이의 수소 결합 형성에 기인합니다. 그러나 C6H11OH의 소수성 사이클로헥산 고리는 전반적인 극성을 감소시켜 메탄올이나 에탄올과 같은 극성이 높은 다른 알코올보다 물에 덜 용해됩니다. 물에 대한 C6H11OH의 용해도는 용매로 사용하는 경우와 물을 매체로 사용하는 산업 공정에서 중요한 고려 사항입니다.
다음 일련의 반응 중 사이클로헥산올을 1,2-에폭시사이클로헥산으로 전환시키는 것은 무엇입니까?
사이클로헥산올을 1,2-에폭시사이클로헥산으로 전환하려면 다음과 같은 일련의 반응을 수행할 수 있습니다.
- 사이클로헥산올은 먼저 황산과 같은 강산성 촉매로 처리되어 탈수를 통해 사이클로헥센을 형성합니다.
- 생성된 시클로헥센은 m-클로로과벤조산(MCPBA)과 같은 과산과 반응하여 에폭시드, 특히 1,2-에폭시시클로헥산을 형성합니다.
따라서 시클로헥사놀을 1,2-에폭시시클로헥산으로 전환하는 올바른 일련의 반응에는 과산을 사용하여 시클로헥산을 탈수하여 시클로헥센을 형성한 후 시클로헥센을 에폭시화하여 1,2-에폭시시클로헥산을 형성하는 것이 포함됩니다.
시클로헥사놀에는 왜 숫자 접두어가 필요하지 않습니까?
시클로헥사놀은 시클로헥사놀의 단일 이성질체이기 때문에 이름에 숫자 접두사가 필요하지 않습니다. 이성질체는 분자식은 동일하지만 원자의 구조적 배열이 다른 분자입니다. 사이클로헥산올은 사이클로헥산 고리에 단일 수산기 작용기(-OH)가 부착되어 있으며 분자식은 C6H12O입니다. 사이클로헥사놀에는 원자 배열이 하나만 있기 때문에 위치나 작용기 수를 지정하기 위해 숫자 접두어가 필요하지 않습니다. 대조적으로, 시클로헥사논 및 시클로헥산디온과 같은 다른 화합물은 카르보닐기의 위치와 수가 서로 다른 여러 이성질체를 가지므로 작용기의 위치를 지정하려면 숫자 접두어가 필요합니다.
