重炭酸リチウム (LiHCO3) は、さまざまな用途に使用される化合物です。アルカリ性の特性があり、研究、医薬品、および特定の病状の潜在的な治療法として使用されています。
| IUPAC名 | 重炭酸リチウム |
| 分子式 | LiHCO3 |
| CAS番号 | 5006-97-3 |
| 同義語 | 炭酸水素リチウム、重炭酸リチウム |
| インチチ | InChI=1S/CH2O3.Li/c2-1(3)4;/h(H2,2,3,4);/q;+1 |
重炭酸リチウムの性質
重炭酸リチウムの配合
炭酸水素リチウムの化学式は LiHCO3 です。リチウムカチオン(Li)、炭酸水素アニオン(HCO3)、水素原子(H)で構成されています。この式は、化合物中のリチウムおよび重炭酸イオンの存在を反映しています。
重炭酸リチウムのモル質量
炭酸水素リチウム (LiHCO3) のモル質量は、1 モルあたり約 68 グラム (g/mol) です。これは、その構成要素であるリチウム、水素、炭素、酸素の原子量を加算することによって計算されます。
重炭酸リチウムの沸点
炭酸水素リチウムは高温で分解するため、明確に定義された沸点がありません。加熱すると二酸化炭素(CO2)と水(H2O)が失われ、炭酸リチウム(Li2CO3)に変化します。
重炭酸リチウム 融点
炭酸水素リチウムの融点は約 250 ℃ (華氏 482 度) です。この温度では、固体から液体への相転移が起こります。
重炭酸リチウムの密度 g/mL
炭酸水素リチウム (LiHCO3) の密度は約 2.21 グラム/ミリリットル (g/mL) です。リチウムおよびその他の重元素が存在するため、比較的高密度の化合物です。
重炭酸リチウムの分子量
炭酸水素リチウムの分子量は約 68 g/mol です。分子量は、化合物の単一分子内のすべての原子の原子量の合計を表します。
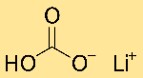
重炭酸リチウムの構造
炭酸水素リチウムは結晶構造を持っています。リチウム、炭酸水素原子、水素原子が繰り返しパターンで配置されたネットワークを形成します。この構造はイオン結合と共有結合によって結合されています。
重炭酸リチウムの溶解度
炭酸水素リチウムは水に溶けにくいです。水にある程度溶けて弱アルカリ性の溶液になります。ただし、他のリチウム化合物に比べて溶解度は比較的低いです。
| 外観 | 白色の結晶性粉末 |
| 比重 | ~2.21 g/mL |
| 色 | 白 |
| 匂い | 無臭 |
| モル質量 | ~68 g/モル |
| 密度 | ~2.21 g/mL |
| 融合点 | ~250°C (482°F) |
| 沸点 | 分解された |
| フラッシュドット | 適用できない |
| 水への溶解度 | わずかに溶け、弱アルカリ性の溶液になります。 |
| 溶解性 | 限界 |
| 蒸気圧 | 利用不可 |
| 蒸気密度 | 利用不可 |
| pKa | 利用不可 |
| pH | 弱アルカリ性 |
重炭酸リチウムの安全性と危険性
炭酸水素リチウムには、特定の安全上の考慮事項と危険性があります。リスクを最小限に抑えるために、化合物を慎重に取り扱うことが不可欠です。皮膚や目に直接触れると刺激を引き起こす可能性があります。呼吸器系の不快感を引き起こす可能性があるため、粉塵や煙の吸入は避けてください。加熱すると分解して二酸化炭素と水蒸気を放出しますが、密閉空間では潜在的に危険です。さらに、炭酸水素リチウムを不適合物質から離して適切に保管することが重要です。この化合物を扱うときは、安全な環境を確保するために、適切な換気と個人用保護具を使用する必要があります。
| ハザードシンボル | 利用不可 |
| セキュリティの説明 | 取り扱い注意。吸入、皮膚や目との接触を避けてください。適切に保管してください。換気の良い場所で使用してください。 |
| 国連識別番号 | 利用不可 |
| HSコード | 利用不可 |
| 危険等級 | 利用不可 |
| 梱包グループ | 利用不可 |
| 毒性 | 毒性が低い。デポジット付きで対応します。 |
重炭酸リチウムの合成方法
炭酸水素リチウムはさまざまな方法で合成できます。
一般的なアプローチは、水酸化リチウム (LiOH)と二酸化炭素 (CO2) を反応させることです。反応は水溶液中で起こり、水酸化リチウムがリチウムイオンと水酸化物イオンに解離します。同時に、二酸化炭素は水に溶解し、炭酸 (H2CO3)を形成します。次に、リチウムイオンは炭酸と反応して、炭酸水素リチウム (LiHCO3) と水 (H2O) を生成します。この反応の化学式は次のとおりです。
LiOH + CO2 → LiHCO3 + H2O
別の方法では、密閉系で炭酸リチウム (Li2CO3) を二酸化炭素で処理して、重炭酸リチウムを生成します。この反応の化学式は次のとおりです。
Li2CO3 + CO2 → 2LiHCO3
これらの合成方法は、実験室での炭酸水素リチウムの製造や産業用途にとって重要です。安全プロトコルに従い、合成プロセス中に適切な装置と条件を確保することが重要です。
重炭酸リチウムの用途
炭酸水素リチウムは、その独特の特性により多くの用途に使用されます。主な用途のいくつかを次に示します。
- 研究と実験室: さまざまな化学実験や研究実験で貴重な試薬として機能し、科学者が化学反応や特性を研究できるようになります。
- 潜在的な治療法: アルカリ化剤としてだけでなく、リチウム欠乏症や特定の腎臓障害などの病気の治療法としての潜在的な役割について研究が進行中です。
- 環境への応用: 工業プロセスからの二酸化炭素の除去に貢献でき、温室効果ガス排出の軽減にも応用できる可能性があります。
- アルカリ化剤: 特定の工業プロセスにおいて、酸性度を制御し、pH レベルを調整するアルカリ化剤として機能します。
- 製薬業界: 医薬品製剤では、主に双極性障害などの気分障害の治療薬に炭酸水素リチウムが使用されています。
- リチウム電池の製造: 研究者や実験サークルは、電池の性能を向上させるために、先進的なリチウムベースの電池に炭酸水素リチウムを使用することを研究しています。
- 水処理: 水処理プロセスでは、重炭酸リチウムを使用して水源の pH を調整します。
- 農業: 炭酸水素リチウムの農業現場での用途は限られており、農家は特定の土壌条件を処理し、植物の成長を改善するために炭酸水素リチウムを使用しています。
これらの用途にもかかわらず、炭酸水素リチウムには潜在的な危険性と反応性があるため、慎重に取り扱い、安全上の注意事項に従うことが重要です。研究と技術の進歩が続くにつれて、炭酸水素リチウムの新たな用途が出現し、さまざまな分野での重要性がさらに高まる可能性があります。
質問:
Q: 重炭酸リチウムの化学式は何ですか?
A: 炭酸水素リチウムの化学式は LiHCO3 です。
Q: 重炭酸リチウムはビタミン D 不足を引き起こす可能性がありますか?
A: 炭酸水素リチウムがビタミン D レベルの低下を引き起こすことを示唆する証拠はありません。
Q: 炭酸リチウムと重炭酸リチウムのどちらがより効果的ですか?
A: 炭酸リチウムまたは重炭酸リチウムの有効性は、その特定の用途と使用目的によって異なります。
Q: 重炭酸リチウムはバレリアン抽出物と相互作用しますか?
A: 炭酸水素リチウムとバレリアン抽出物との相互作用は知られていませんが、医療専門家との相談が不可欠です。
Q: 重炭酸リチウムとは何ですか?
A: 炭酸水素リチウムはアルカリ性の性質を持つ化合物で、研究や医薬品などのさまざまな用途に使用されています。
Q: 重炭酸リチウムと炭酸リチウムは水中で加熱できますか?
A: 炭酸水素リチウムと炭酸リチウムは水中で加熱できますが、分解して他の化合物を形成します。
Q: 3.45g の LiHCO3 が分解されるときの重量減少はどれくらいですか?
A: 3.45 g の LiHCO3 が分解されるときの重量損失は、特定の反応と生成される生成物によって異なります。
Q: LiHCO3 は強電解質ですか?
A: いいえ、炭酸水素リチウム (LiHCO3) は弱電解質です。
Q: H2SO4 と LiHCO3 の反応によりどのような塩が生成されますか?
A: H2SO4 と LiHCO3 の反応では、硫酸リチウム (Li2SO4)、二酸化炭素 (CO2)、水 (H2O) が生成されます。
Q: LiHCO3 は酸ですか、それとも塩基ですか?
A: 炭酸水素リチウム (LiHCO3) はアルカリ性であるため、塩基として作用します。
Q: N-メチルエタンアミンは LiHCO3 と反応しますか?
A: N-メチルエタンアミンと LiHCO3 の反応性は、特定の反応条件と目的の生成物によって異なります。
