上の画像はもう見たはずですよね?
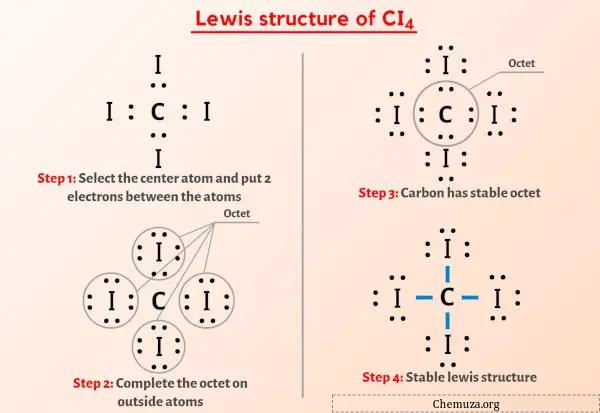
上の画像について簡単に説明します。
CI4 ルイス構造の中心には炭素 (C) 原子があり、その周りを 4 つのヨウ素 (I) 原子が取り囲んでいます。炭素 (C) 原子と各ヨウ素 (I) 原子の間には 4 つの単結合があります。 4 つのヨウ素(I) 原子には 3 つの孤立電子対があります。
CI4 のルイス構造の上の画像から何も理解できなかった場合は、 CI4のルイス構造を描画する方法について段階的に詳しく説明しますので、そのままお付き合いください。
それでは、CI4 のルイス構造を描く手順に進みましょう。
CI4 ルイス構造を描画する手順
ステップ 1: CI4 分子内の価電子の総数を見つける
CI4分子内の価電子の総数を調べるには、まず炭素原子とヨウ素原子に存在する価電子を知る必要があります。
(価電子は、原子の最も外側の軌道に存在する電子です。)
ここでは、周期表を使って炭素とヨウ素の価電子を簡単に求める方法を説明します。
CI4 分子内の総価電子
→ 炭素原子によって与えられる価電子:
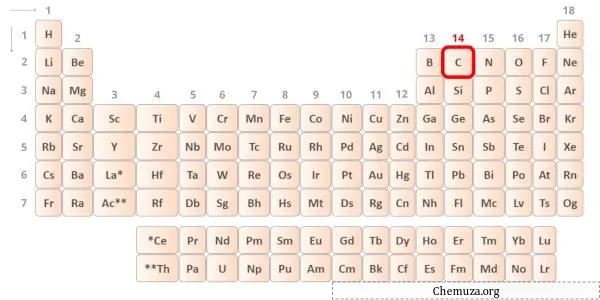
炭素は周期表の第 14 族の元素です。 [1]したがって、炭素に存在する価電子は4です。
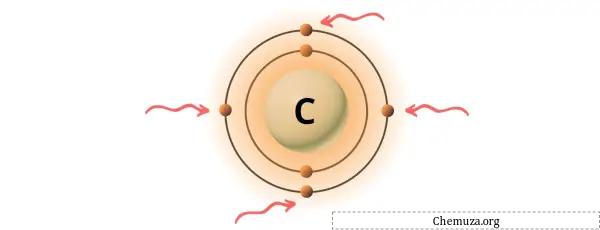
上の画像に示すように、炭素原子には 4 つの価電子が存在することがわかります。
→ ヨウ素原子によって与えられる価電子:
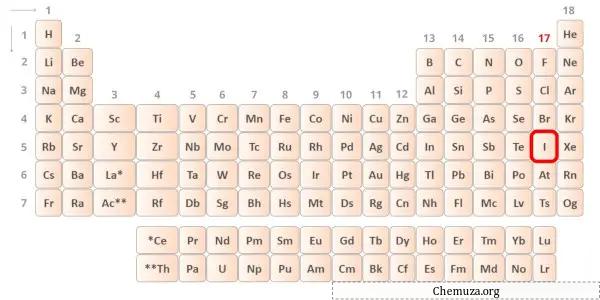
ヨウ素は、周期表の第 17 族の元素です。 [2]したがって、ヨウ素に存在する価電子は7です。
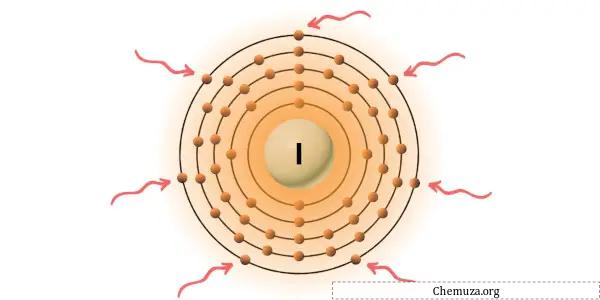
上の画像に示すように、ヨウ素原子には 7 つの価電子が存在することがわかります。
それで、
CI4 分子内の総価電子= 1 個の炭素原子によって供与された価電子 + 4 個のヨウ素原子によって供与された価電子 = 4 + 7(4) = 32 。
ステップ 2: 中心原子を選択する
中心原子を選択するには、最も電気陰性度の低い原子が中心に残ることを覚えておく必要があります。
ここで、与えられた分子は CI4 であり、これには炭素 (C) 原子とヨウ素 (I) 原子が含まれています。
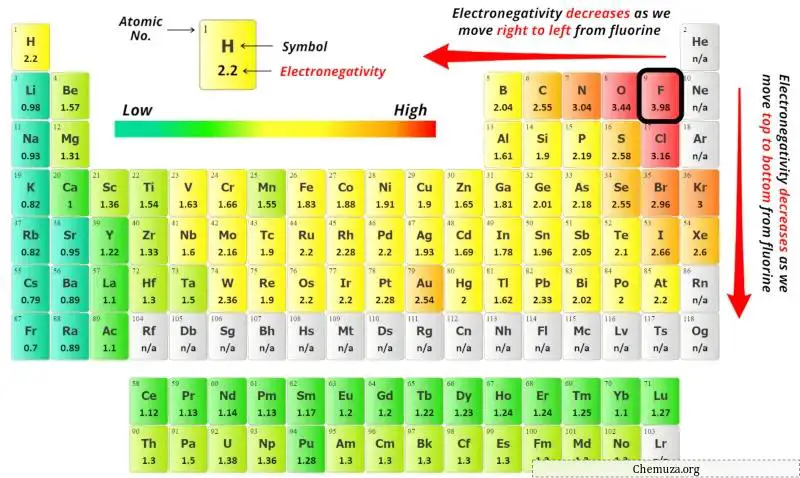
上記の周期表の炭素 (C) 原子とヨウ素 (I) 原子の電気陰性度の値を確認できます。
炭素 (C) とヨウ素 (I) の電気陰性度の値を比較すると、炭素原子の方が電気陰性度が低くなります。
ここで、炭素 (C) 原子が中心原子であり、ヨウ素 (I) 原子が外側の原子です。

ステップ 3: 各原子の間に電子対を配置して各原子を接続する
ここで、CI4 分子では、炭素原子 (C) とヨウ素原子 (I) の間に電子対を配置する必要があります。
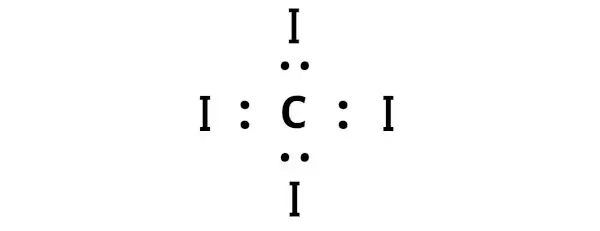
これは、CI4 分子内で炭素 (C) とヨウ素 (I) が化学結合していることを示しています。
ステップ 4: 外部原子を安定化する
このステップでは、外部原子の安定性をチェックする必要があります。
ここで、CI4 分子のスケッチでは、外側の原子がヨウ素原子であることがわかります。
これらの外部ヨウ素原子はオクテットを形成するため、安定しています。
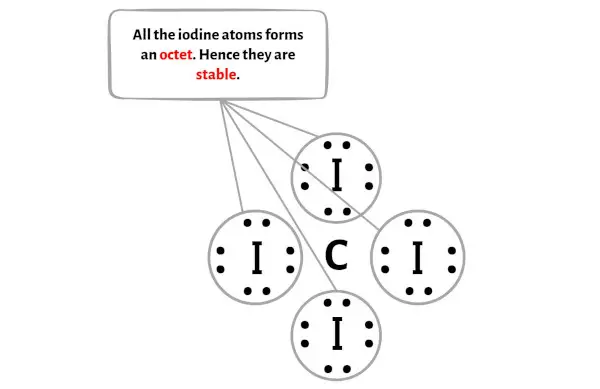
さらに、ステップ 1 では、CI4 分子内に存在する価電子の総数を計算しました。
CI4 分子には合計32 個の価電子があり、これらすべての価電子が上の CI4 の図で使用されています。
したがって、中心原子上に保持すべき電子の対はもう存在しません。
それでは、次のステップに進みましょう。
ステップ 5: 中心原子のオクテットを確認する
このステップでは、中心の炭素原子 (C) が安定であるかどうかを確認する必要があります。
中心の炭素原子 (C) の安定性を確認するには、それがオクテットを形成しているかどうかを確認する必要があります。
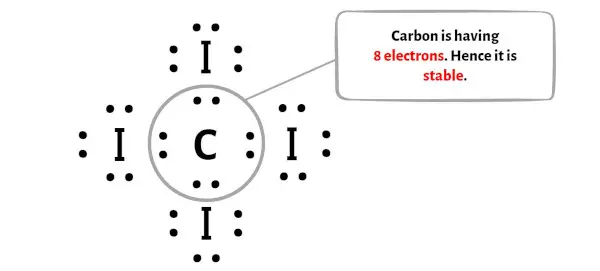
上の画像では、炭素原子がオクテットを形成していることがわかります。これは電子が8個あることを意味します。
したがって、中心の炭素原子は安定しています。
それでは、CI4 のルイス構造が安定であるかどうかを確認する最後のステップに進みましょう。
ステップ 6: ルイス構造の安定性を確認する
これで、CI4 のルイス構造の安定性を確認する必要がある最後のステップに到達しました。
ルイス構造の安定性は、形式電荷概念を使用して検証できます。
つまり、CI4 分子に存在する炭素 (C) 原子とヨウ素 (I) 原子の形式電荷を見つける必要があります。
正式な税金を計算するには、次の式を使用する必要があります。
形式電荷 = 価電子 – (結合電子)/2 – 非結合電子
以下の画像で、CI4 分子の各原子の結合電子と非結合電子の数を確認できます。
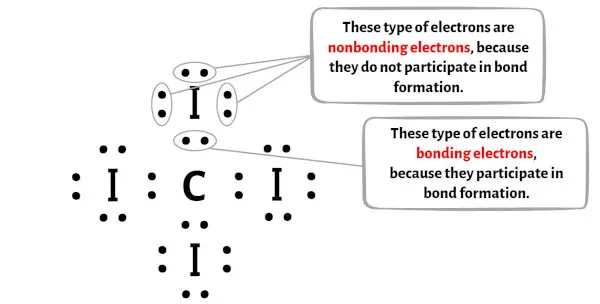
炭素原子 (C) の場合:
価電子 = 4 (炭素は 14 族にあるため)
結合電子 = 8
非結合電子 = 0
ヨウ素 (I) 原子の場合:
価電子 = 7 (ヨウ素は 17 族にあるため)
結合電子 = 2
非結合電子 = 6
| 正式な告発 | = | 価電子 | – | (結合電子)/2 | – | 非結合電子 | ||
| VS | = | 4 | – | 8/2 | – | 0 | = | 0 |
| 私 | = | 7 | – | 2/2 | – | 6 | = | 0 |
上記の形式電荷の計算から、炭素 (C) 原子とヨウ素 (I) 原子の形式電荷は「ゼロ」であることがわかります。
これは、CI4 の上記のルイス構造が安定であり、CI4 の上記の構造にさらなる変化がないことを示しています。
CI4 の上記のルイス ドット構造では、結合電子の各ペア (:) を単結合 (|) として表すこともできます。そうすると、CI4 の次のルイス構造が得られます。
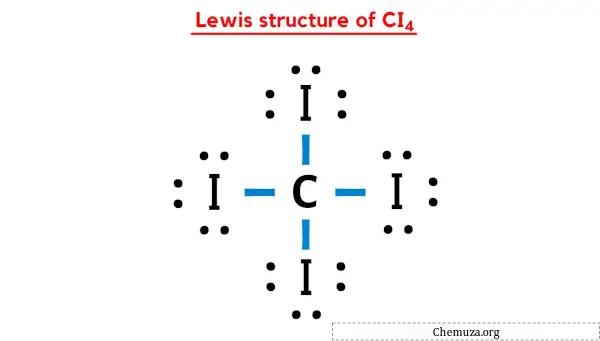
上記の手順をすべて完全に理解していただければ幸いです。
さらに練習して理解を深めたい場合は、以下にリストされている他のルイス構造を試してみてください。
理解を深めるために、次のルイス構造を試してください (または少なくとも見てください)。
