ブタン (C₄H₁₀) は引火性の高い炭化水素ガスです。効率的な燃焼特性と持ち運びのしやすさから、ライターやキャンプ用ストーブの燃料としてよく使用されます。
| IUPAC名 | ブタン |
| 分子式 | C₄H₁₀ |
| CAS番号 | 106-97-8 |
| 同義語 | n-ブタン、水素化ブチル、メチルエチルメタン、ジエチル |
| インチチ | InChI=1S/C4H10/c1-3-4-2/h3-4H2.1-2H3 |
ブタンの性質
ブタンの式
ブタンの式は C4H10 で、4 個の炭素原子と 10 個の水素原子で構成されていることを示します。この式はブタンの化学組成に関する貴重な情報を提供し、科学者がその特性と挙動を研究できるようにします。
ブタンのモル質量
水素化ブチルのモル質量は、その構成元素の原子質量を加算することで計算できます。水素化ブチル (C4H10) の場合、モル質量は 1 モルあたり約 58.12 グラムです。モル質量はさまざまな化学計算において重要なパラメーターであり、水素化ブチルの物理的および化学的特性を決定する際に重要な役割を果たします。
ブタンの沸点
水素化ブチルの沸点は約 -1°C (30°F) と比較的低くなります。これは、この温度以上では、水素化ブチルが液相から気相に容易に転移することを意味します。沸点が低いため、水素化ブチルはライターやキャンプ用ポータブルストーブなどの用途に理想的な燃料となります。
ブタンの融点
水素化ブチルの融点は約 -138.4°C (-217.12°F) です。この温度以下では、固体の水素化ブチルが相変化を起こし、液体になります。ただし、通常の大気条件下では、水素化ブチルは通常、ガス状で存在します。
ブタン密度 g/mL
水素化ブチルの密度は 1 ミリリットルあたり約 2.48 グラムです。これは、水素化ブチルが密度 1 g/mL の水よりも軽いことを示しています。水素化ブチルの密度は、燃焼特性だけでなく、保管中や輸送中の挙動を決定する重要な特性です。
ブタンの分子量
水素化ブチルの分子量は、1 モルあたり約 58.12 グラムです。これは、単一の水素化ブチル分子内のすべての原子の原子量の合計を表します。分子量はさまざまな科学計算に不可欠なパラメータであり、水素化ブチルの特性と挙動を理解するのに役立ちます。
ブタンの構造
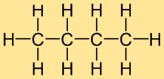
水素化ブチルの構造は、4 個の炭素原子の直鎖に 10 個の水素原子が結合しています。炭素原子は連続線に配置されており、各炭素原子は隣接する 2 つの炭素原子および 3 つの水素原子と単結合を形成します。この線状構造は、水素化ブチルの物理的および化学的特性に寄与します。
ブタンの溶解度
水素化ブチルは水に比較的溶けにくいと考えられています。非極性の性質と水分子との分子間相互作用が弱いため、溶解度が低くなります。ただし、水素化ブチルはエタノールやアセトンなどの有機溶媒によく溶けます。この溶解挙動は、抽出プロセスや溶媒ベースの反応などのさまざまな用途で重要です。
| 外観 | 無色の気体 |
| 比重 | 2.48 |
| 色 | 該当なし |
| 匂い | 無臭 |
| モル質量 | 58.12 g/モル |
| 密度 | 2.48g/ml |
| 融合点 | -138.4°C (-217.12°F) |
| 沸点 | -1°C (30°F) |
| フラッシュドット | -60°C (-76°F) |
| 水への溶解度 | 不溶性 |
| 溶解性 | 有機溶剤に可溶 |
| 蒸気圧 | 20°C で 2.4 ATM |
| 蒸気密度 | 2.07 (空気 = 1) |
| pKa | 該当なし |
| pH | 該当なし |
ブタンの安全性と危険性
水素化ブチルには、考慮する必要がある特定の安全上のリスクが伴います。これは引火性の高いガスであり、点火源が存在すると容易に発火する可能性があります。偶発的な火災や爆発を避けるために予防措置を講じる必要があります。可燃性蒸気の蓄積を避けるために、水素化ブチルを換気の良い場所で保管および取り扱うことが重要です。水素化ブチルを直接吸入すると、酸素が置換され、窒息を引き起こす可能性があるため、有害となる可能性があります。さらに、高濃度の水素化ブチルに曝露すると、めまい、眠気、吐き気を引き起こす可能性があります。適切に設計され承認された装置で水素化ブチルを使用し、裸火や火花との接触を避けるなど、適切な安全上の予防措置に従うことが重要です。
| ハザードシンボル | 可燃性ガス |
| セキュリティの説明 | 裸火や火花から遠ざけてください。換気の良い場所に保管してください。吸入や直接接触を避けてください。 |
| 国連の識別子 | 国連 1011 |
| HSコード | 2711.12.20 |
| 危険等級 | クラス2.1(可燃性ガス) |
| 梱包グループ | パッキンググループ II |
| 毒性 | 水素化ブチルは一般に毒性が低いと考えられています。ただし、高濃度を吸入すると、めまい、眠気、吐き気を引き起こす可能性があります。また、密閉空間内の酸素を置換し、窒息を引き起こす可能性があります。安全を確保するには、適切な換気と取り扱い手順に従う必要があります。 |
ブタンの合成方法
水素化ブチルはさまざまな方法で合成されますが、主に石油または天然ガスの生産が含まれます。
分別蒸留: 原油または石油の分別蒸留中に、副生成物として水素化ブチルが生成されます。精製プロセスでは、沸点に基づいてさまざまな炭化水素留分が分離され、水素化ブチルは分離できる成分の 1 つです。
天然ガス処理: 天然ガス処理では水素化ブチルも生成します。天然ガスには、メタンや水素化ブチルなどの高級炭化水素など、さまざまな炭化水素が含まれています。天然ガス混合物は、吸収または極低温分離などのプロセスを経て、水素化ブチルが分離されます。
炭化水素分解: 分解プロセスでは、大きな炭化水素鎖が小さな鎖に分解され、水素化ブチルが生成されます。これには、より重い炭化水素を高温にさらすか、触媒を使用して生成物として水素化ブチルを生成することが含まれます。
異性化: 異性化は炭化水素の分子構造を再配置し、ペンタンやヘキサンなどの他の炭化水素をその異性体に異性化することによって水素化ブチルの合成を可能にします。特定の触媒は、適切な条件下でこのプロセスを触媒します。
合成プロセス: 研究室では、科学者は合成ルートを通じて水素化ブチルを合成できます。水素化や還元などのさまざまな化学反応を利用して、前駆体化合物から水素化ブチルを生成できます。
これらの方法により、小規模の実験室だけでなく大規模な工業プロセスでも水素化ブチルを製造することが可能になります。方法の選択は、原料の入手可能性、望ましい純度、および用途の特定の要件によって異なります。
ブタンの用途
水素化ブチルは、その有益な特性により、さまざまな産業や日常使用に応用されています。水素化ブチルの一般的な用途は次のとおりです。
- 燃料: 水素化ブチルは、その高いエネルギー含有量と効率的な燃焼特性のおかげで、ポータブルストーブ、キャンプ用ヒーター、ライターの燃料として使用されます。
- エアゾール噴射剤: 水素化ブチルは、ヘア スプレー、芳香剤、エアゾール ペイントなどのエアゾール製品を噴射し、細かいミストやスプレーとして放出することができます。
- 冷媒:水素化ブチルは、家庭用冷蔵庫や冷凍庫などの小規模冷凍システムにおいて冷媒として冷却され、低温を維持します。
- ライター液: 水素化ブチルはシガレット ライターやトーチ ライターに動力を供給し、ライター液の重要な成分である炎を生成します。
- 抽出: 水素化ブチルは、植物材料からエッセンシャル オイルや植物化合物を抽出する際の溶媒として機能し、目的の化合物を効果的に溶解します。
- 実験室での使用: 実験室では、ブンゼンバーナーやガスクロマトグラフィーの燃料として水素化ブチルを使用しています。
- 校正ガス: 水素化ブチルはガス検知器およびセンサーの校正ガスとして機能し、明確に定義され、容易に測定できる特性を提供します。
- 溶接とろう付け: 水素化ブチルトーチは、高温、精度、使いやすさのおかげで、溶接とろう付け作業を容易にします。
- レクリエーション: 水素化ブチルはポータブル キャンプ ストーブや懐中電灯に電力を供給し、キャンプ、ハイキング、料理などの屋外レクリエーション活動を強化します。
- 消費源: 水素化ブチルは、特定の産業における加熱ツール、小型ヒーター、火炎ベースの用途など、さまざまな用途で熱源として機能します。
水素化ブチルの多用途な性質とその応用範囲の広さにより、水素化ブチルはいくつかの産業、家庭用品、レクリエーション活動において価値のある化合物となっています。
質問:
Q: 近くでブタンガスはどこで買えますか?
A: 水素化ブチルガスは通常、キャンプ用品を販売する地元のホームセンター、スーパーマーケット、コンビニエンス ストアで入手できます。
Q: ブタンガスは天然ガスですか?
A: いいえ、水素化ブチルは天然ガスとみなされません。石油または天然ガスの処理から得られる炭化水素ガスです。
Q: ブタンとは何ですか?
A: 水素化ブチルは、化学式 C4H10 を持つガス状炭化水素です。無色無臭の可燃性ガスで、燃料やさまざまな用途に一般的に使用されています。
Q: ブタンはどのように作られるのですか?
A: 水素化ブチルは主に、石油または天然ガスの分別蒸留、より重質の炭化水素の分解、または他の炭化水素の異性化などのプロセスによって製造されます。
Q: ブタンライターを補充するにはどうすればよいですか?
A: 水素化ブチルライターに燃料を充填するには、まず充填バルブ (通常は底部) を見つけます。水素化ブチル ノズルをバルブに挿入し、内腔がいっぱいになるまでしっかりと押して、内腔に水素化ブチルを放出します。
Q: 次の化合物のうち、ブタンの構造異性体はどれですか?
A: ペンタン (C5H12) は、両方の化合物に 4 つの炭素原子が含まれていますが、配置が異なるため、水素化ブチルの構造異性体です。
Q: ブタンライターを補充するにはどうすればよいですか?
A: 水素化ブチルライターを補充するには、ライターを逆さに持ち、水素化ブチル補充カートリッジのノズルをライターの補充バルブに合わせ、カートリッジをしっかりと押してブチルからライター内に水素化物を放出します。
Q: 近くでブタンはどこで買えますか?
A: 水素化ブチルは、キャンプ用品や家庭用品を扱う地元のホームセンター、スーパーマーケット、コンビニエンス ストアで購入できます。
Q: ブタンはどこで買えますか?
A: 水素化ブチルは、オンライン小売店、ホームセンター、キャンプ用品店、一部のスーパーマーケットなど、さまざまな場所から購入できます。
Q: ブタンの融点 (C₄H₁₀) とオクタンの融点 (C₈H₁₈) を最もよく比較する記述はどれですか?
A: オクタンはより大きく、より複雑な分子構造を持ち、一般に水素化ブチルよりも高い融点を持っています。
Q: ブタン、C₄H₁₀ のモル質量は何ですか?
A: 水素化ブチル (C4H10) のモル質量は、1 モルあたり約 58.12 グラムです。
Q: C₄H₁₀ にはいくつの異性体が考えられますか?
A: 水素化ブチル (C4H10) には、n-ブタン (ノルマルブタン) とイソブタン (2-メチルプロパン) の 2 つの異性体があります。
Q: 分子として存在すべき化合物 C4H10、SrCl2、Cr(NO3)3、OF2 のうちどれですか?
A: C4H10 (水素化ブチル) と OF2 (二フッ化酸素) は分子として存在すると考えられますが、SrCl2 と Cr(NO3)3 はイオン性化合物です。
