硫酸アンモニウム ((NH4)2SO4) は、植物に必須の栄養素を提供する広く使用されている肥料です。また、難燃剤、タンパク質の精製、食品添加物としても使用されます。
| IUPACの名称 | テトラオキソ硫酸アンモニウム(VI) |
| 分子式 | (NH4)2SO4 |
| CAS番号 | 7783-20-2 |
| 同義語 | 硫酸アンモニウム、硫酸アンモニウム(2:1)、硫酸二アンモニウム、硫酸二アンモニウム塩、マスカグナイト、アクタマスター、ドラミン |
| インチチ | InChI=1S/2H3N.H2O4S/c;;1-5(2,3)4/h2*1H3;(H2,1,2,3,4) |
硫酸アンモニウムの性質
硫酸アンモニウムの式
硫酸アンモニウムの式は (NH4)2SO4 です。これは、硫酸アンモニウム 1 分子中に 2 つのアンモニウム イオン (NH4)+ と 1 つの硫酸イオン (SO4)2- が含まれていることを意味します。アンモニウムイオンと硫酸イオンはイオン結合によって結合されています。
硫酸アンモニウムのモル質量
(NH4)2SO4 のモル質量は 132.14 g/mol です。モル質量を計算するには、式内のすべての原子の原子質量を合計する必要があります。原子質量は次のとおりです。
- 窒素: 14.01 g/mol
- 水素: 1.01 g/mol
- 硫黄: 32.06 g/mol
- 酸素: 16.00 g/mol
したがって、(NH4)2SO4 のモル質量は次のようになります。
(2 x 14.01) + (8 x 1.01) + 32.06 + (4 x 16.00) = 132.14 g/mol
硫酸アンモニウムの沸点
(NH4)2SO4 の沸点は、沸点に達する前に分解するため、明確に定義されていません。 235°C 以上に加熱すると、(NH4)2SO4 は水分を失い始め、硫酸水素アンモニウム (NH4)HSO4 を形成します。 280℃以上に加熱すると、重硫酸アンモニウムはさらにアンモニア (NH3) と硫酸 (H2SO4) に分解します。
硫酸アンモニウム 融点
(NH4)2SO4 の融点は 235°C です。これは、(NH4)2SO4 が固体から液体に変化する温度です。ただし、上で述べたように、(NH4)2SO4 もこの温度で分解し始めるため、純粋な液相ではありません。
硫酸アンモニウムの密度 g/ml
(NH4)2SO4 の密度は、室温および常圧で 1.77 g/ml です。これは、1 ミリリットルの (NH4)2SO4 の重さが 1.77 グラムであることを意味します。物質の密度は温度と圧力に依存するため、条件が異なるとわずかに変化する可能性があります。
硫酸アンモニウムの分子量
(NH4)2SO4 の分子量はそのモル質量と同じで、132.14 g/mol です。分子量は物質 1 モルの質量であり、6.022 x 10^23 分子に相当します。分子量は、炭素 12 原子の質量の 1/12 に等しい原子質量単位 (amu) で表すこともできます。 amu では、(NH4)2SO4 の分子量は 132.14 amu です。
硫酸アンモニウムの構造
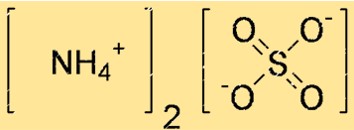
(NH4)2SO4 の構造は、ルイスドット構造または球と棒のモデルで表すことができます。ルイス ドット構造は、各原子の価電子と原子間の結合を示します。ボールとスティックのモデルは、各原子の形状とサイズ、および原子間の結合を示します。
上記の構造では、二重線 (=) は二重結合を表し、単線 (-) は単結合を表し、点 (.) は非共有電子対を表します。
硫酸アンモニウムの溶解度
(NH4)2SO4 の溶解度は、所定の温度で所定量の水に溶解できる (NH4)2SO4 の量です。次のデータに示すように、(NH4)2SO4 の溶解度は温度の上昇とともに増加します。
| 温度(℃) | 溶解度(g/水100ml) |
| 0 | 70.6 |
| 外観 | 微細な白色の吸湿性顆粒または結晶 |
| 比重 | 1.77 |
| 色 | 白 |
| 匂い | 無臭 |
| モル質量 | 132.14 g/モル |
| 密度 | 1.77g/cm3 |
| 融合点 | 235~280℃(分解) |
| 沸点 | 該当なし(分解) |
| フラッシュドット | 不燃性 |
| 水への溶解度 | 水100gあたり70.6g(0℃)、水100gあたり74.4g(20℃)、水100gあたり103.8g(100℃) |
| 溶解性 | アセトン、アルコール、エーテルに不溶 |
| 蒸気圧 | 無視できる |
| 蒸気密度 | 適用できない |
| pKa | 5.5 (アンモニウムイオンの場合) |
| pH | 5 ~ 6 (5% 溶液の場合) |
硫酸アンモニウムの安全性と危険性
(NH4)2SO4 は人間の健康にそれほど危険ではありませんが、接触または吸入すると皮膚、目、鼻、喉に炎症を引き起こす可能性があります。また、摂取すると吐き気、腹痛、下痢、嘔吐、眠気を引き起こす可能性があります。それは水生生物に有害であり、環境への放出は避けるべきです。 235℃以上に加熱すると分解し、アンモニアや硫酸などの有毒ガスを生成します。一般に食品添加物として安全であると認識されていますが、人によってはアレルギー反応や喘息の症状を引き起こす可能性があります。
| ハザードシンボル | 必要はありません |
| セキュリティの説明 | 環境への放出を避けてください。内容物/容器は認可された廃棄物処理施設に廃棄してください。 |
| 国連識別番号 | 適用できない |
| HSコード | 31022100 |
| 危険等級 | 適用できない |
| 梱包グループ | 適用できない |
| 毒性 | LD50 (経口、ラット) = 2.840 mg/kg |
硫酸アンモニウムの合成方法
(NH4)2SO4は無機塩であるため、さまざまな方法で合成できます。一般的な方法には次のようなものがあります。
2NH3 + H2SO4 -> (NH4)2SO4
(NH4)2CO3 + CaSO4 -> (NH4)2SO4 + CaCO3
- 他のプロセスの副産物: コークス炉ガス精製、カプロラクタム製造、ニッケル精製、排煙脱硫などのさまざまな工業プロセスでは、副産物として (NH4)2SO4 が生成される可能性があります。これらのプロセスでは、アンモニアまたはアンモニウム化合物を使用してガス流から硫黄またはその他の不純物を除去し、その結果、廃棄物または有価生成物として (NH4)2SO4 が生成されます。
硫酸アンモニウムの用途
(NH4)2SO4 は、次のようなさまざまな用途がある無機塩です。
- アルカリ性土壌肥料: (NH4)2SO4 は土壌の pH を下げ、植物の成長に窒素と硫黄を供給します。ブルーベリー、ジャガイモ、トマトなど、酸性土壌を必要とする作物に適しています。
- 農業用スプレーアジュバント: (NH4)2SO4 は、水溶性の殺虫剤、除草剤、殺菌剤の作用を妨げる可能性のある鉄イオンやカルシウムイオンを結合することにより、その効果を向上させます。また、植物によるグリホサートや他の浸透性除草剤の取り込みも改善します。
- タンパク質の精製: (NH4)2SO4 は、イオン強度を高め、タンパク質の溶解度を低下させることにより、水溶液からタンパク質を沈殿させることができます。塩析法は、サイズ、電荷、疎水性に基づいてタンパク質を分離するために使用できます。
- 食品添加物: パン、チーズ、ワイン、野菜の缶詰などのさまざまな食品では、(NH4)2SO4 が酸性度調整剤、生地調整剤、酵母栄養剤、および引き締め剤として使用されています。 FDA はそれが一般的に安全であると認めています。
- その他の用途: (NH4)2SO4 は、他のアンモニウム塩、消火剤、難燃剤、革のなめし、繊維の染色、金属電気メッキ、分析化学の製造に使用できます。
質問:
Q: 硫酸アンモニウムの化学式は何ですか?
A: 硫酸アンモニウムの化学式は (NH4)2SO4 です。これは、硫酸アンモニウム 1 分子中に 2 つのアンモニウム イオン (NH4)+ と 1 つの硫酸イオン (SO4)2- が含まれていることを意味します。
Q: 硫酸アンモニウムは溶けますか?
A: (NH4)2SO4 は水に溶けますが、アセトン、アルコール、エーテルには溶けません。 0℃では水100グラム当たり70.6グラム、20℃では水100グラム当たり74.4グラム、100℃では水100グラム当たり103.8グラムを溶解することができる。
Q: 水 1 ガロンあたりの硫酸アンモニウムの量はどれくらいですか?
A: 水 1 ガロンあたりの (NH4)2SO4 の量は、目的の濃度と水の温度によって異なります。たとえば、目的の濃度が 10% (w/v) で水温が 20°C の場合、水 1 ガロンあたりの (NH4)2SO4 の量は次のようになります。
10% (w/v) = 水 100 ml あたり 10 グラム 1 ガロン = 3785.41 ml 10 グラム x 3785.41 ml / 100 ml = 378.54 グラム したがって、水 1 ガロンあたりの (NH4)2SO4 の量は 378.54 グラムです。
Q:硫酸アンモニウムと塩化カルシウムの水溶液を混ぜると反応は起こりますか?
A: いいえ、(NH4)2SO4 水溶液と塩化カルシウムを混ぜても反応は起こりません。実際、これら 2 つの塩は水溶性であり、不溶性の沈殿物を形成しません。得られた溶液には、アンモニウム (NH4)+、硫酸塩 (SO4)2-、カルシウム (Ca2+)、および塩化物 (Cl)- の 4 つのイオンが含まれています。
Q: 硫酸アンモニウムでタンパク質を沈殿させるにはどうすればよいですか?
A: (NH4)2SO4 を使用してタンパク質を沈殿させるには、次の手順に従うことができます。
- 既知の濃度と体積の (NH4)2SO4 水溶液を準備します。
- タンパク質溶液を (NH4)2SO4 溶液にゆっくりと撹拌しながら加えます。
- 混合物の濁度または光学密度を監視して、タンパク質の沈殿量を決定します。
- 混合物を遠心分離して、タンパク質ペレットを上清から分離します。
- 上清を捨て、タンパク質ペレットを緩衝液または水で洗浄して過剰な塩を除去します。
- さらなる分析または使用のために、タンパク質ペレットを適切なバッファーに再懸濁または可溶化します。
Q: 硫酸アンモニウム 6.90 分子は何グラムですか?
A: 6.90 分子の (NH4)2SO4 が何グラムであるかを調べるには、アボガドロ数と (NH4)2SO4 のモル質量を使用する必要があります。アボガドロ数は 6.022 x 10^23 であり、これは、任意の物質の 1 モルに同じ数の分子が含まれていることを意味します。 (NH4)2SO4 のモル質量は 132.14 g/mol です。これは、1 モルの (NH4)2SO4 の重さが何グラムであることを意味します。したがって、この式を使用して、6.90 分子の (NH4)2SO4 が何グラムであるかを計算できます。
グラム = 分子 x モル質量 / アボガドロ数 グラム = 6.90 x 132.14 / 6.022 x 10^23 グラム = 1.52 x 10^-21 したがって、6.90 分子の (NH4)2SO4 分子には 1.52 x 10^-21 グラムが含まれます。
Q: 硫酸アンモニウムにはどのくらいの硫黄が含まれていますか?
A: (NH4)2SO4 には 24 質量%の硫黄が含まれています。これは、組成パーセント式と硫黄と (NH4)2SO4 のモル質量を使用して計算できます。硫黄のモル質量は 32.06 g/mol、(NH4)2SO4 のモル質量は 132.14 g/mol です。したがって、(NH4)2SO4 中の硫黄の割合は次のようになります。
パーセンテージ = 硫黄のモル質量 x 100 / 硫酸アンモニウムのモル質量 パーセンテージ = 32.06 x 100 / 132.14 パーセンテージ = 24.26%
Q: 次の塩のうち、中性塩はどれですか? na2so4 nacn kf (nh4)2so4
A: 中性塩は、水に溶解したときに溶液の pH に影響を与えない塩です。強酸と強塩基の反応によって生成されます。与えられた 4 つの塩のうち、na2so4 だけが中性塩です。水酸化ナトリウム (強塩基) と硫酸 (強酸) の反応によって生成されます。他の塩は酸性または塩基性のいずれかです。 Nacn は、水酸化ナトリウム (強塩基) と青酸 (弱酸) の反応によって形成される塩基性塩です。 Kf は、水酸化カリウム (強塩基) とフッ化水素酸 (弱酸) の反応によって形成される塩基性塩です。 (Nh4)2so4 は、水酸化アンモニウム (弱塩基) と硫酸 (強酸) の反応によって形成される酸塩です。
Q: (nh4)2so4 のモル質量はいくらですか?
A: (nh4)2so4 のモル質量は 132.14 g/mol です。モル質量を求めるには、式内のすべての原子の原子質量を合計する必要があります。原子質量は次のとおりです。
- 窒素: 14.01 g/mol
- 水素: 1.01 g/mol
- 硫黄: 32.06 g/mol
- 酸素: 16.00 g/mol
したがって、(nh4)2so4 のモル質量は次のようになります。
(2 x 14.01) + (8 x 1.01) + 32.06 + (4 x 16.00) = 132.14 g/mol
Q: (nh4)2so4 は水に溶けますか?
A: はい、(nh4)2so4 は水に溶けます。 0℃では水 100 グラムあたり 70.6 グラム、20℃では水 100 グラムあたり 74.4 グラム、100 ℃では水 100 グラムあたり 103.8 グラムまで溶解できます。
