七酸化塩素または Cl2O7 は、爆発性と反応性が非常に高い化合物です。有機物と接触すると激しく分解する可能性があり、化学合成や分析に使用される強力な酸化剤です。
| IUPAC名 | 七酸化塩素 |
| 分子式 | Cl2O7 |
| CAS番号 | 12015-53-1 |
| 同義語 | 無水過塩素酸、七酸化二塩素、酸化塩素(VII)、酸化塩素、過塩素酸パーククロリル |
| インチチ | InChI=1S/Cl2O7/c2-1(3,4,5,6)10-7(8,9)11-12-13-14-10 |
七酸化塩素モル質量
七酸化塩素、化学式 Cl2O7 のモル質量は 182.9 g/mol です。この化合物は 2 つの塩素原子と 7 つの酸素原子で構成されており、強い酸化力を持っています。七酸化塩素のモル質量は、アボガドロ定数を使用してサンプルの特定の質量または体積に含まれる物質の量を計算するために使用されます。
七酸化塩素の沸点
七酸化塩素は、無色から黄色がかった、反応性が高く揮発性の固体です。七酸化塩素は沸点に達する前に分解するため、沸点は明確に定義されていません。七酸化塩素は、有機物、水、その他の物質と反応して爆発性化合物を形成する強力な酸化剤です。
七酸化塩素の融点
七酸化塩素の融点は -96°C (-141°F) で、低融点の固体です。七酸化塩素は、融点が低く反応性が高いため、室温では黄色がかった液体として存在します。七酸化塩素は重度の火傷を引き起こす可能性があり、強力な酸化剤であるため、慎重に取り扱うことが重要です。
七酸化塩素の密度 g/ml
七酸化塩素の密度は室温で 2.48 g/mL です。七酸化塩素は密度が高いため、濃厚な液体となり、すぐに容器の底に沈んでしまいます。七酸化塩素は高密度で反応性が高いため、取り扱いが難しい化合物であり、化学合成や分析で使用する場合には特別な安全上の注意が必要です。
七酸化塩素の分子量
七酸化塩素の分子量は相対分子量としても知られ、182.9 g/mol です。七酸化塩素の分子量は、物質の量、質量、体積を含む化学計算において重要です。七酸化塩素は分子量が高いため、高密度で揮発性の化合物となり、慎重な取り扱いと保管が必要です。
七酸化塩素の構造
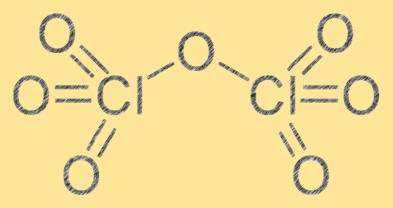
七酸化塩素の構造は、2 つの塩素原子と 7 つの酸素原子で構成されています。分子式は Cl2O7 であり、その分子幾何学は酸素原子間の反発により歪んだ八面体形状をしています。七酸化塩素は強力な酸化剤であり、さまざまな有機および無機物質と反応する可能性があります。七酸化塩素の構造は、その化学的特性とさまざまな反応における挙動を理解するために不可欠です。
七酸化塩素の式
七酸化塩素の化学式は Cl2O7 です。この式は、七酸化塩素の各分子に 2 つの塩素原子と 7 つの酸素原子が含まれていることを示しています。この式は、七酸化塩素が関与する化学反応の化学量論を計算するために使用されます。七酸化塩素の式は、その分子量、密度、その他の物理的および化学的特性を決定する際にも重要です。
| 外観 | 無色から黄色がかった固体 |
| 比重 | 25℃で2.48 |
| 色 | 無色~黄色っぽい |
| 匂い | 辛い、酸っぱい |
| モル質量 | 182.9g/モル |
| 密度 | 2.48 g/mL(25℃) |
| 融合点 | -96°C (-141°F) |
| 沸点 | 沸点前に分解する |
| フラッシュドット | 適用できない |
| 水への溶解度 | 水と激しく反応する |
| 溶解性 | 有機溶剤に可溶 |
| 蒸気圧 | 利用不可 |
| 蒸気密度 | 利用不可 |
| pKa | 利用不可 |
| pH | 適用できない |
七酸化塩素の安全性と危険性
七酸化塩素は反応性が高く危険な化合物であり、適切に取り扱わないと重大な安全上のリスクが生じます。接触すると重度の火傷や目、皮膚、呼吸器系への損傷を引き起こす可能性があります。七酸化塩素は水や有機物質と激しく反応し、爆発や火災の危険を引き起こす可能性があります。七酸化塩素を取り扱う際には、手袋、ゴーグル、マスクなどの適切な個人用保護具を使用することが不可欠です。化合物は、発火源、熱源、または湿気の源から離れた、しっかりと密閉された容器に入れて保管および輸送する必要があります。七酸化塩素に関連するリスクを最小限に抑えるために、適切な取り扱い手順と安全上の注意事項に従う必要があります。
| ハザードシンボル | 酸化剤、腐食性 |
| セキュリティの説明 | 水、酸、有機物質、還元剤との接触を避けてください。適切な個人用保護具を使用してください。熱、湿気、発火源を避け、密閉した容器に保管してください。目、皮膚、呼吸器系に接触した場合は、直ちに医師の診察を受けてください。 |
| 国連識別番号 | 国連 3083 |
| HSコード | 28299090 |
| 危険等級 | 5.1 (酸化性物質) |
| 梱包グループ | Ⅱ |
| 毒性 | 吸入、経口摂取、または皮膚からの吸収により非常に有毒です。重度の火傷や組織損傷を引き起こします。水、有機物質、その他の反応性物質と接触すると、爆発や火災の危険を引き起こす可能性があります。 |
七酸化塩素の合成方法
七酸化塩素は反応性が高く、合成が困難な化合物です。
七酸化塩素を合成する最も一般的な方法の 1 つは、塩素ガスとオゾンを反応させることによるものです。この反応は発熱性であり、注意深く制御しないと爆発反応を引き起こす可能性があります。
別の方法では、塩素ガスと塩素酸カリウムを反応させ、副生成物として七酸化塩素と塩化カリウムを生成します。この方法では、爆発性中間体の生成を防ぐために反応条件を注意深く制御する必要もあります。
七酸化塩素は、塩素ガスを五酸化二塩素と反応させることによって合成でき、副生成物として七酸化塩素と六酸化二塩素が生成します。ただし、五酸化二塩素の危険な性質のため、研究者はこの方法を一般的に使用しません。
七酸化塩素を合成する他の方法には、制御された条件下で塩素ガスをベンゼンやトルエンなどのさまざまな有機化合物と反応させることが含まれます。ただし、これらの方法は反応条件を慎重に最適化する必要があり、塩素-オゾンまたは塩素-塩素酸カリウムの方法ほど信頼性がなく、一般的に使用されていません。
全体として、七酸化塩素の合成には反応条件の注意深い制御が必要であり、化合物の反応性が高いため、重大な安全上のリスクが伴います。七酸化塩素やその他の危険物質を扱う場合は、安全上の注意事項と適切な取り扱い手順に従う必要があります。
七酸化塩素の用途
- Cl2O7 は、化学合成および研究における酸化剤として主に使用されます。
- 強力な酸化剤として作用し、広範囲の有機および無機化合物と反応するため、多くの化学反応に役立ちます。
- Cl2O7 の最も一般的な用途の 1 つは、水処理、紙パルプ製造、繊維製造で使用される強力な消毒剤および漂白剤である二酸化塩素の製造です。
- また、医薬品や農薬を含むいくつかの有機化合物の合成において強力な酸化剤としても使用されます。
- Cl2O7 は、さまざまな有機および無機化合物の反応性を研究するために学術および研究で使用されています。また、エポキシ樹脂や無水酢酸などの特定の化合物の合成における触媒としても機能します。
- 危険な性質のため、大規模な産業用途では通常、Cl2O7 は使用されません。爆発性中間体の生成やその他の安全上の危険を避けるために、慎重な取り扱いと保管が必要です。
全体として、Cl2O7 は化学合成や研究において有用な化合物ですが、その使用に伴うリスクを最小限に抑えるためには、安全上の注意と適切な取り扱い手順が必要です。
質問:
Q: Cl2O7とは何ですか?
A: Cl2O7 は、2 つの塩素原子と 7 つの酸素原子で構成される化学式 Cl2O7 の化合物です。
Q: Cl2O7 の正しい名前は何ですか?
A: Cl2O7 の正しい名前は七酸化二塩素です。
Q: Cl2O7 はイオン性ですか、それとも共有結合性ですか?
A: Cl2O7 は共有結合性化合物です。塩素と酸素という 2 つの非金属元素で構成され、原子間の電子の共有により分子化合物を形成します。
Q: 水と反応して弱酸を生成する酸化物は次のうちどれですか? MgO、Cl2O7、P4O10、Bi2O3、N2O5。
A: 水と反応して弱酸を生成する酸化物は N2O5 です。 N2O5 が水と反応すると、弱酸である硝酸が生成されます。リストされている他の酸化物、MgO、P4O10、Bi2O3、および Cl2O7 は、水と反応して弱酸を形成しません。
