塩化アセチルまたは C2H3ClO は、刺激臭のある無色の発煙液体です。主に有機合成の試薬として、また医薬品や染料の製造ではアセチル化剤として使用されます。
| UPAC名 | 塩化アセチル |
| 分子式 | C2H3ClO |
| CAS番号 | 75-36-5 |
| 同義語 | 塩化エタノイル、塩化酢酸、塩化酢酸、クロロアセチルクロリド、AcCl |
| インチチ | InChI=1S/C2H3ClO/c1-2(3)4/h1H3 |
塩化アセチルの性質
塩化アセチル モル質量
化学式 C2H3ClO の塩化アセチルのモル質量は約 78.50 g/mol です。これは、分子内の各原子の原子質量、つまり炭素 (12.01 g/mol)、水素 (1.01 g/mol)、塩素 (35.45 g/mol)、酸素 (16.00 g/mol) を加算することによって計算されます。塩化アセチルのモル質量は、化学反応における反応物と生成物の量を決定するための化学量論的計算において重要です。
塩化アセチルの沸点
塩化アセチルの沸点は、標準大気圧で 51.5°C (124.7°F) です。この沸点が低いことと、反応性が高い性質があるため、実験室では塩化アセチルを慎重に取り扱う必要があります。これは刺激臭のある無色の発煙性液体で、エタノールやアセトンなどの極性溶媒によく溶けます。
塩化アセチルの融点
C2H3ClO の融点は、標準大気圧で -112.1°C (-169.8°F) です。このため、揮発性が高く反応性の高い化合物となるため、慎重な取り扱いと保管が必要になります。
塩化アセチルの密度 g/mL
塩化アセチルの密度は 25°C (77°F) で 1.104 g/mL です。これは、C2H3ClO は水よりも密度が高く、水に沈むことを意味します。 C2H3ClO の密度は、所定の体積にどれだけの物質を保管できるか、また物質の取り扱いと保管に必要な適切な安全対策を決定する上で重要です。
塩化アセチルの分子量
C2H3ClO の分子量は 78.50 g/mol です。この値は、化学反応に必要な C2H3ClO の量を決定したり、異なる測定単位間で変換したりするために重要です。
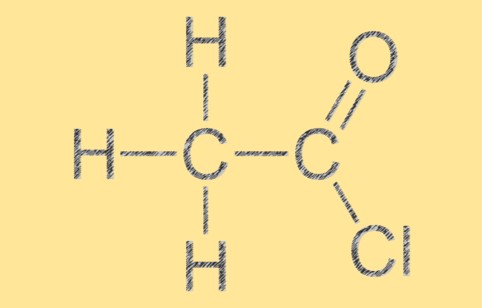
塩化アセチルの構造
塩化アセチルは三角形の平面分子構造を持ち、中心の炭素原子が他の 3 つの原子に囲まれて平面的な三角形の配置になっています。この分子には、炭素原子と酸素原子の間に C=O 二重結合があり、炭素原子と塩素原子の間に単結合があります。 C2H3ClO の分子構造により、C2H3ClO に特有の反応性と化学的特性が与えられます。
塩化アセチルの配合
塩化アセチルの化学式は C2H3ClO で、これは分子内の原子の数と種類を表します。この式は、化学反応における化学量論計算や実験室での化合物の特定に重要です。 C2H3ClO は、主に有機合成の試薬として、また医薬品や染料の製造ではアセチル化剤として使用されます。
| 外観 | 無色の液体 |
| 比重 | 1.104 g/ml(25℃) |
| 色 | 無色 |
| 匂い | エーカー |
| モル質量 | 78.50g/モル |
| 密度 | 1.104 g/ml(25℃) |
| 融合点 | -112.1℃ |
| 沸点 | 51.5℃ |
| フラッシュドット | -26℃ |
| 水への溶解度 | 水と激しく反応する |
| 溶解性 | ほとんどの有機溶媒に可溶 |
| 蒸気圧 | 25℃で69.7mmHg |
| 蒸気密度 | 2.7 (空気=1) |
| pKa | -6.3 |
| pH | 非常に酸性 |
塩化アセチルの安全性と危険性
C2H3ClO は反応性が高く、人間の健康と安全に重大なリスクをもたらす危険な物質です。これは腐食性で有毒な物質であり、暴露されると重度の皮膚の火傷、目の損傷、呼吸器への炎症を引き起こす可能性があります。塩化アセチルは水と激しく反応して、呼吸器への刺激物である塩酸ガスを生成することもあります。 C2H3ClO の取り扱いには細心の注意を払い、適切な個人用保護具を着用し、換気の良い場所でのみ使用することが重要です。事故を防止し、この物質を安全に取り扱うためには、適切な保管、ラベル貼付、輸送も不可欠です。
| ハザードシンボル | 腐食性、有毒性 |
| セキュリティの説明 | 蒸気を吸い込まないでください。保護手袋と目/顔の保護具を着用してください。火災が発生した場合は、CO2、粉末消火器、または泡消火器を使用してください。 |
| AN識別子 | UN1717 |
| HSコード | 2915.90.9000 |
| 危険等級 | 8 |
| 梱包グループ | Ⅱ |
| 毒性 | 非常に有毒で腐食性があります。重篤な皮膚や目の火傷を引き起こします。吸い込んだり飲み込んだりすると致命的な危険があります。 |
塩化アセチルの合成方法
C2H3ClO は、酢酸と塩化チオニル、三塩化リン、または五塩化リンを反応させることによって生成されます。これらの方法には、反応性が高く危険な試薬が使用されるため、細心の注意を払って使用する必要があります。
C2H3ClO を合成する最も一般的な方法には、酢酸と塩化チオニルの反応が含まれます。この方法では通常、過熱や分解を防ぐために慎重な温度制御を行いながら、制御された方法で塩化チオニルを酢酸に添加します。この反応により、副生成物として C2H3ClO と二酸化硫黄ガスが生成されます。
C2H3ClOを合成する別の方法には、酢酸と三塩化リンまたは五塩化リンとの反応が含まれます。この方法では、酢酸と三塩化リンまたは五塩化リンを混合し、加熱して反応を開始します。この反応により、副生成物として C2H3ClO とリン酸が生成されます。
これらの方法には反応性が高く危険な化学物質が使用されているため、換気の良い場所で適切な個人用保護具を着用した経験豊富な化学者のみが実行する必要があることに注意することが重要です。さらに、C2H3ClO の合成は、有毒ガスや腐食性ガスへの曝露を最小限に抑えるために、ドラフト内で実行する必要があります。
塩化アセチルの用途
塩化アセチルは、産業や研究で多くの用途に使用される多用途の化合物です。 C2H3ClO の一般的な用途には次のようなものがあります。
- 医薬品の製造: 鎮痛剤、抗生物質、麻酔薬などのさまざまな医薬品の合成には C2H3ClO が使用されます。
- 染料と香料の製造: 香水や石鹸に使用されるクマリンなど、さまざまな染料や香料の製造には C2H3ClO が使用されます。
- ポリマー製造: 反応物として C2H3ClO に結合したポリカーボネートやポリ塩化ビニルなどのさまざまなポリマーの製造。
- アセチル化誘導体の生成: C2H3ClO は、アミノ酸やアルコールなどの化合物のアセチル化誘導体の生成に重要な役割を果たします。
- 化学反応: C2H3ClO は高い反応性を示し、アセチル化反応やフリーデルクラフツ反応などのさまざまな化学反応において貴重な試薬となります。
- 実験室研究: C2H3ClO は、化学反応の試薬やさまざまな化合物の溶媒として、実験室研究で頻繁に使用されます。
C2H3ClO は危険物質であり、細心の注意を払って取り扱う必要があることに注意することが重要です。 C2H3ClO を使用する場合は、その取り扱いと使用に伴うリスクを最小限に抑えるために、適切な安全プロトコルと規制に従う必要があります。
