酸化アンモニウム ((NH4)2O) は、水に溶け、弱塩基として作用する白色の結晶性化合物です。アンモニアと酸素の反応によって生成され、肥料、洗浄剤、消火剤として使用されます。
| IUPAC名 | 酸化アンモニウム |
| 分子式 | (NH4)2O |
| CAS番号 | 12046-03-6 |
| 同義語 | 水酸化アンモニウム、アンモニア水、アンモニア水 |
| インチチ | InChI=1S/H4N.O/h1H4;/q+1;-1 |
酸化アンモニウムの性質
酸化アンモニウムの配合
酸化アンモニウムの式は (NH4)2O です。窒素原子1個と水素原子4個が酸素原子1個と結合した化合物です。
酸化アンモニウムのモル質量
酸化アンモニウムのモル質量は、1 モルあたり約 52.07 グラムです。分子内に存在するすべての原子の原子量を加算することによって計算されます。モル質量は、特定の量の物質中に存在する粒子の数を決定するのに役立ちます。
酸化アンモニウムの沸点
(NH4)2O の沸点は約 90℃です。これは、液体の蒸気圧が周囲の圧力と等しくなり、液体が気体に変わる温度です。物質の沸点は、さまざまな化合物を識別および区別するために使用できる重要な物理的特性です。
酸化アンモニウムの融点
(NH4)2O の融点は約 -6°C です。これは固体が液体に変わる温度です。物質の融点は、物質の純度を決定するだけでなく、さまざまな化合物を識別および区別するために使用できます。
酸化アンモニウムの密度 g/ml
(NH4)2O の密度は約 1.02 g/ml です。密度は単位体積あたりの質量であり、物質の基本的な物理的特性です。物質の密度は、物質の純度を決定するだけでなく、さまざまな化合物を識別および区別するために使用できます。
酸化アンモニウムの分子量
酸化アンモニウムの分子量は約 52.07 g/mol です。物質の分子内に存在するすべての原子の原子量の合計です。分子量は、特定の質量内に存在する物質のモルを計算するために使用でき、科学の多くの分野で使用される重要な物理的特性です。
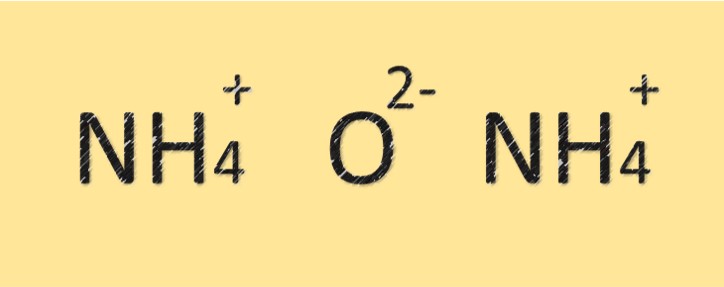
酸化アンモニウムの構造
酸化アンモニウムは窒素原子と酸素原子から構成される化合物です。分子式は (NH4)2O で、2 つの窒素原子と 1 つの酸素原子で構成されています。窒素原子は共有結合によって酸素原子と結合しており、正電荷を持っています。この化合物はアンモニウムイオンの存在により、塩基性またはアルカリ性の性質を持ちます。
| 外観 | 白色の結晶固体 |
| 比重 | 1.02g/cm3 |
| 色 | 白 |
| 匂い | アンモニア |
| モル質量 | 52.07g/モル |
| 密度 | 1.02g/cm3 |
| 融合点 | -6℃ |
| 沸点 | 90℃ |
| フラッシュドット | 該当なし |
| 水への溶解度 | 可溶性 |
| 溶解性 | 水に溶ける |
| 蒸気圧 | 該当なし |
| 蒸気密度 | 該当なし |
| pKa | 該当なし |
| pH | 11.6 (100 g/L、H2O、20℃) |
酸化アンモニウムの安全性と危険性
(NH4)2O は目、皮膚、呼吸器系を刺激します。その蒸気を吸入すると、咳、息切れ、肺への炎症を引き起こす可能性があります。皮膚に接触するとかゆみや発赤を引き起こす場合があります。化合物は慎重に取り扱う必要があり、手袋や保護眼鏡などの保護手段を使用する必要があります。暴露した場合は、患部を水で洗い流し、症状が続く場合は医師の診察を受ける必要があります。また、可燃性があるため、発火源から遠ざけて保管する必要があります。
| ハザードシンボル | 刺激物 |
| セキュリティの説明 | S26-S36/37/39 |
| 国連識別番号 | UN2672 |
| HSコード | 2841.90.90 |
| 危険等級 | 8 |
| 梱包グループ | Ⅲ |
| 毒性 | 目、皮膚、呼吸器系を刺激する |
酸化アンモニウムの合成方法
(NH4)2O は、硝酸アンモニウムの熱分解やアンモニアガスと酸素ガスの反応など、いくつかの方法で合成できます。
1 つの方法には、一般的な肥料である硝酸アンモニウムの熱分解が含まれます。この反応によりアンモニアと二酸化窒素が生成され、これらは次に二酸化窒素と一酸化窒素に酸化されます。一酸化窒素はさらにアンモニアガスと反応して (NH4)2O を形成します。
別の方法では、加熱した触媒上にアンモニア ガスを通過させ、窒素原子と酸素原子を結合させて (NH4)2O を形成します。これらの方法は両方とも、(NH4)2O を白色の結晶性固体として生成します。これは再結晶によって精製できます。
酸化アンモニウムの用途
(NH4)2O は、アンモニウム含有量が高く、アルカリ性が強いため、産業界ではさまざまな目的に使用されています。肥料として植物に窒素源を提供します。洗浄剤は油や汚れを溶かすために使用されます。冶金産業では、特にアルミニウムの製造において、金属酸化物の還元剤として使用されます。冷媒として、工業用冷却システムや硝酸の製造における窒素源として使用されます。研究室では、化学者は化学反応のためのアンモニア源としてそれを使用します。 (NH4)2O は多用途性を備えているため、あらゆる分野で複数の用途に使用できる貴重な化学物質となっています。
