ホスゲンは、工業プロセスや戦争で使用される有毒ガスです。それを吸い込むと重大な健康リスクが生じ、呼吸器損傷を引き起こし、死に至る可能性があります。
| IUPAC名 | 二塩化カルボニル |
| 分子式 | COCl2 |
| CAS番号 | 75-44-5 |
| 同義語 | 二塩化炭酸、ホスゲンガス、塩化カルボニル |
| インチチ | InChI=1S/CCl2O/c2-1(3)4 |
ホスゲンの性質
ホスゲン配合
ホスゲンまたは二塩化炭素の化学式は COCl2 です。 1 つの炭素原子 (C)、1 つの酸素原子 (O)、2 つの塩素原子 (Cl) で構成されています。この分子組成は、その特性と反応を理解するために不可欠です。
ホスゲンのモル質量
二塩化炭素のモル質量は約 98.92 g/mol です。これは、その構成要素である炭素 (12.01 g/mol)、酸素 (16.00 g/mol)、塩素 (それぞれ 35.45 g/mol) の原子質量を加算することによって計算されます。
ホスゲンの沸点
二塩化炭酸の沸点は約 -23.3°C (-9.94°F) と比較的低くなります。この温度では、液体状態から気体状態に変化します。これは、さまざまな工業プロセスでの応用にとって重要です。
ホスゲンの融点
二酸化炭素の融点は非常に低く、約 -118.3°C (-180.94°F) です。この温度では、固体の二塩化炭素が液体に変わります。この性質を理解することは、二塩化炭素を安全に取り扱うために重要です。
ホスゲン密度 g/mL
二塩化炭酸の密度は、室温 (25°C または 77°F) で約 1.432 g/mL です。この特性は、その挙動や他の物質との相互作用を決定する上で重要です。
ホスゲンの分子量
二塩化炭素の分子量は 98.92 g/mol です。この値は、化学量論や反応に必要な二塩化炭素の量の決定など、化学におけるさまざまな計算に不可欠です。
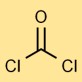
ホスゲンの構造
二塩化炭酸は、炭素原子が酸素原子と二重結合し、各塩素原子と単結合する直線状の分子構造を持っています。この配置は応答性と安定性に影響します。
ホスゲンの溶解度
二塩化炭酸は水に溶けにくく、液体中には少量のガスしか溶解しません。ただし、水と反応して塩酸と二酸化炭素を生成する可能性があるため、水環境では危険です。
二塩化炭酸のこれらの特性を理解することは、工業用途やその他の環境で化学物質を安全に取り扱い、使用するために不可欠です。この有毒で反応性の化合物を取り扱うときは、事故や健康被害を防ぐために常に適切な予防措置を講じる必要があります。
| 外観 | 無色の気体 |
| 比重 | 3.428 (ガス) |
| 色 | 該当なし |
| 匂い | 窒息する、刺すような |
| モル質量 | 98.92 g/モル |
| 密度 | 1,432g/mL(液体) |
| 融合点 | -118.3°C (-180.94°F) |
| 沸点 | -23.3°C (-9.94°F) |
| フラッシュドット | 該当なし |
| 水への溶解度 | 水と反応する |
| 溶解性 | 水と反応して塩酸と二酸化炭素を生成する |
| 蒸気圧 | 736mmHg(25℃) |
| 蒸気密度 | 2.98 (空気 = 1) |
| pKa | 該当なし |
| pH | 該当なし |
これらの物理化学的特性は、二塩化炭素に関する重要な情報を提供し、二塩化炭素の安全な取り扱いとさまざまな環境での挙動の理解を容易にします。
ホスゲンの安全性と危険性
二塩化炭酸は、その毒性と反応性の性質により、重大な安全上のリスクを引き起こします。二塩化炭素を取り扱う場合は、呼吸用保護具、手袋、目の保護具など、適切な個人用保護具 (PPE) を着用してください。吸入による暴露を避けるために、作業エリアでは十分な換気を確保してください。重篤な刺激や火傷を引き起こす可能性があるため、皮膚や目に接触しないようにしてください。二塩化炭素ガスは無臭なので、気づきにくいです。したがって、監視デバイスは非常に重要です。暴露した場合は、直ちに医師の診察を受けてください。規制とベストプラクティスに従って、二塩化炭素を安全に保管および輸送してください。その危険性を理解することは、事故を防止し、人間の健康と環境の両方を保護するために不可欠です。
| ハザードシンボル | どくろ |
| セキュリティの説明 | 非常に有毒なガス。取り扱いには細心の注意を払ってください。適切な PPE を使用してください。吸入や皮膚との接触を避けてください。 |
| 国連識別番号 | UN1076 |
| HSコード | 2812.10.0000 |
| 危険等級 | 2.3 (有毒ガス) |
| 梱包グループ | 私 |
| 毒性 | ホスゲンは毒性が高く、吸入したり皮膚に接触すると死亡する可能性があります。厳格なセキュリティ対策を講じてください。 |
二塩化炭素のリスクと安全性の側面を理解することは、安全な取り扱いと事故の防止にとって非常に重要です。毒性が高く、重大な健康リスクを引き起こすため、適切な安全手順と予防措置が不可欠です。
ホスゲンの合成法
いくつかの方法で二塩化炭素を合成できます。
一般的なアプローチは、塩化銅(II)などの適切な触媒の存在下、高温で塩素ガスを一酸化炭素と反応させる「ディーコンプロセス」です。別の方法には、塩素ガスによる一酸化炭素の「直接塩素化」が含まれ、これは触媒として鉄または他の金属塩化物によって促進されます。
二塩化炭酸の製造には、酸素と塩化第一銅などの金属触媒を使用した、塩化メチレンまたは塩化メチルの「酸化的カルボニル化」が含まれます。二塩化炭酸を合成する別の方法は、尿素製造中に副生成物として二塩化炭酸を生成する「尿素ルート」です。
ただし、二塩化炭素は非常に危険な物質であり、その合成には細心の注意と専門知識が必要であることに注意することが重要です。作業者は、有毒ガスへの曝露を回避し、作業者と環境の安全を確保するために、厳格な安全対策と保護具を備えた、よく管理された産業環境でこれらのプロセスを実行する必要があります。
ホスゲンの用途
二塩化炭酸は、その独特の特性によりさまざまな産業用途に使用されていますが、その毒性のため、その使用には細心の注意を払う必要があることに注意することが重要です。その用途の一部を次に示します。
- 化学中間体: 二塩化炭酸は、ポリウレタンフォーム、コーティング、接着剤の製造に重要な役割を果たすイソシアネートなど、いくつかの必須化学物質の生成に役立ちます。
- 殺虫剤の生産: 二塩化炭酸は特定の殺虫剤や除草剤の合成を促進し、作物の保護と害虫駆除に貢献します。
- ポリカーボネートの製造: 二酸化炭素は、眼鏡から水筒まで幅広い製品に使用されるポリカーボネート プラスチックの製造において重要な成分です。
- 繊維産業: 二塩化炭酸は、繊維産業で使用される特定の染料やその他の化学物質の製造に関与しています。
- 発泡体の製造: 二酸化炭素は、断熱材に使用されるある種の発泡体を含む発泡材料の製造において重要な役割を果たします。
- 医薬品: 二塩化炭酸は、特定の医薬品の製造における化学中間体として機能します。
- 実験室研究: 研究者は実験室での実験で二塩化炭素を使用することがあります。
- 合成ゴムの製造: 二酸化炭素は、一部の合成ゴムの製造に不可欠な部分です。
- 水の浄化: 以前は水の浄化に二塩化炭酸が少量使用されていましたが、現在ではより安全な代替品がこの目的でより一般的に使用されています。
二塩化炭素には重要な産業用途がありますが、その毒性と危険性が高いため、事故を防止し、労働者と人々の健康を確保するために、取り扱い、保管、輸送中に厳格な安全対策が必要です。環境。
質問:
Q: ホスゲンガスは人体にどのような影響を与えますか?
A: 二塩化炭素ガスは呼吸器損傷を引き起こし、呼吸困難や致命的な肺水腫を引き起こす可能性があります。
Q: ホスゲンとは何ですか?
A: 二酸化炭素は、さまざまな工業プロセスで使用される非常に有毒な化合物です。
Q: ホスゲンガスとは何ですか?
A: 二塩化炭素ガスは化合物のガス状であり、窒息や呼吸器系への有毒な影響で知られています。
Q: ホスゲンは体に何をしますか?
A: 二酸化炭素は肺を損傷し、体液の蓄積や重度の呼吸困難を引き起こす可能性があります。
Q: グリニャールはどのくらいの頻度でホスゲンと反応しますか?
A: グリニャール試薬は二塩化炭素と 1 回だけ反応し、ケトンを形成します。
Q: 塩素ガスとホスゲンは人間のどの臓器を攻撃しますか?
A: 塩素と二塩化炭素のガスは主に肺を攻撃します。
Q: ホスゲンガスはどのようにして人を殺すのですか?
A: 二塩化炭素ガスは肺に重度の炎症を引き起こし、体液の蓄積や窒息につながります。
Q: ホスゲンガスを発明したのは誰ですか?
A: 二酸化炭素ガスは、1812 年にイギリスの化学者ジョン デービーによって発見されました。
Q: 二塩化炭素ガスの影響はありますか?
A: 二塩化炭素ガスは呼吸器損傷、肺水腫を引き起こし、重篤な場合には死に至る可能性があります。
Q: 二酸化炭素のルイス構造は?
A: 二塩化炭酸のルイス構造は、酸素と二重結合した炭素と 2 つの塩素原子との単結合で構成されます。
Q: 二塩化炭素ガス 第一次世界大戦?
A: 二塩化炭素は第一次世界大戦中に化学兵器として使用され、兵士に壊滅的な影響を与えました。
Q: ホスゲンガスが初めて使用されたのはいつですか?
A: 二塩化炭素ガスは、1915 年の第一次世界大戦中に初めて化学兵器として使用されました。
Q: ホスゲンはどこから来たのですか?
A: 二酸化炭素は通常、塩素と一酸化炭素または他の炭素含有化合物を反応させることによって生成されます。
