塩化スルフリル (SO2Cl2) は、二酸化硫黄と塩素の組み合わせによって形成される化合物です。化学反応の試薬として、また害虫を駆除する燻蒸剤として使用されます。
| IUPAC名 | 塩化スルフリル |
| 分子式 | SO2Cl2 |
| CAS番号 | 7791-25-5 |
| 同義語 | 二塩化硫黄、オキシ塩化硫黄、二塩化硫黄酸化物 |
| インチチ | InChI=1S/Cl2O2S/c1-5(2)6(3)4 |
塩化スルフリルの性質
塩化スルフリルの式
二塩化硫酸の化学式はSO2Cl2です。それは、1 つの硫黄原子、2 つの酸素原子、2 つの塩素原子の組み合わせから派生します。この式は、二塩化硫酸分子内の原子の組成と配置を表します。
塩化スルフリル モル質量
二塩化硫酸のモル質量は、その構成元素の原子量を加算することで計算できます。二塩化硫酸のモル質量は 1 モルあたり約 134.97 グラムです。この値は、化学反応や化学量論のさまざまな計算にとって重要です。
塩化スルフリルの沸点
二塩化硫酸の沸点は約 69 ℃です。温度がこの点を超えると、二塩化硫酸は相変化を起こし、液体から気体に変化します。沸点は、二塩化硫酸の使用または取り扱いの条件を決定する際の重要なパラメータです。
塩化スルフリルの融点
二塩化硫酸の融点は約-54℃です。この温度より低い温度では、二塩化硫酸は固体から液体の状態に変化します。融点は、二塩化硫酸が凝固または液化する条件を示すため、二塩化硫酸の保管および取り扱いにとって重要です。
塩化スルフリルの密度 g/mL
二塩化硫酸の密度は約 1.638 グラム/ミリリットル (g/mL) です。密度は単位体積あたりの物質の質量を表し、その物理的挙動を決定するのに役立ちます。二塩化硫酸の密度は、その浮力、溶解度、他の物質との適合性を理解するために重要です。
塩化スルフリルの分子量
二塩化硫酸の分子量は約 134.97 原子質量単位 (u) です。これは、二塩化硫酸分子の構成原子の原子質量の合計です。分子量は、さまざまな化学計算や、特定のサンプル中の物質の量を決定するための重要な情報を提供します。
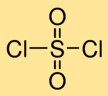
塩化スルフリルの構造
二塩化硫酸は、1 つの硫黄原子が 2 つの酸素原子に二重結合し、2 つの塩素原子と単結合した分子構造を持っています。この配置により、酸素原子と塩素原子に囲まれた中心の硫黄原子が形成され、二塩化硫酸にその特徴的な構造が与えられます。
塩化スルフリルの溶解度
二塩化硫酸は水に溶けにくいです。水と反応して塩酸と硫酸を生成し、加水分解反応性を高めます。ただし、二塩化硫酸は塩素化炭化水素や芳香族化合物などの有機溶媒にある程度の溶解性を示すため、特定の用途に適しています。
| 外観 | 無色の液体 |
| 比重 | 1,638g/mL |
| 色 | 該当なし |
| 匂い | 辛くて息が詰まる |
| モル質量 | 134.97 g/モル |
| 密度 | 1,638g/mL |
| 融合点 | -54℃ |
| 沸点 | 69℃ |
| フラッシュドット | 該当なし |
| 水への溶解度 | 激しく反応する |
| 溶解性 | 塩素化炭化水素や芳香族化合物などの有機溶媒に可溶 |
| 蒸気圧 | 43.6mmHg(25℃にて) |
| 蒸気密度 | 4.43 (空気 = 1) |
| pKa | 該当なし |
| pH | 該当なし |
塩化スルフリルの安全性と危険性
二塩化硫酸はいくつかの安全上の問題を引き起こすため、取り扱う際には注意が必要です。これは腐食性物質であり、接触すると皮膚、目、気道に重度の火傷を引き起こす可能性があります。その蒸気を直接吸入すると、呼吸器への刺激や肺の損傷を引き起こす可能性があります。水と激しく反応して有毒ガスを発生し、爆発の危険性があります。したがって、二塩化硫酸を取り扱う場合は、換気の良い場所で行い、手袋、ゴーグル、呼吸保護具などの適切な保護具を着用することが重要です。流出した場合は、適切な手順を使用して直ちに拭き取り、不適合物質から離れた涼しく乾燥した場所に保管する必要があります。
| ハザードシンボル | 腐食性(C)、酸化性(O) |
| セキュリティの説明 | 重度の皮膚火傷や目の損傷を引き起こします。水と激しく反応する。 |
| 国連識別番号 | UN 1834 (二塩化硫酸) |
| HSコード | 28121000 |
| 危険等級 | 8 (腐食性物質) |
| 梱包グループ | II(中危険) |
| 毒性 | 非常に有毒です。飲み込んだり、吸入したり、皮膚から吸収されたりすると有害です。 |
塩化スルフリルの合成方法
一般に、二塩化硫酸を合成するためにいくつかの方法が使用されます。
1 つの方法には、二酸化硫黄 (SO2) と塩素ガス (Cl2)の間の反応が含まれます。活性炭や塩化アルミニウムなどの触媒の存在下で、ガスは反応して二塩化硫酸 (SO2Cl2) を形成します。この反応は通常、約 100 ~ 200°C の高温で発生します。
二塩化硫黄を合成する別の方法には、三酸化硫黄 (SO3) と塩化水素 (HCl) の反応が含まれます。制御された条件下では、これら 2 つの化合物が結合して二塩化硫酸が生成されます。この反応は発熱性であり、通常は気相で起こります。
塩化チオニルプロセスでは、硫酸 (H2SO4) と五塩化リン (PCl5)の室温反応により二塩化硫酸が生成されます。この反応では、二塩化硫酸のほか、リン酸 (H3PO4) や塩化水素 (HCl) などの副生成物が生成されます。産業環境では一般的にこの方法が使用されます。
これらの合成方法では、含まれる物質の反応性と危険な性質のため、試薬の慎重な取り扱いと安全上の注意事項の考慮が必要であることに注意することが重要です。
さらに、化学者は反応条件を制御し、二塩化硫酸の合成を確実に成功させるために、凝縮器や還流システムなどの適切な装置を使用することがよくあります。
塩化スルフリルの用途
二塩化硫酸 (SO2Cl2) は、その独特の特性により、さまざまな産業でさまざまな用途に使用されています。二塩化硫酸の主な用途をいくつか紹介します。
- 化学試薬: 有機合成では通常、二塩化硫酸を多用途化学試薬として使用します。二塩化硫酸は塩素化、スルホン化、エステル化などのさまざまな反応に積極的に関与し、有機化合物に塩素、硫黄、または酸の官能基を導入できます。
- 殺虫剤と燻蒸剤: 二塩化硫酸は、貯蔵穀物、製粉工場、食品加工施設で害虫を防除するための強力な燻蒸剤として機能し、その強力な殺生物特性により貯蔵されている農産物に損害を与える可能性のある昆虫、幼虫、害虫を積極的に除去します。
- 重合: 塩化ビニルなどの特定のモノマーの重合では、二塩化硫酸が活性触媒または開始剤として機能し、建設、自動車、電気産業で広く使用されている熱可塑性ポリマーであるポリ塩化ビニル (PVC) の製造を促進します。
- 医薬品: 二塩化硫酸は、さまざまな感染症の治療に使用される必須の抗生物質や治療薬である医薬化合物、特にスルホンアミドの合成において重要な役割を果たしています。
- 染料の製造: 二塩化硫酸は、染料、特に硫黄または塩素を含む染料の製造に積極的に関与します。目的の官能基を積極的に導入し、堅牢度や染料の安定性を向上させます。
- 化学中間体: 二塩化硫酸は、二酸化硫黄、硫酸、塩化スルホニルなどの他の化学物質の合成における活性中間体として機能し、洗剤製造、プラスチック製造、医薬品などの多くの産業で用途が見出されます。
- 水処理: 水の浄化と消毒の場合、二塩化硫酸は水源に存在する有害な細菌、ウイルス、その他の微生物を積極的に中和し、除去します。
- 実験室での応用: さまざまな実験室手順では、たとえば、第一級および第二級アミンの検出と測定などに二塩化硫酸が積極的に使用されています。アミンと積極的に反応して安定したスルホンアミドを形成し、その分析と特性評価を容易にします。
質問:
Q: 13.5 g の塩化スルフリル中の SO2Cl2 のグラム分子の総数は何ですか?
A: 13.5 g の塩化スルフリル中の SO2Cl2 のグラム分子の総数は、指定された質量を SO2Cl2 のモル質量で割ることによって計算できます。
Q: SO2Cl2 は極性ですか、それとも無極性ですか?
A: SO2Cl2 は極性結合の存在と非対称な分子構造により極性分子です。
Q: SO2Cl2 の圧力はいつ低下しますか?
A: SO2Cl2 の圧力降下は、温度、体積、反応条件などのさまざまな要因に依存します。これは時間だけでは判断できません。
Q: この混合物中の SO2Cl2 の分圧はどれくらいですか?
A: 混合物中の SO2Cl2 の分圧は、温度、体積、SO2Cl2 のモル分率または濃度に応じて、理想気体の法則を使用して決定できます。
Q: SO2Cl2 分子間にはどのようなタイプの分子間力が予想されますか?
A: SO2Cl2 分子間の予想される分子間力には、双極子間相互作用とロンドン分散力が含まれます。
Q: SO2Cl2 の分圧はどの時点で初期値の 10 分の 1 に減少しますか?
A: SO2Cl2 の分圧が初期値の 10 分の 1 に減少するのに必要な時間は、システムの特定の条件と関与する化学反応の速度によって異なります。
Q: SO2Cl2 のモル質量はどれくらいですか?
A: SO2Cl2 のモル質量は、1 モルあたり約 134.97 グラムです。
Q: SO2Cl2 の分子構造は何ですか?
A: SO2Cl2 の分子構造は湾曲または V 字型で、中心の硫黄原子が 2 つの酸素原子と 2 つの塩素原子に結合しています。
Q: SO2Cl2 のルイス構造は何ですか?
A: SO2Cl2 のルイス構造は、酸素原子に二重結合した硫黄原子と、別の酸素原子に結合した単結合で構成され、硫黄原子には 2 つの塩素原子が結合しています。
